Материал: Фарм производство БАР
По спектру действия:
антибактериальные, губительно действующие на грамположительные (бензилпенициллин, ристомицин, новобиоцин), грамотрицательные (полимиксин) бактерии, а также антибиотики широкого спектра действия (левомицетин, канамицин, мономицин, гентамицин);
противогрибковые (амфотерицин В, нистатин, леворин, гризеофу-
львин);
противоопухолевые, включающие в себя: актиномицины, антракциклины (доксорубицин, эпирубицин, идарубицин), оливомицины, брунеомицины, блеомицины.
В зависимости от химической структуры и ряда других свойств антибиотики делят на ряд классов:
1.-лактамные – пенициллины, цефалоспорины, причем составляют более 40 % рынка антибиотиков.
2.Макролиды – макроциклические (эритромицин, джозамицин, олеандомицин).
3.Аминогликозиды – (стрептомицин, канамицин, гентамицин, амикацин, тобрамицин).
4.Тетрациклины – тетрациклин, метациклин.
5.Гликопептиды – ванкомицин, ристомицин, блеомицин.
6.Антрациклины – доксорубицин, эпирубицин, идарубицин.
7.Амфениколы – левомицетин.
8.Линкосамиды – линкомицин.
9.Полиеновые – ациклические (нистатин, леворин).
10.Полипептиды – полимиксин, грамицидин.
Мы считаем целесообразным привести химическую структуру широко используемых антибиотиков (табл. 2).
28
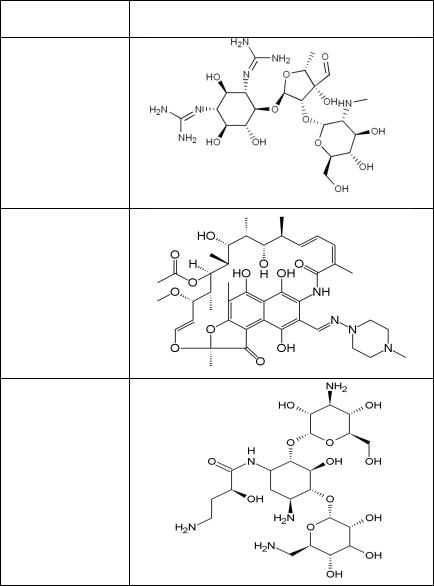
Таблица 2 – Химическая структура антибиотиков
Антибиотик |
Химическая структура |
|
|
1 |
2 |
Стрептомицин
Рифампицин
Амикацин
29
Продолжение таблицы 2 |
|
|
Продолжение таблицы 2 |
|
|
|
|
|
|
1 |
2 |
1 |
2 |
|
|
|
|
|
|
|
|
|
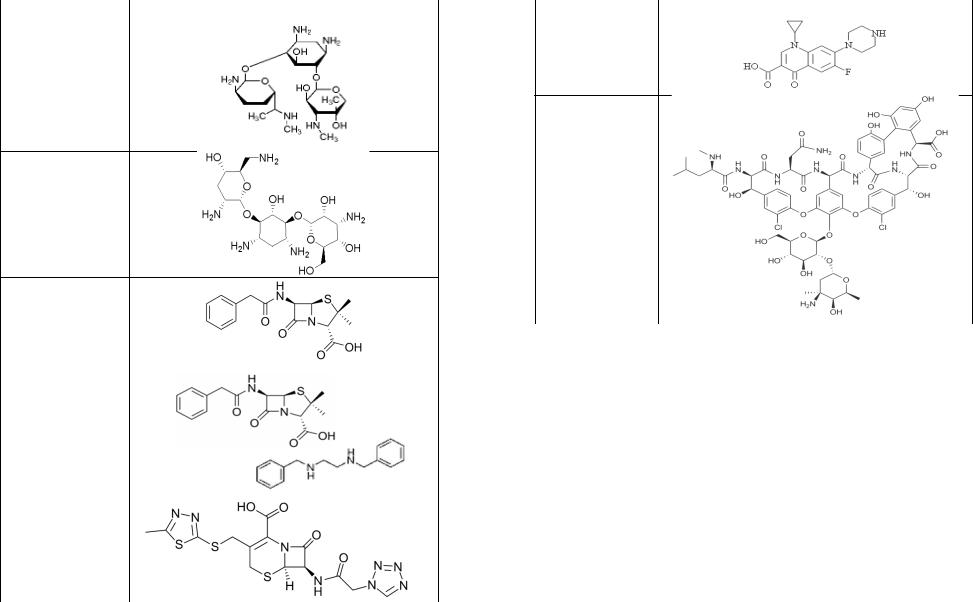
Ципрофлоксацин |
|
Гентамицин |
|
|
|
|
Тобрамицин |
Ванкомицин |
Бензилпенициллин |
|
|
|
Анализируя влияние антибиотиков на бактерии и клетки (молекуляр- |
|
|
|
|
|
|
ный механизм) можно определить их действие как: |
|
||
|
|
1. Подавление активности микробных ферментов, ответственных за |
|
|
синтез клеточной мембраны (амоксициллин, цефалоспорины, пеницилли- |
Бензатина- |
|
ны, ампициллин), например, путем конкурентного блокирования транс- |
бензилпенициллин |
|
пептидаз, участвующих в синтезе мукопептида, входящего в состав кле- |
|
|
точной мембраны. |
|
|
2. Подавление в микробной клетке синтеза белка путем взаимодей- |
|
|
ствия с 50S рибосомальной субъединицей бактерий (кларитромицин, |
|
||
|
|
клиндамицин). |
|
|
3. Непосредственное взаимодействие с ДНК, что препятствует синте- |
Цефазолин |
|
зу нуклеиновых кислот (противоопухолевое действие: антрациклиновые |
|
|
антибиотики – доксорубуцин, эпирубцин, идарубицин и др.; блеомицин, |
|
|
митомицин). |
|
|
|
30 |
31 |
|
4.Нарушение движения рибосомы по нити информационной РНК (эритромицин, линкомицин).
5.Нарушение целостности цитоплазматической мембраны (противогрибковые антибиотики – нистатин, амфотерицин В, полимиксины и др.).
6.Нарушение прикрепления РНК к рибосомам (тетрациклины, макролиды, левомицитин).
7.Селективное ингибирование ДНК-зависимой РНК полимеразы в микробной клетке (рифампицин).
8.Нарушение энергетического обмена (олигомицин).
В табл. 3 представлены продуценты и характеристика антибиотиков.
Таблица 3 – Продуценты и характеристика антибиотиков
|
|
|
Спектр |
|
Антибиотик |
Продуцент |
Химическая |
и |
|
природа |
механизм |
|||
|
|
|||
|
|
|
действия |
|
|
|
|
|
|
1 |
2 |
3 |
4 |
|
|
|
|
|
|
Амикацин |
Получают полу- |
С22Н43N5O13, 585,61 Да |
Грамотрицательные |
|
|
синтетическим |
Аминогликозид |
и грамположитель- |
|
|
путем из |
|
ные бактерии |
|
|
канамицина А |
|
|
|
|
|
|
|
|
Амфотерицин В |
Streptomyces |
С47Н73NO17, 926,12 Да |
Дрожжи, дрожже- |
|
|
nodosus |
Полиеновый |
подобные грибы, |
|
|
|
антибиотик |
включая |
|
|
|
|
Candida albicans |
|
|
|
|
|
|
Бацитрацин |
Bacillus subtilis |
Полипептид |
Грамположительные |
|
|
|
|
бактерии |
|
|
|
|
|
|
Бензилпенициллин |
Penicillium |
С16Н18N2O4S, 334,4 Да |
Грамотрицательные |
|
|
notatum |
Гетероциклическое |
и грамположитель- |
|
|
|
соединение, постро- |
ные бактерии |
|
|
|
енное из сконденсиро- |
|
|
|
|
ванных тиазолидино- |
|
|
|
|
вого и беталактмного |
|
|
|
|
кольца |
|
|
|
|
|
|
|
Блеомицин |
Streptomyces |
С55Н84N20O21 S2 |
Противоопухолевое |
|
|
verticillus |
С55Н84N17O21S3 |
средство. Вызывает |
|
|
|
Гликопептид |
фрагментацию мо- |
|
|
|
|
лекул ДНК |
|
|
|
|
|
|
|
|
32 |
|
Продолжение таблицы 3
1 |
2 |
3 |
4 |
|
|
|
|
Ванкомицин |
Amycolatopsis |
С66Н75N9O24 |
Грамположитель- |
|
orientalis |
Трициклический |
ные бактерии. Ин- |
|
|
гликопептид |
гибирует биосин- |
|
|
|
тез клеточных |
|
|
|
мембран, изменяет |
|
|
|
их проницаемость, |
|
|
|
нарушает синтез |
|
|
|
РНК |
|
|
|
|
Гентамицин |
Micromonospora |
С21Н43N5O7, 418,54 Dа |
Грамположитель- |
|
purpurea |
Аминогликозид |
ные и грамотрица- |
|
|
|
тельные бактерии |
|
|
|
|
Джозамицин |
Streptomyces |
С42Н69NO15, 828,02 Dа |
Грамположитель- |
|
narbonensis var. |
Макролид |
ные и грамотрица- |
|
Josamyceticus var. nova |
|
тельные бактерии |
|
|
|
|
Доксорубицин |
Streptomyces peucetius |
С27Н29NO11, 543,53 Dа |
Противоопухоле- |
|
var. Caesius |
Антрациклиновый ан- |
вое средство. Вза- |
|
|
тибиотик |
имодействует с |
|
|
|
ДНК и препят- |
|
|
|
ствует синтезу |
|
|
|
нуклеиновых кис- |
|
|
|
лот |
|
|
|
|
Канамицин А |
Streptomyces |
С18Н36N4O11, 484,51 Dа |
Грамположитель- |
|
kanamyceticus |
Аминогликозид |
ные и грамотрица- |
|
|
|
тельные бактерии |
|
|
|
|
Линкомицин |
Streptomyces |
С18Н34N2O6S, 406,55 Dа |
Грамположитель- |
|
lincolnensis var. |
Линкозамиды |
ные бактерии |
|
Lincolnensis |
|
|
|
|
|
|
Митомицин С |
Streptomyces |
С15Н18N4O5, 334,33 Dа |
Противоопухоле- |
|
caespitosus |
|
вое средство. Вза- |
|
|
|
имодействует с |
|
|
|
ДНК и препят- |
|
|
|
ствует синтезу |
|
|
|
нуклеиновых кис- |
|
|
|
лот |
|
|
|
|
Мономицин |
Streptomyces circulatus |
С23Н45N5O14, 615,6 Dа |
Лейшманиоз, ток- |
|
var. |
Аминогликозид |
соплазмоз, саль- |
|
Monomycini |
|
монеллез |
|
|
|
|
|
|
33 |
|
Продолжение таблицы 3
1 |
2 |
3 |
4 |
|
|
|
|
Нистатин |
Streptomyces noursei |
С47Н75NO17, 276,42 Dа |
Дрожжеподобные |
|
|
Антибиотик |
грибы рода Candida |
|
|
полиеновой группы |
|
|
|
|
|
Полимиксин |
Bacillus polymyxa |
Полипептид |
Грамотрицательные |
|
|
|
и грамположитель- |
|
|
|
ные бактерии |
|
|
|
|
Рифампицин |
Streptomyces |
С42Н58N4O12, 822,96 Dа |
Грамположительные |
|
mediterranei |
|
и грамотрицательные |
|
|
|
бактерии, включая |
|
|
|
микобактерии тубер- |
|
|
|
кулеза и лепры |
|
|
|
|
Рубомицина |
Streptomyces |
С27Н29NO10HCI, |
Противоопухолевое |
гидрохлорид |
coeruleorubidis |
563,98 Dа |
|
|
|
|
|
Стрептомицин |
Streptomyces griseus |
С21Н39N7O12, 581,58 Dа |
Грамотрицательные |
|
|
Аминогликозид |
бактерии и микобак- |
|
|
|
терии туберкулеза |
|
|
|
|
Тетрациклин |
Streptomyces |
С22Н24N2O8, 444,45 Dа |
Грамположительные |
|
aureofaciens |
|
и грамотрицательные |
|
|
|
бактерии. Нарушает |
|
|
|
образование ком- |
|
|
|
плекса между транс- |
|
|
|
портной РНК и ри- |
|
|
|
босомой, приводя к |
|
|
|
нарушению синтеза |
|
|
|
белка |
|
|
|
|
Тобрамицин |
Streptomyces |
С18Н37N5O9, 467,52 Dа |
Грамотрицательные |
|
tenebrarius |
Аминогликозид |
бактерии |
|
|
|
|
Цефалоспорин С |
Cephalospororium sp. |
С16Н21N3O8S |
Грамположительные |
|
|
|
и грамотрицательные |
|
|
|
бактерии |
|
|
|
|
Эритромицин |
Streptomyces erythreus |
С37Н67NO13, 733,95 Dа |
Грамположительные |
|
|
Макролид |
бактерии |
|
|
|
|
34
2.3. Пути биотехнологического получения антибиотиков
Необходимость поисков новых антибиотиков обусловлена многими причинами. Постоянно ведутся поиски эффективных антибиотиков для борьбы с теми заболеваниями, на возбудители которых не действуют существующие препараты. Потребность в антибиотиках обусловлена также тем, что при их использовании в лечебных целях происходит накопление резистентных к этим соединениям форм организмов. Длительное и не всегда оправданное применение антибиотиков приводит зачастую к ускорению эволюции патогенных организмов в сторону закрепления их устойчивости к этим препаратам. Поэтому необходимо постоянно заменять одни виды антибиотиков на другие. Для этого нужно находить наиболее активные микроорганизмы – продуценты антибиотиков.
Основные этапы поисков антибиотиков:
выделение микробов-антагонистов из почвы;
определение антагонистического спектра и активности антибиоти-
ков;
подбор условий культивирования продуцентов антибиотиков;
выделение и химическая очистка антибиотиков;
изучение физико-химических и фармакологических свойств антибиотиков;
испытание химико-терапевтической эффективности;
идентификация антибиотиков.
Биосинтез антибиотиков – наследственная особенность организмов, проявляющаяся в том, что каждый вид (штамм) способен образовывать один или несколько вполне определенных, строго специфичных для него антибиотических веществ. Вместе с тем известно, что одинаковые антибиотики могут образовываться несколькими видами организмов.
Выявление потенциальной возможности образовывать в процессе жизнедеятельности антибиотики связано с условиями культивирования организмов. В одних условиях организм образует антибиотик, в других условиях тот же организм не будет обладать способностью синтезировать антибиотическое вещество.
35
В связи с резистентностью микроорганизмов к антибиотикам постоянно проводится их совершенствование, что приводит к появлению новых поколений. Например, цефалоспориновые антибиотики, приводящие к нарушению синтеза компонентов клеточной мембраны, присутствуют в виде 4-х поколений полусинтетических цефалоспориновых антибиотиков: Цефадроксил, Цефазолин, Цефалексин – 1 поколение; Цефамандол, Цефуроксим – 2 поколение; Цефиксим, Цефоперазон, Цефотаксим, Цефтазидим, Цефтриаксон – 3 поколение; Цефпиром, Цефепим – 4 поколение.
Основными продуцентами антибиотиков являются актиномицеты, плесневые грибы, бактерии. Главным местом их обитания является почва. Для выделения микроорганизмов, образующих антибиотики, берут пробы почвы, высушивают ее до воздушно-сухого состояния и делают высевы на специальные питательные среды.
Выделенные штаммы-продуценты антибиотиков часто вариабельны и нестабильны. Поэтому методом селекции отбирают наиболее перспективные штаммы, а затем проводят отбор индуцированных мутантов. Мутантное действие на микроорганизмы достигается применением различных источников лучистой энергии (УФ-лучи, рентгеновские лучи, нейтроны и др.).
Антибиотики продуцируются плесневыми грибами, актиномицетами, эубактериями и рядом других микроорганизмов. Некоторые из этих организмов способны продуцировать большое количество антибиотиков. Так, шесть родов филаментозных грибов производят 1000 различных антибиотиков, в том числе пенициллин и цефалоспорин, а три рода актиномицетов – 3000 антибиотиков. Среди актиномицетов наибольший вклад вносит род Streptomyces, один из видов которого S. griseus синтезирует более 50 антибиотиков. В процессе образования антибиотиков задействовано значительное число генов. Массовая расшифровка первичной структуры геномов микроорганизмов показала, что эта величина равна 1–2 %. Так, у Bacillus subtilis число таких генов достигает 2 %, что обеспечивает микроорганизму большие возможности для защиты и адаптации. С другой стороны, это обстоятельство затрудняет анализ путей биосинтеза антибиотиков и идентификацию отдельных мутаций, способных увеличить выход продукта. Тем не менее, большинство известных в настоящее время
36
высокопродуктивных штаммов продуцентов антибиотиков получено традиционными методами мутагенеза и селекции.
Выделенные культуры микроорганизмов-антагонистов изучают по содержанию в них антибиотических веществ, необходимых для практических целей. При этом методом хроматографии определяют наличие известных антибиотиков. Если обнаруживают новый антибиотик, то вначале осуществляют первичное выделение и химическую очистку антибиотика, определяют его токсичность и химико-терапевтические свойства на животных, зараженных возбудителями различных заболеваний.
Биосинтез молекулы любого антибиотика происходит с участием ряда ферментов – от нескольких единиц до нескольких десятков. Координация действия ферментов, т.е. обеспечение правильной последовательности ферментативных реакций, обеспечивается разными, не всегда еще ясными путями.
Процесс развития микроорганизмов (продуцентов антибиотиков) имеет, как правило, двухфазный характер:
В первой фазе развития культуры, носящей название трофофазы
(тропофазы) (фаза сбалансированного роста микроорганизма), идет интенсивное накопление биомассы продуцента. Продуцент синтезирует белки, нуклеиновые кислоты, углеводы, ферменты и другие биологически активные вещества (БАВ), необходимые для роста микроорганизма; наблюдается быстрое потребление основных компонентов субстрата (источников углерода, азота, фосфора и др.), интенсивное поглощение кислорода. В культуральной среде может снижаться рН, как результат накопления органических кислот. В трофофазе антибиотик, как правило, не образуется или его количество незначительное. Возможно, в этой фазе синтез ферментов, принимающих участие в образовании антибиотика, подавлен.
Вторая фаза развития культуры, носящая название идиофазы (фаза несбалансированного роста) характеризуется снижением общего количества биомассы. В период второй фазы происходит развитие микроорганизма и образование новых клеток, но в культуре начинают преобладать автолитические процессы, что приводит к снижению общего числа биомассы. Продукты метаболизма микроорганизмов частично используются на построение клеток мицелия, частично – на синтез антибиотика. Среда обога-
37