Материал: Фарм производство БАР
ций не бывает 100 %-ой. Для отбора используют схемы, позволяющие идентифицировать трансформированные клетки.
Эффективным методом трансформации E. Coli плазмидами является электропорация (воздействие на клеточные мембраны электрическим током для увеличения их проницаемости). Необходимо отметить, что электропорация в настоящее время самый эффективный и удобный, но довольно дорогой метод, используемый для генетической трансформации бактерий. Для введения клонированных генов в соматические клетки
также применяют микроинъекции и микроукалывания или слияние с клеткой нагруженных ДНК мембранных везикул (липосом).
Бактериофаги – используются в качестве носителей генетической информации. Рекомбинантный ген встраивается в геном вируса и в последующем реплицируется с генами вируса при размножении в инфицированной клетке-хозяине. С этой целью применяют бактериофаг лямбдавирус с двухцепочечной ДНК, которая после проникновения в клетку смыкается в кольцо. Бактериофаг М-13 – вирус нитевидной формы с кольцевой замкнутой ДНК, которая в клетке превращается в двухцепочечную и реплицируется в клетках-потомках. В поисках эукариотических систем экспрессии, для получения биологически активных белков, созданы бакмиды – экспрессирующие векторы на основе бакуловирусов для E. Coli и клеток насекомых. Выход рекомбинантных бакуловирусов в такой системе повысился до 99 %. Клетки насекомого, инфицированные бакуловирусами, синтезировали гетерологичный белок. Векторы на основе фага удобны для создания клонеток (банка генов), но не для тонких манипуляций с фрагментом ДНК. Для детального изучения и преобразования фрагменты ДНК переклонируют в плазмиды.
Кроме указанных векторов в генной инженерии применяют космиды – плазмиды, несущие cos-участок (комплементарные липкие концы) ДНК фага лямбда. Наличие cos-участка позволяет проводить упаковку ДНК в головку фага in vitro, что обеспечивает возможность их введения в
клетку путем инфекции, а не трансформации.
Фазмиды – это гибриды между фагами и плазмидами. Они способны развиваться как фаг и как плазмида. Уступая космидам по клонирующей
18
емкости, фазмиды дают возможность отказаться от переклонирования генов из фаговых в плазмидные векторы.
Заключение
Таким образом, для получения любого белкового продукта необходимо обеспечить транскрипцию кодирующего его гена и трансляцию соответствующей мРНК. Для инициации транскрипции (синтеза РНК) в нужном сайте необходим промотор, для её остановки – терминирующий кодон.
Методика по клонированию включают следующие биотехнологические этапы:
1.Рестриктазное расщепление из организма-донора нужных генов нативной ДНК (клонируемая ДНК, встраиваемая ДНК, ДНК-мишень, чужеродная ДНК);
2.Быстрая расшифровка всех нуклеотидов в очищенном фрагменте ДНК, позволяющая определить точные границы гена и аминокислотную последовательность, кодируемую геном;
3.Обработка рестрикционными эндонуклеазами вектора для клонирования, который может реплицироваться в клетке-хозяине;
4.Сшивание ДНК-лигазой двух фрагментов ДНК с образованием новой рекомбинантной молекулы – конструкция «клонирующий вектор – встроенная ДНК»;
5.Введение этой конструкции в клетку-хозяина (реципиента), где она реплицируется и передается потомкам. Этот процесс называется трансформацией. После трансформации бактериальная клетка воспроизводит фрагмент клонируемой ДНК миллионами идентичных клеток;
6.Идентификация и отбор клеток, несущих рекомбинантную ДНК (трансформированные клетки);
7.Получение специфического белкового продукта, синтезированного клетками-хозяевами.
Таким образом, технология рекомбинантных ДНК включает целый набор процедур, благодаря которым удается клонировать фрагменты ДНК,
19
содержащие специфические гены. Для отбора клеток, содержащих рекомбинантную ДНК, используют специальные приемы. Чтобы уменьшить количество кольцевых плазмидных молекул, образующихся при сшивании фрагментов ДНК-лигазой Т4, рестрицированную плазмидную ДНК обрабатывают щелочной фосфатазой, удаляющей 5′–концевые фосфатные группы. Для отбора трансформированных клеток, содержащих гибридные плазмиды, проводят: 1) тестирование на резистентность к определенным антибиотикам или колориметрическую реакцию; 2) иммунологические тесты или выявление специфического белка – продукта клонированного гена; 3) гибридизацию с зондом, комплементарным какому-либо участку искомого гена. Чтобы иметь возможность клонировать целый ген, донорскую ДНК расщепляют лишь частично. При этом получаются фрагменты разной длины, из которых затем создают геномную библиотеку. Для клонирования крупных фрагментов ДНК были сконструированы векторы на основе бактериофагов лямбда и З1-го, а также плазмиды F. Для получения фрагментов ДНК, кодирующих эукариотические белки, на очищенной мРНК как на матрице синтезируют комплементарную цепь ДНК с помощью обратной транскриптазы; эта цепь в свою очередь используется в качестве матрицы для синтеза второй цепи. После ферментативной обработки эту двухцепочечную комплементарную ДНК встраивают в вектор. Независимо от того, какая именно стратегия клонирования используется, после идентификации клонированной последовательности необходимо показать, что она представляет собой нативный структурный ген.
Весьма перспективным направлением генно-инженерных исследова-
ний является создание рекомбинантных препаратов на основе пробиоти-
ков. После того как было установлено, что ряд бактерий способны проявлять пробиотические свойства и благотворно влиять на здоровье человека, началось использование технологии рекомбинантных ДНК с целью получения генетически измененных штаммов и создание пробиотических или производственных культур с заданными уникальными свойствами.
Несомненный интерес представляет один из первых рекомбинантных пробиотиков («Субалин»), разработанный специалистами Украины и Рос-
20
сии. Предложен препарат, который помимо высокой антагонистической активности по отношению к патогенным и условно патогенным бактериям проявлял антивирусную активность благодаря введению генетической информации, которая кодирует продукцию антивирусной субстанции – α-2- интерферона. Для этой цели были отобраны несколько штаммов B. subtilis. Трансформацию отобранных бактериальных культур проводили плазмидами рВМВ, которые кодируют синтез секреторного (рВМВ 105) и внутриклеточного (рВМВ 104) интерферона. Указанные плазмиды содержат ген интерферона в виде химически-синтезированного аналога гена человеческого лейкоцитарного α-2-интерферона. В структуре плазмиды рВМВ 105 ген интерферона связан с геном сигнального пептида, гомологической последовательности гена α-амилазы, который обеспечивает эффективную секрецию из клеток гетерологичного белка. Плазмида рВМВ 104 не имеет в своей структуре такой последовательности нуклеотидов перед геном интерферона в связи с чем продуцируемый белок остается внутри клетки. При изучении стабильности плазмид в разных штаммах бацилл установлено, что максимальной стабильностью обладает плазмида рВМВ 105 в штаммме B .subtilis. Даже через 10 пассажей обнаруживалась 100 %-ая сохранность плазмиды. На разных экспериментальных инфекциях на животных изучена и подтверждена эффективность и безопасность препарата «Субалин» при пероральном введении. Интерферон α-2 человека был обнаружен во всех тестируемых органах лабораторных животных. Максимальное количество интерферона зарегистрировано в печени, легких и кишечнике.
Применение плазмидных векторов используют для создания рекомбинантных штаммов бифидобактерий. Так, например, в Японии в настоящее время осуществляются интенсивные исследования по использованию модифицированных генно-инженерными методами штаммов бифидобактерий для терапии онкологических заболеваний. Основанием для этого является тот факт, что штаммы бифидобактерий после системного введения способны селективно локализоваться и быстро пролиферировать в границах солидных опухолей. Используя анаэробные и непатогенные бактерии
21
B. Longum, в экспериментах удалось доставить в опухоль определенные терапевтические гетерологичные гены, в том числе компоненты системы пролекарство – фермент – лекарство. Для этой цели была сконструирована плазмида рBLES 100S-eCD, включающая ген цитозиндезаминазы. Трансформированные этой плазмидой B. longum были способны продуцировать цитозиндезаминазу в гипоксических опухолях, что приводило к локальной конверсии системно вводимого нетоксичного 5-фторцитозина в токсичное для тканей соединение 5-фторурацил. Противоопухолевый эффект от применения этого продукта был продемонстрирован на модели крыс с опухолями молочных желез при введении трансформированных B. longum непосредственно в область опухоли или внутривенно. При этом анаэробная B. longum накапливается в гипоксических солидных опухолях (анаэробная среда опухоли). В настоящее время проходит испытания противоопухолевый препарат рекомбинантных бифидобактерий (продуцирует цитозиндезаминазу) под кодовым названием «APS001» селективно накапливающийся в гипоксической среде опухоли. Созданы рекомбинантные штаммы бифидобактерий, являющиеся продуцентами ферментов: α-амилазы и глутаматдегидрогеназы.
Таким образом, сегодня генно-инженерная технология позволяет получать штаммы-продуценты многих белковых субстанций: ферментов, различных факторов, гормонов, вакцин, цитокинов и других компонентов фармацевтических препаратов. Кроме того, несомненный интерес представляют рекомбинантные штаммы пробиотиков, например, бифидобактерий или бацилл, которые, попадая в организм человека или животных способны продуцировать запрограммированные биологически активные вещества.
22
Контрольные вопросы
1.Что такое эндонуклеазы рестрикции типа II и почему они так важны для технологии рекомбинантных ДНК?
2.Опишите применение плазмиды hBR322 в качестве вектора. Какими особенностями они обладают?
3.Опишите основные преимущества и недостатки использования в качестве штаммов продуцентов рекомбинантных белков дрожжей и бактерий.
4.Что означает процесс «электропорация» и для чего её применяют?
5.Опишите структуру плазмид и охарактеризуйте плазмидные век-
торы.
6.Опишите способы введения рекомбинантных плазмид в грамотрицательную бактерию, например, E. Coli.
7.Какова структура бактериофагов?
8.Привести примеры фармацевтических субстанций на основе рекомбинантных белков.
9.Что представляет собой банк клонов и каким образом создаются банки клонов?
10.Почему часто прибегают к частичному гидролизу для создания банков клонов?
11.Каковы отличительные особенности прокариотической клетки?
12.Каковы отличительные особенности эукариотической клетки?
13.Указать основные биотехнологические этапы методики клониро-
вания.
14.Каковы основные методы анализа генетически модифицированных организмов?
15.Что представляют собой трансгенные животные? Охарактеризуйте технологию их получения.
16.Классификация векторов, применяемых в генной инженерии.
17.Привести данные об областях применения рекомбинантных микроорганизмов.
18.Какие преимущества у рекомбинантных штаммов пробиотических микроорганизмов?
23
ГЛАВА 2. ПОЛУЧЕНИЕ АНТИБИОТИКОВ
2.1. Этапы развития производства антибиотиков
Широкое применение антибиотиков для лечения инфекционных заболеваний помогло сохранить миллионы жизней. Большинство основных антибиотиков получено из грамположительной почвенной бактерии Streptomyces. В тоже время существует ряд антибиотиков, выделенных и из других грамположительных и грамотрицательных бактерий.
Историю развития науки об антибиотиках можно представить следующим образом:
1870 г. – Д. Сандерсон обнаружил отсутствие роста бактерий в среде, содержащей плесень;
1872 г. – Д. Листер доказал способность Penicillium glaucum подавлять рост бактерий;
1871–1872 г.г. – А. Г. Полотебневым показано, что молодая культура зеленой плесени – грибы рода Penicillium способны задерживать развитие возбудителей кожных заболеваний человека;
1877 г. – Пастер Л., Джеберт С., Лебединский И. опубликовали сообщение о росте Bacillus anthracis анаэробными бактериями;
1889 г. – А. Вюимен предложил термин «антибиотик», обозначающий действующий агент процесса «антибиоза», т.е. сопротивления, оказываемого одним живым организмом другому;
1894 г. – И. И. Мечников обратил внимание на возможность использования некоторых сапрофитных бактерий в борьбе с патогенными микроорганизмами;
1929 г. – А. Флеминг впервые выделил комплекс пенициллинов из
Penicillium notanum;
1939 г. – Р. Дюбо впервые выделил тиротрицин из почвенной споровой аэробной палочки Bacillus brevis;
1940 г. – Х. Флори, Дж. Чейн выделена субстанция пенициллина;
1941 г. – начато клиническое применение очищенного пеницил-
лина;
24
1942 г. – М. Г. Бражникова и Г. Ф. Гаузе выделили грамицидин С.
1944 г. – С. А. Ваксман открыл стрептомицин, образуемый лучи-
стыми грибами рода Actinomyces (Streptomyces griseus).
Применение пенициллина в борьбе с различными инфекционными заболеваниями (пневмонии, сепсиса, гнойных инфекций кожи, дифтерии, сифилисе, гонореи, скарлатине и др.) и воспалительными процессами явилось мощным стимулом для поиска новых, еще более эффективных антибиотических веществ, образуемых различными группами микроорганизмов (бактериями, актиномицетами), низшими растениями (дрожжами, водорослями, плесневыми грибами, высшими грибами), высшими растениями и животными организмами.
2.2.Классификация и структура антибиотиков
Ядро молекулы пенициллина – 6-аминопенициллановая кислота (6-АПК) – состоит из 4-членного -лактамного (А) и 5-членного тиазолидинового (В) колец (см. рис. 1). Пенициллины отличаются характером радикала в боковой цепи. Наиболее ценным оказался бензилпенициллин (радикал = СН2–С6Н5) поэтому при выращивании гриба продуцента, например, Penicillium crustosum процесс биосинтеза направляют в сторону образования преимущественно бензилпенициллина. После выделения в 1959 году из Penicillium chrysogenum 6-АПК появилась возможность химического синтеза новых пенициллинов путем присоединения к ним различных радикалов к свободной аминогруппе. Известно более 15000 полусинтетических пенициллинов, однако лишь немногие превосходят пенициллин по антибактериальной активности (ампициллин, оксациллин и др.). Пенициллины выпускаются в виде хорошо растворимых в воде натриевых и калиевых солей.
25
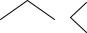
|
|
|
|
|
|
|
|
|
|
|
|
S |
|
CH3 |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
H2N |
|
|
C |
|
|
|
|
|
C |
|
B |
|
C |
CH3 |
||
|
|
|
A |
|||||||||||||
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
|
COOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
C |
|
|
N |
|
|||||||||
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|||||||||
Рисунок 1 – Структура молекулы пенициллина – 6-аминопенициллановая кислота
Стрептомицин – антибиотик широкого спектра действия. Активен в отношении туберкулезных бактерий, возбудителей чумы, туляремии, стрептококков, стафилококков, пневмококков, гонококка и др. По химической природе стрептомицин относится к аминогликозидным антибиотикам.
Эритромицин – антибиотик из группы макролидов, продуцентом которого является почвенный гриб Streptomyces erythreus. Активен в отношении грамположительных (стафилококки, стрептококки, пневмококки и др.) и грамотрицательных бактерий, например, бруцелл. Эффективен в отношении стафилококков устойчивых к пенициллину, тетрациклинам, стрептомицину.
Со времен открытия пенициллина в конце 20-х годов из различных микроорганизмов было выделено более 6000 антибиотиков. Каждый год ученые обнаруживают от 100 до 200 новых антибиотиков. До клиники доходит 1–2 % всех обнаруживаемых антибиотиков.
Возникает вопрос: каковы причины постоянного роста числа анти-
биотиков за последние 40–50 лет? Среди них можно назвать следующие:
1.Многие антибиотические вещества – незаменимые лечебные препараты. Они широко применяются при лечении большого числа инфекционных заболеваний, которые ранее, до открытия антибиотиков, считались неизлечимыми или сопровождались высоким легальным исходом. К их числу следует отнести некоторые формы туберкулеза, чуму, азиатскую холеру, брюшной тиф, бруцеллез, пневмонию, различные септические процессы.
2.Антибиотики – необходимые вещества для сельского хозяйства, прежде всего как лечебные препараты, применяемые в животноводстве, пти-
26
цеводстве, пчеловодстве и растениеводстве, а отдельные антибиотические вещества – и как стимуляторы роста животных.
3.При широком применении антибиотиков в качестве лечебных препаратов происходит быстрое накопление резистентных к этим соединениям форм микроорганизмов. Проблема резистентности микроорганизмов ставит задачу замены одних антибиотиков другими, то есть поиска все новых и новых антибиотических веществ.
4.Антибиотические вещества – новые, ранее неизвестные по химическому строению соединения, представляют огромный интерес для специалистов в области химии природных соединений. Изучение структуры этих веществ, а также синтез некоторых из них способствовали бурному развитию химии, а следовательно, и самой науки об антибиотиках. Достаточно указать, что к настоящему времени синтезированы такие антибиотики, как пенициллины, хлорамфеникол, тетрациклины и др.
5.Антибиотики нашли широкое применение в научных исследованиях
вкачестве веществ, используемых при изучении отдельных сторон метаболизма организмов, расшифровки тонких молекулярных механизмов биосинтеза белка, механизма функционирования мембран и других биохимических превращений как специфические ингибиторы определенных реакций. Например, одни антибиотики специфически ингибируют отдельные этапы синтеза белка на рибосомах (хлорамфеникол, пуромицин, тетрациклин), другие – синтез на разных уровнях нуклеиновых кислот (саркомицин подавляет активность полимераз; актиномицин, блеомицин, рубомицин и другие нарушают функцию ДНК), третьи – образование клеточных стенок (пенициллины) и т.д.
6.Изучение путей образования антибиотиков способствует глубокому проникновению в механизмы синтетической деятельности продуцентов этих биологически активных соединений, раскрытию основных этапов их метаболизма.
По своему спектру действия, химической структуре и молекулярному механизму действия известные антибиотики классифицируются следу-
ющим образом.
27