Материал: Фарм производство БАР
Продолжение таблицы 15
1 |
2 |
3 |
4 |
|
|
|
|
|
|
|
|
|
Стимулирует фибро- |
|
|
|
|
бласты, глиальные |
|
ТРФР |
Тромбоциты, |
|
клетки, освобождает |
|
Тромбоцитарный |
моноциты, |
30–32 |
гранулы из нейтро- |
|
фактор роста |
макрофаги |
|
филов и моноцитов, |
|
|
|
|
вызывает хемотаксис |
|
|
|
|
фибробластов |
|
|
|
|
|
|
|
Моноциты, |
|
Стимулирует фиб- |
|
ТФР |
макрофаги, |
|
робласты, остеобла- |
|
Трансформирующий |
кератиноциты, |
5–12,5 |
сты, ингибирует про- |
|
фактор роста |
мегакариоциты, |
|
лиферацию Т- и В- |
|
|
фибробласты |
|
клеток |
|
|
|
|
|
|
|
Костномозговые |
|
Подавляет диффе- |
|
ЛИФ |
клетки, |
|
ренцировку эмбрио- |
|
фибробласты, |
|
нальных стволовых |
||
Лейкоз ингибирую- |
46 |
|||
Т-клетки, |
клеток |
|||
щий фактор |
|
|||
моноциты, |
|
|
||
|
|
|
||
|
макрофаги |
|
|
|
|
|
|
|
Система медиаторов связана не только с иммунитетом, она имеет более широкое биотехнологическое значение, она поддерживает определенный уровень пролиферации, дифференцировки и активации многих видов клеток. Цитокины играют существенную роль во всех физиологических процессах, включая развитие и старение организма. Как видно из таблицы 3, большинство медиаторов (цитокинов) клеточного взаимодействия образуется в лимфоцитах и клетках моноцитарно-макрофагального ряда. Цитокины классифицируются по органам (тимус, костный мозг, лимфатические узлы и пр.), в которых они преимущественно образуются, по клет- кам-продуцентам и клеткам-мишеням, по характеру действия, физикохимическим свойствам. Цитокины участвуют во многих видах взаимодействия, обеспечивающих функционирование иммунной системы и контроль гемопоэза. Первая группа цитокинов была представлена интерферонами
228
(ИФН), часть цитокинов была классифицирована как интерлейкины (ИЛ), пронумерованные в порядке их обнаружения.
6.2.1. Технология получения интерферонов
Интерферон был открыт в 1957 году И. Линденманом и Х. Исааком. Авторами обнаружено интересное явление – заражение клеток крови вирусом приводит к выделению ими белка, который обладает противовирусной активностью. Этот белок получил название интерферона (интерференция – отталкивание). Интерес к этому феномену был огромен. Интерфероны – низкомолекулярные белки с молекулярной массой 20–40 кDа. Синтез интерферона осуществляется клетками в ответ на проникновение в них вируса, в результате чего прекращается развитие и размножение вируса в тка-
нях. Биологическое действие интерферона характеризуется следующими факторами:
универсальностью – интерферон активен против большинства ДНК и РНК-содержащих вирусов;
выраженной тканевой специфичностью;
последствием – после удаления интерферона в обработанных клетках сохраняется способность подавлять размножение вирусов;
внутриклеточной активностью с дистанционным характером действия – интерферон действует на вирусы лишь в процессе их размножения, через цитоплазматическую мембрану клетки, а не непосредственно на геном;
нечувствительность к антителам против вирусов, их индуцирую-
щих.
Общие эффекты в действии интерферонов могут проявляться как противовирусные, антипролиферативные и иммуномодулирующие. Антипролиферативное действие интерферонов обусловлено множеством эффектов: ингибированием трансляции, подавлением экспрессии клеточных протоонкогенов и других ростовых факторов клетки.
В зависимости от вида индуктора и типа клеток-продуцентов интер-
фероны разделяют на α-, β- и γ-типы: α-интерферон или лейкоцитарный интерферон продуцируют лейкоциты, которые обработаны вирусами или другими агентами (вирусы, бактерии и их токсины, полисахариды и синте-
229
тические вещества); β-интерферон или фибробластный интерферон про-
дуцируется фибробластами, обработанными вирусами или другими аген-
тами; γ-интерферон или иммунный интерферон. Существует несколько подтипов интерферонов. Молекулы интерферона имеют различия в аминокислотном составе.
По своим структурным и функциональным свойствам интерфероны подразделяют на две группы. К интерферонам I типа принадлежат ин-
терфероны альфа (α), бета (β), дельта (δ), эпсилон (ε), каппа (κ), тау (τ), омега (ω). К интерферонам II типа относится γ-интерферон. Все интерфероны I типа имеют очень много общего в аминокислотных, и соответственно, в нуклеотидных последовательностях и структуре соответствующих генов. У всех видов животных α-интерферон состоит из многих индивидуальных представителей (около 20 подвидов), гомологичность между которыми на уровне нуклеотидных последовательностей составляет около 80 %. Все гены этого семейства формируют кластер, сгруппированный преимущественно на одной хромосоме (у человека – хромосома 9). В отличие от α-интерферона у большинства видов животных β-интерферон существует в виде только одного представителя. Кроме того, в отличие от α-интерферона, β-интерфероны представляют собой гликопротеины. При анализе библиотеки ДНК были открыты ω-интерфероны. Они присутствуют не у всех видов животных, а у человека из 6 представителей этого семейства только один существует в функциональной форме, а остальные представлены псевдогенами. Только у коров и овец в эпителии эмбрионов на ранних стадиях эмбрионального развития был обнаружен τ-интерферон.
Интерферон-γ не имеет структурной гомологичности с интерферонами I типа. В отличие от генов интерферона I типа, гены интерферона II типа содержат интроны (участок ДНК, который является частью гена, но не содержит информации о последовательности аминокислот белка). Интерфероны типа II выполняют важные функции регуляторов иммунной системы. Интерферон-β, как и γ-интерферон представляет собой гликопроте-
ин. Интерфероны I и II типов объединены только по основной функции, а именно по противовирусной активности.
Как правило, в норме клетки не продуцируют заметного количества интерферонов до тех пор, пока не состоится его индукция. Однако очень
230
небольшие количества иРНК интерферона можно определить при помощи высокочувствительных методов анализа и без какой-либо явной индукции интерферона. Можно говорить о том, что при нормальных условиях, постоянной продукции интерферона не наблюдается.
Необходимо остановиться на механизме действия интерферонов.
Сами по себе молекулы интерферона не влияют непосредственно на внутриклеточные процессы. Подобно гормонам, факторам роста и другим медиаторам межклеточного взаимодействия интерфероны взаимодействуют лишь с рецепторами, расположенными на поверхности клеточных мембран. Эндогенные интерфероны для проявления своей биологической активности должны сначала секретироваться клетками, в которых они синтезируются, а затем взаимодействуют с поверхностными рецепторами. После связывания интерферона с рецепторами инициируется цепь сложных внутриклеточных реакций, которые начинаются передачей сигнала к ядру и активацией транскрипции генов, которые отвечают на интерфероны. Транскрипция соответствующих генов и синтез соответствующих белковых продуктов приводит к выработке эффекторных внутриклеточных механизмов, что и является специфичным действием интерферонов. В итоге мы наблюдаем цепочку многочисленных эффектов интерферона (как на клеточном уровне, так и на уровне организма в целом), главным из которых является ингибирование репликации вируса в инфицированных клетках. Рецепторы интерферона I и II типа различны, хотя и имеют определенную структурную общность. Все интерфероны I типа конкурируют за одни и те же рецепторы, в то время как взаимодействие γ-интерферона с клетками осуществляется при участии других рецепторов. Под действием интерферонов наблюдается продукция других цитокинов, индукция специфических ферментов, подавление пролиферации клеток, иммуномодуляция (усиление фагоцитарной активности макрофагов, специфической цитотоксичности лимфоцитов по отношению к клеткам-мишеням) и т.д.
Сегодня в Украине зарегистрирован ряд препаратов интерферона: природные (α-интерфероны: человеческий лейкоцитарный интерферон (ЗАО «Биолек», ОАО «Биофарма); β-интерфероны: человеческий фибробластный интерферон-β 1b (Бетаферон –«Schering AG») и рекомбинантные
231
(Роферон – α 2a – «Roche», Интрон-А – α 2b – «Schering-Plough», Лафе-
рон – α 2b – «ФармБиотек»).
Мы рассмотрим методы биотехнологического получения ряда фармацевтических препаратов, содержащих интерфероны различных типов.
Получение лейкоцитарного α-интерферона. Лейкоцитарный ин-
терферон относится к интерферонам первого поколения и его производство до сих пор существует в ряде стран (Финляндия, Украина, Россия и др.). Мы рассмотрим основные этапы получения интерферона из лейкоцитов крови человека под воздействием вируса – интерфероногена.
Прежде всего, остановимся на культивировании вирусов при помощи куриных эмбрионов и контроле вирусов на культуре клеток в реакции гемагглютинации или определения цитопатического действия.
Начало применения развивающихся куриных эмбрионов для выращивания вирусов приходится на 1928–1935 гг. Этот период австрийский ученый Бернет назвал «первой золотой эпохой» развития вирусологии, поскольку она открыла возможность культивирования вирусов на довольно удобной лабораторной модели, как правило, интактной в отношении многих возбудителей инфекционных заболеваний. По сути, это был первый биотехнологический процесс накопления вирусов, пригодный для промышленного и массового производства вирусной биомассы.
Развивающиеся куриные эмбрионы являются универсальным и простым для манипуляций объектом. Это объясняется тем, что куриный эмбрион содержит четыре различных естественных питательных субстрата для накопления вирусов (амниотическую и аллантоисную жидкость, хори- он-аллантоисную оболочку и желточный мешок), клетки которых, как и клетки самого эмбриона, являются высокочувствительными к различным вирусам. Для получения куриных эмбрионов используют яйца от белых леггорнов, имеющих тонкую скорлупу. Они могут быть использованы только в течение 10 дней после снесения. В противном случае развитие зародыша, несмотря на оплодотворение, сильно задерживается. Инкубацию проводят в обычных инкубаторах с автоматическим приспособлением для переворачивания яиц, вентилятором, термометром и гигрометром, при температуре 37,2–37,8 °С и влажности 60–70 %. Работу по заражению ку-
232
риных эмбрионов проводят в асептических условиях. В настоящее время, согласно международным требованиям (GMP), работу с вируссодержащим материалом проводят в ламинарных боксах, обеспеченных избыточным потоком стерильного воздуха, прошедшего через мембранные фильтры. Для получения вируса, используемого при производстве интерферона, заражение проводят в аллантоисную полость. Заражение осуществляют на 10–11 сутки развития эмбриона. В области воздушной камеры скорлупу дезинфицируют спиртовым раствором йода и прожигают. Затем прокалывают её зондом и в образовавшееся отверстие вносят 0,1–0,2 мл инокулята с оттитрованным вирусом. При этом инъекционную иглу вводят на 1–2 мм ниже границы. Заражение проводят вирусом в определенном титре. Чтобы иметь стерильную суспензию вируса к вирусному материалу добавляют по 100–1000 мг стрептомицина и 100–1000 ЕД пенициллина. После заражения эмбриона отверстие в скорлупе заливают парафином и яйца помещают в инкубатор. Яйца с эмбрионами выдерживают в течение 48 часов. Затем их охлаждают в течение 3–4 часов при температуре 2–4 °С и подвергают овоскопии (от лат. ovum – яйцо и греч. skopro – смотрю). При обнаружении погибших эмбрионов яйца выбраковывают. Перед получением вируса скорлупу над воздушной камерой дезинфицируют и отделяют пинцетом. Аллантоисную жидкость отсасывают пипеткой или с помощью специального аппарата. Из одного эмбриона, в зависимости от его возраста, можно собрать до 8–10 мл аллантоисной жидкости. Аллантоисную жидкость можно получить без эритроцитов, подвергнув её центрифугированию при 3000 об/мин в течение 20–30 минут при температуре 2–6 °С. После получения аллантоисной жидкости её проверяют на стерильность, а также на содержание вируса и его количества путем титрования, например, в реакции гемагглютинации или определения цитопатического действия.
Для критерия оценки биологической активности вирусов используют титрование на клеточной культуре – обнаруживают дозу, вызывающую цитопатический эффект в 50 % зараженных культур (ЦПД-50) или определяют гемагглютинирующие единицы вируса.
Одним из методов контроля активности вируса является реакция гемагглютинации, основанная на способности вируса склеивать эритроци-
233
ты. Для проведения реакции готовят ряд последовательных двукратных |
Количество живых лейкоцитов в полученной пленке должно быть не менее |
разведений вируса и прибавляют к ним определенное количество эритро- |
97 %. Определение нежизнеспособных лейкоцитов проводят окрашивани- |
цитов (например, куриных). В тех образцах, где количество вируса было |
ем эозинатом натрия. |
достаточно для полной агглютинации, наблюдается образование конгло- |
2. Эритроциты лизируют с помощью хлорида аммония (0,83 %-ый |
мератов из эритроцитов, которые быстро оседают на дно, образуя на всей |
раствор при значении рН – 7,0 ± 0,5) согласно методике Кэнтелла (1981 г.). |
поверхности красную пленку. При отсутствии вируса эритроциты оседают |
3. Обработанную хлоридом аммония лейкоцитарную пленку ресус- |
на дно в виде компактного осадка. За титр принимают предельное разведе- |
пендируют в среде Игла МЕМ, содержащую бикарбонат натрия, антибио- |
ние вируссодержащей жидкости, вызвавшее агглютинацию эритроцитов на |
тик и сыворотку крови человека, очищенную от иммуноглобулинов. |
50 %. |
4. В качестве праймера добавляют 20 ЕД/мл сырого α-интерферона |
Другим методом контроля активности вируса является определение |
(сырой α-интерферон – это продукт полученный в результате процесса ин- |
ЦПД-50. Цитопатическое действие вируса используемого при производ- |
дукции, но не подвергшийся очистке и обработке хлористоводородной |
стве лейкоцитарного интерферона должно быть 10-8–10-9 ЦПД-50. Титро- |
кислотой при рН = 2,0 в течение 5 дней с целью инактивации вирусных |
вание вирусов проводят на культуре клеток, например, фибробластов. |
агентов). |
Жидкость, содержащую вирус, разводят методом последовательных разве- |
5. Полученную суспензию инкубируют в стерильных стеклянных |
дений (на среде Игла, среде 199 и др.) от 10-1 до 10-10. Образцы разведений |
емкостях. Лейкоциты праймируют в течение 2–3 часов при температуре |
вируса 10-8–10-10 в необходимом количестве переносят в лунки плашек, со- |
(36 ± 0,5) °С и периодическом перемешивании (50–200 об/мин), а затем |
держащих культуру клеток. Плашки с культурой клеток, зараженных ви- |
добавляют вирус-индуктор (вирус Сендай или вирус болезни Ньюкасла и |
русом, помещают в термостат при температуре (37 ± 1) °С на 72 часа. За- |
др.) до конечной концентрации 150–250 гемагглютинационных единиц/мл. |
тем проводят учет биологической активности вируса по эффекту цитопа- |
Используется аллантоисная жидкость с титром вируса не менее |
тического действия. Титром вируса считается максимальное разведение |
108/мл ЦПД-50. После 1 часа инкубации для прикрепления вируса лейко- |
вируса, при котором эффект цитопатического действия выражен в образ- |
циты разводят до 4 · 106 кл/мл (в 2,5 раза) той же средой. Затем культуру |
цах с одинаковым разведением. |
инкубируют 15–20 часов при (36 ± 0,5) °С, удаляют клетки и дебрис при |
Технология получения лейкоцитарного α-интерферона состоит из |
500–1000 об/мин в течение 15–20 минут при температуре 2–8 °С. В полу- |
следующих стадий: |
ченном растворе определяют титр интерферона. |
1. Для получения лейкоцитарной пленки используют кровь или |
6. Раствор интерферона концентрируют в 50 раз, используя филь- |
плазму доноров из специализированных центров (в Украине это центры |
трующую систему с тангенциальным потоком через которую проходят со- |
переливания крови), утвержденных национальным органом контроля им- |
единения с молекулярной массой 10 кDа и менее. Процесс проводят при |
мунобиологических препаратов. Доноры проходят контроль на контами- |
температуре 2–8 °С. Концентрированный раствор интерферона центрифу- |
нацию вирусными (гепатиты В и С, ВИЧ и др.) и бактериальными агента- |
гируют при 9000 g в течение 30 минут при температуре 2–8 °С. Возможно |
ми. Кровь или плазму центрифугируют при 1000–1500 об/мин в течение |
хранение раствора при температуре минус 60–70 °С. |
20–25 минут при температуре 2–8 °С. Отделяют слой лейкоцитов со значи- |
7. Затем проводят очистку интерферона при помощи аффинной хро- |
тельным содержанием эритроцитов. В ряде методов предлагается исполь- |
матографии. Данный метод очистки предусматривает использование мо- |
зовать поливиниловый спирт для лучшего разделения компонентов крови. |
ноклональных антител, специфических к α-интерферону человека, напри- |
234 |
235 |
мер, антител NK2 коммерческого производства («Celltech Limited», England). Моноклональные антитела соединяют с активированной CNBr Сефарозой 4В. Концентрированный сырой интерферон размораживают и очищают центрифугированием 15000–18000 g в течение 60 минут при температуре 2–8 °С. Прозрачный раствор интерферона фильтруют через фильтры с размером пор 0,22–0,45 мкм и наносят на колонку с моноклональными антителами. Интерферон элюируют с колонки раствором, содержащим 0,1 М лимонной кислоты и 0,3 М хлористого натрия (рН – 2,0).
8.Кислотную инкубацию и нейтрализацию вирусов при рН 2,0 проводят при 4 °С в течение не менее 5-ти суток. За этот период происходит необходимая инкубация посторонних агентов, включая вирусы.
9.После 5-ти дней инкубации рН раствора доводят до значения 7,2–7,4 и стандартизуют раствор до содержания белка 1–3 мг/мл.
10.На данном этапе проводят гель-фильтрационную хроматографию интерферона. Раствор интерферона наносят на колонку с препаративной гранулированной сефарозой в количестве 5 % от объема колонки. Элюирование проводят фосфатным буфером. Все фракции, содержащие основное количество интерферона объединяют и подвергают стерилизующей фильтрации через мембраны с размером пор 0,22 мкм. Раствор хранят при температуре минус 60–70 °С.
11.При получении интраназального интерферона проводят очистку ультрафильтрацией через мембраны с порогом отсечения 300 кDа (без проведения стадии аффинной хроматографии). К раствору интерферона добавляют криопротекторы, препарат разливают во флаконы и подвергают лиофилизации.
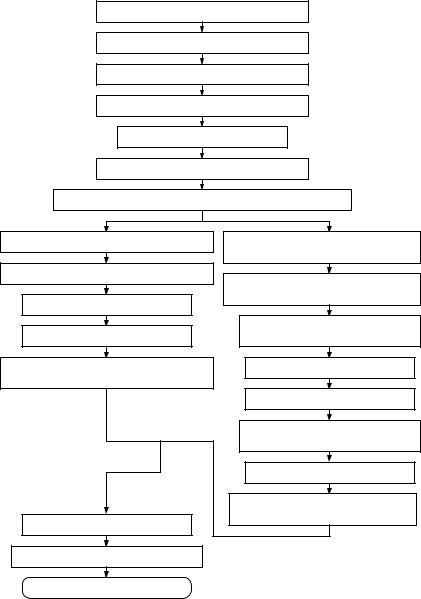
Технология получения лейкоцитарного интерферона представлена на рис. 17.
236
Изготовление лейкоцитарного интерферона
Получение и контроль вируса индуктора
Выделение и очистка лейкоцитов человека
Получение суспензии лейкоцитов человека
Проведение прайминга
Проведение биосинтеза интерферона
Отделение культуральной жидкости, содержащей интерферон
Получение интраназальной формы препарата
Очистка интерферона ультрафильтрацией
Стерилизующая фильтрация
Инактивация вируса
Стандартизация и стабилизация раствора интерферона
Разлив раствора интерферона
Лиофилизация раствора интерферона
Контроль готового препарата
Получение инъекционной формы препарата
Очистка и концентрирование раствора интерферона ультрафильтрацией
Очистка интерферона аффинной хроматографией
Стерилизующая фильтрация
Инактивация вируса
Очистка интерферона гель-хроматографией
Стерилизующая фильтрация
Стандартизация и стабилизация раствора интерферона
Рисунок 17 – Технология получения лейкоцитарного интерферона
237