Материал: Фарм производство БАР
в результате стимулирующего действия, прежде всего глюкозы и некоторых других веществ, эта информация списывается РНКполимеразой с инсулинового гена в виде мРНК на рибосомах, в которых осуществляется соединение аминокислот с образованием белков. На рибосомах происходит сборка полипептидной цепи из 109 аминокислот с образованием препроинсулина под влиянием рестриктаз, в результате образуются фрагменты от нескольких сотен до нескольких тысяч нуклеотидов;
при синтезе препроинсулина в -клетках поджелудочной железы первые 23 аминокислоты «проводят» молекулу через мембрану клетки. Эти аминокислоты отщепляются рестриктазами и образуется пептид проинсулин, состоящий из 86 аминокислот. Молекула проинсулина сворачивается таким образом, что начальный и конечный её сегменты сближаются,
ацентральная часть молекулы удаляется под влиянием фермента рестрикции.
Работы по генно-инженерному получению инсулина начались с 1978 года, когда появилось сообщение (США) о получении штамма кишечной палочки, продуцирующего крысиный проинсулин.
В 1978 году были синтезированы отдельные цепи человеческого инсулина посредством экспрессии их синтетических генов в клетках E. Coli. Каждый из полученных синтетических генов подстраивался к 3′-концу гена фермента -галактозидазы и вводился в векторную плазмиду (pBR322). Клетки E. Coli, трансформированные такими рекомбинантными плазмидами, производили гибридные (химерные) белки, состоящие из фрагмента
-галактозидазы и A или B пептида инсулина, присоединенного к ней через остаток метионина. При обработке химерного белка бромцианом пептид освобождается. Однако замыкание дисульфидных мостиков между образованными цепями инсулина происходило с трудом.
В 1981 году синтезирован ген-аналог проинсулина – мини С-проинсулин, в котором 35-звенный С-пептид был заменен на сегмент из шести аминокислот: Арг-Арг-Гли-Сер-Лиз-Арг и показана его экспрессия в E. Coli.
158
В1980 году У. Гилберт с сотрудниками выделили мРНК инсулина из опухоли -клеток поджелудочной железы крысы и с помощью обратной транскриптазы получили с неё кДНК. Полученную кДНК встроили в плазмиду pBR322 E. Coli, в среднюю часть гена пенициллиназы. Рекомбинантная плазмида содержала информацию о структуре проинсулина. В результате трансляции мРНК в клетках синтезировался гибридный белок, содержащий последовательности пенициллиназы и проинсулина, который выщепляли из такого белка трипсином.
В1980 году американскими учеными Миллером и Бакстером был впервые описан процесс клонирования человеческого гена в E. Coli с последующей индукцией и получением белка инсулина, идентичного человеческому.
Впромышленных условиях рекомбинантный инсулин впервые был получен американской фармацевтической компанией «Eli Lilli» совместно
сбиотехнологической компанией «Genentech» (США) и продукт был выпущен на рынок в 1982 г. При производстве человеческого инсулина использована технология рекомбинантных ДНК: помещают кДНК гена человеческого проинсулина в E. Coli или S. serevisae и гидролизуют полученный проинсулин до молекулы инсулина.
Вэто же время компания «Novo-Nordisk» (Дания) разработала технологию получения генно-инженерного инсулина человека, основанную на использовании генетически модифицированных дрожжевых культур в роли суперпродуцентов инсулина человека. Использование эукариот, имеющих сходную с человеческой систему процессинга белков в роли продуцентов инсулина, позволило получить гормон или его предшественник в нативной форме. Значительным преимуществом данной технологии является полное отсутствие в препаратах бактериальных токсинов и пирогенов клеточной стенки. Несмотря на все эти преимущества, получение инсулина
сиспользованием бактериальных штаммов суперпродуцентов остается более предпочтительным благодаря более высокому уровню экспрессии инсулина в составе гибридного белка.
159
В настоящее время генно-инженерный инсулин производят путем ферментации генетически измененных микроорганизмов: кишечной палочки или дрожжей, которые способны синтезировать предшественник инсулина (проинсулин) в составе химерного протеина. Из полученного биосинтетическим путем промежуточного продукта реконструируют инсулин человека (энзиматическим путем) по следующей схеме: культивирование штамма со встроенным геном гибридного белка, включающим полную последовательность инсулина человека; очистка и ренатурация гибридного белка; протеолитическое расщепление гибридного белка с получением инсулина; очистка инсулина. Данная схема во многом напоминает процесс биосинтеза инсулина в островках Лангерганса, где гормон сначала появляется в виде белка-предшественника (проинсулина), а потом протеолитическими ферментами от проинсулина отщепляется соединительный С-пептид. В производстве для расщепления гибридного белка используют сходные по специфичности ферменты: трипсин и карбоксипептидазу В. Гидролиз производят путем обработки ферментами последовательно или одновременно.
Примером получения рекомбинантного инсулина является технология, предложенная российскими учеными из ОАО «Национальные биотехнологии», Института биоорганической химии РАН и Государственного института кровезаменителей и медицинских препаратов. Ими был создан штамм-продуцент гибридного белка E. Coli JM109/pPINS07.
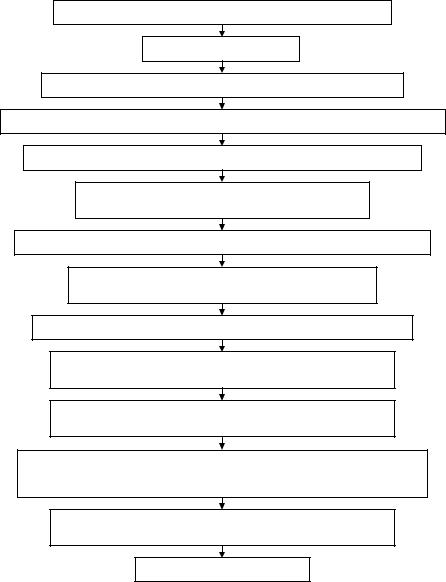
На рис. 16 представлена биотехнологическая схема получения рекомбинантного инсулина.
160
Культивирование штамма продуцента E. Coli JM109/pPINS07
Разрушение клеток
Отделение осадка гибридного белка-сырца центрифугированием
Растворение гибридного белка с одновременным восстановлением нерегулярных S-S
Ренатурация гибридного белка с образованием правильных S-S
Хроматографическая очистка гибридного белка на ионообменном сорбенте (КМ-сефароза)
Гидролиз гибридного белка трипсином (получение диаргинининсулина)
Хроматографическая очистка диаргинининсулина на ионообменном сорбенте (SP-Sepharose FF)
Концентрирование фракций, содержащих 90% диаргинининсулина
Трансформация диаргинининсулина карбоксипептидазой В (получение первичного инсулина)
Очистка первичного инсулина методом обращено-фазовой ВЭЖХ до чистоты более 96 %
Хроматографическая очистка генно-инженерного инсулина человека от высоко- и низкомолекулярных примесей при помощи
гель-фильтрации
Кристаллизация и перекристаллизация инсулина в присутствии ионов Zn+2
Сушка кристаллов Zn-инсулина
Рисунок 16 – Биотехнологическая схема получения рекомбинантного инсулина
161
Как видно из приведенной схемы из выращенной биомассы выделяется предшественник инсулина, гибридный белок, экспрессируемый в количестве 40 % от всего клеточного белка, содержащий препроинсулин. Превращение его в инсулин in vitro осуществляется в той же последовательности, что и in vivo – отщепляется липидирующий полипептид, препроинсулин превращается в инсулин через стадии окислительного сульфитолиза с последующим восстановительным замыканием трёх дисульфидных связей и ферментативным вычленением связывающего С-пептида. Как видно из схемы, для очистки инсулина используют различные виды хроматографических очисток: ионообменные, гельфильтрационные и ВЭЖХ, что позволяет получить инсулин высокой степенью чистоты. Использование аффинной хроматографии значительно снизило содержание в препарате балластных белков с молекулярной массой большей, чем у инсулина. К этим белкам относится проинсулин и частично расщепленные проинсулины, которые способны индуцировать выработку антиинсулиновых антител. Особую роль играет обращено-фазовая ВЭЖХ. Использование ВЭЖХ является предпочтительным в крупномасштабном производстве, поскольку метод лишен ряда недостатков, присущим другим видам хроматографии (например, ионно-обменную хроматографию отличает длительность очистки за счет низких значений давления; высокая себестоимость метода за счет низкой емкости сорбентов и их высокой стоимости). Определяющими факторами при проведении обращено-фазовой ВЭЖХ являются: рН подвижной фазы, температура, добавки для введения в подвижную фазу, максимальная нагрузка на хроматографическую колонку и др. Одной из основных проблем в производстве генно-инженерного инсулина человека является очистка инсулина от родственных пептидов, в частности от А21-дезамидоинсулина, отличающегося от инсулина дезамидированным аспарагином в 21-ом положении А цепи. Содержание инсулиноподобных примесей и А21-дезамидоинсулина в фармакопейных субстанциях инсулина человека жестко регламентируется.
В Российской Федерации вопросами получения генно-инженерного инсулина занимается ряд ученых, в том числе, и специалисты ОАО «Национальные биотехнологии». Ими предложена промышленная схема получения препарата инсулина человека на основе штамма E. Coli
162
JM109/pНINS11. По мнению авторов, использование предложенного ими штамма имеет ряд преимуществ перед штаммом E. Coli JM109/pPINS07, который рассматривался нами ранее. Так, согласно рис. 16 видно, что при использовании штамма E. Coli JM109/pPINS07 получение рекомбинантного инсулина сводится к следующему: культивирование штаммапродуцента E. Coli JM109/pPINS07, разрушение бактериальных клеток дезинтеграцией, отделение телец включения, содержащих гибридный белок, их растворение в буфере, содержащем мочевину и дитиотреитол, кислотное осаждение примесных соединений, очистку гибридного белка хроматографией на КМ-сефарозе, расщепление гибридного белка трипсином и карбоксипептидазой В осуществляют последовательно, при этом продукты трипсинолиза хроматографируют на СП-сефарозе, а полученную после расщепления карбоксипептидазой Б фракцию инсулина очищают методом обращено-фазовой высокоэффективной жидкостной хроматографии (ОФ ВЭЖХ) с последующей гель-фильтрацией. В данном методе, по мнению авторов, присутствует многостадийная технологическая цепочка. Кроме того, последовательное расщепление гибридного белка трипсином и карбоксипептидазой В требует и последовательных хроматографических очисток диаргинин-инсулина после триптического гидролиза гибридного белка и инсулина после расщепления карбоксипептидазой В, которые приводят к значительным потерям конечного продукта. Необходимо также отметить, что использован штамм-продуцент E. Coli JM109/pPINS07, несущий рекомбинантную плазмиду pPINS07, которая кодирует гибридный белок с высокой долей лидерного пептида, составляющего около 50 %. Поэтому использование данного штамма при получении инсулина удорожает процесс производства из-за повышения затрат на биосинтез и снижает выход целевого продукта.
Преимуществом созданной плазмиды pНINS11 является то, что она обеспечивает более высокий выход конечного продукта инсулина за счет повышения выхода правильно свернутого гибридного белка после его ренатурации.
Полученный штамм-продуцент E. Coli JM109/pНINS11 характери-
зуется следующими признаками:
163
1.Морфологические признаки: клетки мелкие, палочковидной формы, грамотрицательные, неспороносные, размером 1 х 3,5 мкм, подвижные
схорошо различимыми тельцами включения после индукции синтеза гибридного белка;
2.Культуральные признаки: при росте на агаризованной среде LB колонии круглые, гладкие, полупрозрачные, блестящие серые. Край ровный, диметр колоний 1–3 мм, консистенция пастообразная. Рост в жидких средах характеризуется ровным помутнением.
3.Физиолого-биохимические признаки: клетки растут при температу-
ре 4–42 °С, оптимум рН 6,8–7,6. В качестве источника азота используют как минеральные соли аммония, так и органические соединения: аминокислоты, пептон, триптон, дрожжевой экстракт. В качестве источника углерода при росте на минимальной среде используют глицерин, углеводы, аминокислоты;
4.Устойчивость к антибиотикам: клетки штамма продуцента про-
являют устойчивость к ампициллину (до 500 мкг/мл), обусловленную
наличием в плазмиде гена -лактамазы (bIa);
5. Стабильность плазмиды в штамме: при поддержании клеток в течение нескольких месяцев на агаризованной среде LB, содержащей ампициллин, не наблюдается потери или перестройки плазмиды, влияющей на экспрессию гибридного белка;
В конструированном штамме гибридный белок после индуцированной экспрессии накапливается в виде телец включения и его содержание составляет не менее 30 % от общего белка клетки.
Рассмотрим технологическую схему получения генно-инженерного инсулина при использовании штамма-продуцента E. Coli JM109/pНINS11.
1. Конструирование плазмиды pНINS11.
а) Плазмиду pHINS11 конструируют на основе известной плазмиды рHINS05. Плазмидную ДНК pHINS05 подвергают исчерпывающему гидролизу рестриктазами BeII и BamHI. Для этого 5 мкг плазмидной ДНК pHINS05 в 20 мкл буфера, содержащего 33мМ трис-ацетата, рН = 7,9; 66 мМ K-ацетата, 10 мМ Mg-ацетата, 0,1 мг/мл БСА и 10 ед. рестриктазы BeII и BamHI инкубируют 1 час при температуре 37 °С. Из полученного гидролизата выделяют BcII-BamHI фрагмент ДНК размером около
164
4,2 т.п.о. при помощи электрофореза в 0,8 % геле легкоплавкой агарозы. Далее ДНК депротеинизируют фенолом, смесью фенола с хлороформом (1 : 1), хлороформом, и осаждают этиловым спиртом, растворяют в 20 мкл воды. Полученный BcII-BamHI фрагмент, содержащий ген гибридного белка и векторную плазмиду pYINS05, лигируют с 20-кратным молярным избытком олигонуклеотидного дуплекса, полученного в результате отжига синтетических нуклеотидов oligo-link24A (SEQ ID NO:4) и oligo-link24B (SEQ ID NO:5).
б) Компетентные клетки штамма E. Coli JM109 трансформируют лигированной смесью (10 мкл) и высевают на LB-агар, содержащий 100 мкг/мл ампициллина. Из выросших колоний выделяют плазмидную ДНК и секвенируют между сайтами рестриктаз EcoRI и BamHI для подтверждения вставки в линкерную часть гена гибридного белка. В результате получают плазмиду pHINS09.
с) Для получения плазмиды с делецией по rор-гену (негативного регулятора копийности) к 5 мкг плазмидной ДНК pHINS09 в 20 мкл буфера добавляют 10 ед. рестриктазы Eco47III и SnaI, генерирующие «тупые» концы, и смесь инкубируют в течение 1 часа при 37 °С. Далее ДНК депротеинизируют фенолом, смесью фенола с хлороформом (1 : 1), хлороформом, осаждают этиловым спиртом, растворяют в 20 мкл воды. Полученную таким образом ДНК лигируют в 30 мкл буфера для лигирования в присутствии 5 ед. ДНК лигазы фага T4 в течение 16 часов при 8 °С. Лигированной смесью (10 мкл) трансформируют компетентные клетки штамма E. Coli JM109 и высевают на LB-агар, содержащий 100 мкг/мл ампициллина. Отбирают бактериальные клоны, несущие плазмидную ДНК размером 3,6 т.п.о. Выделенные плазмиды подвергают рестрикционному анализу и секвенируют по методу Сенгера. В результате получают плазмиду pHINS11.
d) Плазмидой pHINS11 трансформируют компетентные клетки штамма E. Coli JM109 и высевают на LB-агар, содержащий 100 мкг/мл ампициллина. Отдельно локализованную колонию трижды пересевают на чашки с LB-агаром, содержащим 100 мкг/мл ампициллина. Полученной моноклоновой культурой инокулируют 5 мл жидкой среды LB с ампицил-
165
лином и инкубируют в течение ночи при интенсивном встряхивании при |
могенат клеток пропускают через проточную центрифугу (g = 18000). Ос- |
|
37 °С. |
новная масса телец включения (не менее 90 %) осаждается в роторе цен- |
|
Полученный штамм-продуцент E. Coli JM109/pHINS11 хранят в 20 % |
трифуги. Влажный осадок телец включения (2,6 кг) выгружают из ротора |
|
глицерине при минус 40 °С. |
центрифуги, замораживают и хранят при минус 40 °С. Потери гибридного |
|
2. Выращивание биомассы штамма-продуцента E. Coli |
белка при выделении телец включения не превышают 15 %. |
|
JM109/pНINS11. |
4. Растворение телец включения, содержащих гибридный белок, и |
|
Культивирование клеток штамма E. Coli JM109/pНINS11 для полу- |
ренатурация гибридного белка. |
|
чения инокулята и основного выращивания проводят на питательной среде |
В реактор объемом 30 л, заполненный 18 л буферного раствора, со- |
|
следующего состава (г/л): гидролизат казеина соляно-кислотный – 30; экс- |
держащего 0,1 М трис-HСl, рН 8,0 и 8 М мочевины, загружают 1,8 кг пас- |
|
тракт пекарских дрожжей – 14; двузамещенный фосфат калия трех- |
ты телец включения и включают перемешивающее устройство. После рас- |
|
водный – 6; однозамещенный фосфат калия – 3; сульфат магния – 0,5; глю- |
творения телец включения в реактор добавляют дитиотреитол до конечной |
|
коза – до 50; ампициллина натриевая соль – 0,05; вода очищенная до 1 л. |
концентрации 10 мМ и продолжают перемешивание в течение 10–12 ч при |
|
Посевные культуры готовят в количестве 1/10 от объема засеваемой пита- |
15 °С. Количество гибридного белка в растворе составляло 174 г. |
|
тельной среды и выращивают до оптической плотности 7–8 единиц при |
В реактор с охлаждением объемом 250 л заливают 160 л глицин- |
|
длине волны 540 нм, длина оптического пути 10 мм, рН культивирования |
NaOH буфера, рН 9–11 и охлаждают его до температуры 10–14 °С. После |
|
6,9 ± 0,2 (корректировку проводят добавлением глюкозы и щелочи), дли- |
охлаждения буферного раствора в реактор подают раствор гибридного |
|
тельность 4–6 часов; рО2 – 40 ± 15 %. |
белка с восстановленными дисульфидными связями. В течение 20–24 ч |
|
Выращивание основной культуры проводят в ферментере емкостью |
инкубируют раствор гибридного белка, перемешивая и поддерживая тем- |
|
150 л с 90 литрами питательной среды. Объем инокулята – 10 л. Культиви- |
пературу в реакторе 10–14 °С. После ренатурации гибридного белка с об- |
|
рование проводят при следующим параметрах: температура 36,5 ± 0,5 °С; |
разованием правильно замкнутых S-S связей (контроль ОФ ВЭЖХ) прово- |
|
рН 6,7–7,1; рО2 – 40 ± 15 %. Для индукции биосинтеза гибридного белка в |
дят кислотное осаждение примесных белков путем подкисления реакцион- |
|
середине логарифмической фазы роста культуры при оптической |
ной среды в реакторе до рН 4,0–4,5 раствором соляной кислоты. Останав- |
|
плотности 7–9 единиц вносят индуктор – 1-изопропил- -D-1-тиогалакто- |
ливают перемешивание и через 4–5 ч супернатант осветляют на микро- |
|
фильтрационной установке. Содержание ренатурированного гибридного |
||
пиранозид. Культивирование продолжают до образования внутриклеточ- |
||
ных включений гибридного белка («телец включения» – ТВ) у 90–95 % |
белка в осветленном супернатанте составляет 85 г. |
|
клеток. Экспресс-контроль процесса накопления ТВ осуществляют с по- |
5. Очистка ренатурированного гибридного белка на КМ-сефарозе. |
|
мощью фазово-контрастной микроскопии препаратов. |
Правильно свернутый гибридный белок сорбируют из фильтрата на |
|
3. Выделение телец включения. |
ионно-обменную колонку объемом 5 л, заполненную КМ-сефарозой, пред- |
|
Рост культуры в ферментере останавливают путем резкого сокраще- |
варительно уравновешенную 0,05 М Na-ацетатным буфером, рН 4,0–5,5. |
|
ния интенсивности перемешивания, культуру охлаждают до 10–14 °С и |
Сорбированный белок элюируют с колонки градиентом 0,1–0,6 М хлори- |
|
концентрируют на сепараторе в 8–10 раз. В полученную суспензию добав- |
дом натрия в 0,05 М Na-ацетатном буфере, рН 4,0–5,5, содержащем 1,5 М |
|
ляют трис-основной до концентрации 0,1 М, мочевину – до 1,5 М, ЭДТА – |
мочевины. Фракции, содержащие гибридный белок с чистотой не менее |
|
до 1 мМ. Забуференную до рН 6,8–7,0 суспензию трижды пропускают че- |
95 % (контроль методом ОФ ВЭЖХ), объединяют и используют для даль- |
|
рез гомогенизатор при давлении 700–800 атм и температуре 15–20 °С. Го- |
|
|
166 |
167 |