Материал: Фарм производство БАР
D-рибозы осуществляют из культуральной жидкости после отделения микробных клеток центрифугированием и путем колоночной хроматографии с использованием сильноосновного анионита в боратной форме. Полученный раствор витамина В2 подвергают кристаллизации. Необходимо отметить, что производство рибофлавина микробиологическим методом по сравнению с химическим синтезом имеет существенные преимуще-
ства, а именно:
использование доступного сырья;
осуществление процесса получения витамина в одну технологическую стадию;
отсутствие токсических выбросов в атмосферу.
4.2. Получение витамина В12 (цианокобаламин)
Витамин В12 (Со [ -(5,6-диметилбензимидазолил)]-Со -циано- кобамид – C63H88CoN14O14P – цианокобаламин) активизирует обмен углеводов, белков и липидов, участвует в синтезе лабильных метильных групп, в образовании холина, метионина, нуклеиновых кислот, способствует накоплению в эритроцитах соединений с сульфгидрильными группами. Являясь фактором роста, стимулирует функцию костного мозга, что необходимо для нормобластного эритропоэза. Цианокобаламин способствует нормализации нарушенных функций печени и нервной системы, активизирует свертывающую систему крови, в высоких дозах вызывает повышение тромбопластической активности и активности протромбина.
В организме человека и животных определенное количество цианокобаламина синтезируется микрофлорой кишечника, что не удовлетворяет потребность организма в витамине, и дополнительное количество его организм получает с продуктами питания.
Витамин В12 открыт в 1948 году одновременно в США и Англии. В 1972 году в Гарвардском университете был осуществлен химический синтез корриноидного предшественника витамина В12. Химический синтез корнестерона (структурного элемента корринового кольца витамина), включающий 37 стадий, в крупных масштабах не воспроизведен из-за сложности процесса.
128
Витамин В12 регулирует углеводный и липидный обмен, участвует в метаболизме незаменимых аминокислот, пуриновых и пиримидиновых оснований, стимулирует образование предшественников гемоглобина в костном мозге; применяется в медицине для лечения злокачественной анемии, лучевой болезни, заболеваний печени, полиневрита и т.п. Добавление витамина к кормам способствует более полноценному усвоению растительных белков и повышает продуктивность сельскохозяйственных животных на 10–15 %.
Первоначально витамин В12 получали исключительно из природного сырья, однако из 1 тонны печени можно было выделить всего лишь 15 мг витамина. Единственный способ его получения в настоящее время – мик-
робиологический синтез. Обнаружение витамина в качестве побочного продукта при производстве антибиотиков в значительной степени стимулировало поиск организмов-продуцентов витамина и изучение путей его образования. Однако механизмы регуляции биосинтеза витамина В12 до настоящего времени полностью не расшифрованы. Известно, что при высоких концентрациях витамин полностью репрессирует синтез ключевых ферментов своего новообразования.
Продуцентами витамина В12 при его промышленном получении служат актиномицеты, метанобразующие и фотосинтезирующие бактерии, одноклеточные водоросли. В 70-х годах ХХ века интерес ученых привлекли пропионовокислые бактерии, известные еще с 1906 года и широко использующиеся для приготовления препаратов в животноводстве. Выделено 14 видов пропионовокислых бактерий, продуцирующих витамин В12. Для получения высокоочищенных препаратов витамина В12 пропионовокислые бактерии культивируют периодическим способом на средах, содержащих глюкозу, казеиновый гидролизат, витамины, неорганические соли, хлорид кобальта. Добавление в среду предшественника 5,6-диметилбензимидазола (способствует переводу неактивных форм в природный продукт) по окончании первой ростовой фазы (5–6 суток) стимулирует быстрый (18–24 ч) синтез витамина с выходом последнего 5,6–8,7 мг/л. Путем селекции, оптимизации состава среды и условий культивирования выход витамина В12 в промышленных условиях был значительно повышен. Так, выход витамина на среде с кукурузным экстрактом и глюкозой при поддержании ста-
129
бильного значения рН около нейтрального достигает 21–23 мг/мл. Мутант |
Источником углерода в питательной среде служит ацетонобутиловая |
пропионовокислых бактерий продуцирует до 30 мг/мл витамина. Бактерии |
и спиртовая барда, которую поставляют заводы, перерабатывающие зерно |
плохо переносят перемешивание. Применение уплотняющих агентов (агар- |
и мелассу. Для оптимизации питательной среды в неё добавляют соедине- |
агар, крахмал) предотвращающих оседание бактерий, а также использова- |
ния кобальта (хлорид кобальта – 4 г/м3), который входит в состав молеку- |
ние высоко анаэробных условий и автоматического поддержания рН поз- |
лы витамина В12 и субстраты для роста метанобразующих бактерий – низ- |
воляет получить наиболее высокий выход витамина – 58 мг/л. |
шие жирные кислоты и низшие спирты, что позволяет значительно повы- |
Из культуральной жидкости витамин В12 выделяют экстракцией, ор- |
сить выход витамина В12. |
ганическими растворителями, ионообменной хроматографией с последу- |
Подготовленное сырье освобождают в декантаторе от взвешенных |
ющим осаждением витамина из фракций в виде труднорастворимых со- |
частиц и непрерывно подают в нижнюю часть ферментера – емкость. Од- |
единений. В процессе получения витамина В12 с помощью пропионовокис- |
новременно в ферментер поступает посевной материал культуры микроор- |
лых бактерий применяют дорогостоящую антикоррозийную аппаратуру, |
ганизмов, предварительно выращенной в специальных аппаратах. Для вы- |
сложные и дорогостоящие питательные среды. Усовершенствование тех- |
ращивания продуцента требуются облигатно анаэробные условия, так как |
нологического процесса идет в направлении удешевления компонентов |
даже следовые количества кислорода подавляют рост бактерий. При со- |
питательных сред и перехода с периодического культивирования на непре- |
здании анаэробных условий в среду подают диоксид углерода или газы, |
рывный процесс. В последние годы исследуется возможность получения |
выделяющиеся в процессе ферментации. Ежедневно из ферментера отби- |
витамина с использованием иммобилизованных клеток пропионовокислых |
рают 20–30 % объема среды. Продукт ферментации стабилизируют, под- |
бактерий. Учитывая высокую светочувствительность витамина В12 при |
кисляя соляной или фосфорной кислотой до рН 6,3–6,5, а также добавляют |
проведении биотехнологического процесса необходимо все операции осу- |
0,2–0,25 % сульфита натрия, что предотвращает разрушение витамина при |
ществлять в затемненных условиях или используя красный свет. |
тепловой обработке (особенно существенное в щелочной среде). В даль- |
Для нужд животноводства сотрудниками института им. А. Н. Баха |
нейшем отобранная часть культуральной жидкости дегазируется, упарива- |
предложена простая и дешевая технология получения витамина В12. По |
ется в вакууме; концентрат высушивается в распылительной сушке до |
указанной технологии ферментацию осуществляет сложный биоценоз тер- |
влажности 10–15 % и смешивается с наполнителями. |
мофильных микроорганизмов, производящих метановое брожение. Ком- |
Для медицинских целей субстанцию витамина В12 получают в виде |
плекс микроорганизмов включает целлюлозоразлагающие, углеводсбра- |
кристаллического темно-красного порошка, содержащего не менее 99 % |
живающие, аммонифицирующие, сульфитвосстанавливающие и метан- |
основного вещества. Из субстанции готовят различные лекарственные |
образующие бактерии. На первой фазе процесса (10–12 дней) развиваются |
формы: растворы для инъекций и таблетки. |
термофильные углеводсбраживающие и аммонифицирующие бактерии. |
Активно продуцируют витамин В12 представители рода |
При этом в слабокислой среде (рН 5,0–7,0) органические соединения пре- |
Propionibacterium, природные штаммы которых образуют от 1,0 до 8,5 мг/л |
вращаются в жирные кислоты и аммиак. На второй фазе, когда среду под- |
витамина, а полученный искусственный мутант P. Shermanii M-82 спосо- |
щелачивают до рН 8,5; в биоценозе преобладают метанобразующие бакте- |
бен накапливать витамин В12 до 58 мг/л. |
рии, которые сбраживают возникающие на первой фазе продукты до мета- |
Практический интерес для микробиологического синтеза В12 имеют |
на и диоксида углерода. Именно метанобразующие бактерии – главные |
представители актиномицетов и родственных микроорганизмов. Витамин |
продуценты витамина. Обогащение сред очищенными культурами ме- |
В12 в значительных количествах синтезируют Nocardia rugoza (до 18 мг/л), |
танобразующих бактерий увеличивает выход активных форм витамина В12. |
а также представители рода Micromonospora. Высокой кобаломинсинтези- |
130 |
131 |
рующей активностью обладают метагенные бактерии, например,
Methanosarcina barkeri, M. Vacuolita и отдельные штаммы галофильного вида Methanococcus halophilus (до 16 мг/л).
Витамин В12 синтезируют строго анаэробные бактерии из рода клостридий. В значительных количествах образуют витамин В12 ацетогенные клостридии C. Thermoaceticum, C. Formicoaceticum и Acetobacter woodi,
синтезирующие ацетат из CO2.
Известны активные продуценты витамина В12 среди псевдомонад. Некоторые штаммы Pseudomonas denitrificans нашли применение для промышленного получения цианокобаламина. Интерес представляют также термофильные бациллы, а именно, Bacillus eirculans, Bacillus stearothermophilus, которые растут при температурах, соответственно, 60 °С и 75 °С и за 18–24 часа культивирования без соблюдения стерильных условий дают высокий выход витамина.
Например, в России в качестве основного продуцента витамина В12, получаемого для медицинских целей, используют культуру
Propionibacterium shermanii. Для получения витамина В12 Р. shermanii
культивируют периодическим методом в анаэробных стерильных условиях в питательной среде, содержащей кукурузный экстракт, глюкозу, соли кобальта и сульфат аммония.
Образующиеся в процессе брожения органические кислоты нейтрализуют раствором щелочи, добавление которой регулируются автоматически. Через 72 часа культивирования в среду вносят предшественник биосинтеза – 5,6-диметилбензимидазол. Без введения предшественника бактерии синтезируют не имеющий клинического значения псевдовитамин В12, в котором азотистым основанием служит аденин. После введения предшественника ферментацию продолжают ещё 72 часа до содержания витамина в биомассе не менее 250 мкг/г.
Установлено, что основное накопление содержания витамина В12, синтезируемое пропионовыми бактериями, выращенными на сывороточной среде, наблюдается на ранней фазе логарифмического роста (до 72 часов инкубации).
132
Количественное содержание витамина В12, продуцируемое Propionibacterium shermanii, устанавливают микробиологическим методом по зонам роста витаминзависимого штамма E. Coli 133-3.
Витамин В12 накапливается в клетках бактерий, поэтому по окончании процесса культивирования биомассу отфильтровывают или сепарируют и экстрагируют из нее витамин при температуре 85 ± 5 °С водой, подкисленный до рН 4,5–5,0.
Затем водный экстракт витамина охлаждают, доводят раствором щелочи рН до 6,8–7,2; к раствору добавляют сульфат аммония и раствор хлорного железа для коагуляции белков. Коагулят белков, отделяют на фильтр-прессе, и водный экстракт витамина В12 поступает на стадию выделения и очистки кристаллического продукта.
Витамин В12 из водного экстракта, освобожденного от белков, сорбируют на ионообменной смоле СГ-1 и элюируют водным раствором аммиака. Далее элюат пропускают через колонки с окисью алюминия, при этом витамин сорбируется на окиси алюминия, а примеси удаляются с маточным раствором.
С окиси алюминия В12 элюируют водным ацетоном, к водноацетоновому элюату добавляют безводный ацетон до помутнения раствора и смесь выдерживают при температуре 3 ± 1 °С в течение 24–48 ч, при этом происходит кристаллизация витамина В12. Выделившиеся кристаллы технического витамина отфильтровывают, промывают безводным ацетоном, эфиром и сушат в вакууме.
Для химической очистки витамина В12 используют его способность образовывать аддукты (комплексы) с фенолом, резорцином или крезолами. Для этого водный концентрат витамина обрабатывают водным раствором фенола, отделяют фильтрованием выделившийся комплекс, затем его разлагают путем обработки водным ацетоном. Витамин при этом выделяется в виде осадка, а фенол и примеси уходят с водно-ацетоновыми маточными растворами. Для окончательной очистки осуществляют одноили двукратное переосаждение цианокобаламина из водного раствора ацетоном.
Необходимо отметить, что штаммы пробиотиков кишечника человека и животных способны продуцировать цианокобаламин. Поддержание микрофлоры кишечника является гарантией обеспечения нашего организ-
133
ма витамином В12. Так, например, Lactobacillus reuteri CRL 1098 предотвращает побочные эффекты, вызванные дефицитом при питании витамина В12. Кроме того, обнаружено влияние содержания и типа аминокислот на продукцию витамина В12 при культивировании Lactobacillus reuteri.
4.3. Получение витамина D2
В группу витаминов D объединены близкие по своей структуре и функции соединения – витамины D2 и D3. Они оба обладают антирахитическим действием. Недостаток витамина D в рационе детей приводит к возникновению широко известного заболевания – рахита, в основе развития которого лежат изменения фосфорно-кальциевого обмена и нарушения отложения в костной ткани фосфата кальция. Поэтому основные симптомы рахита связаны с нарушением нормального процесса костеобразования. Развивается остеомаляция – размягчение костей. Кости становятся мягкими и под тяжестью тела принимают уродливые формы.
Витамин D2 (эргокальциферол) получают путем микробиологиче-
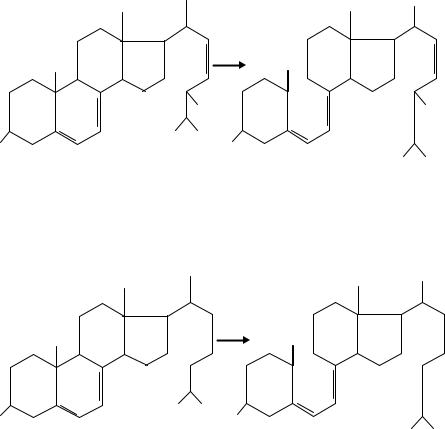
ского синтеза, при производстве которого применяют дешевое сырье (углеводороды) и установлен стимулирующий эффект ультрафиолетовых лучей на синтез эргостерина культурой дрожжей. Эргостерин и является предшественником жирорастворимого витамина D2 Установлено, что под действием ультрафиолета в дрожжевых клетках происходит фотохимическое превращение эргостерина в эргокальциферол. С химической точки зрения эргостерин представляет собой одноатомный ненасыщенный циклический спирт, в основе структуры которого лежит кольцо циклопентанопергидрофенантрена. Под действием УФ-лучей эргостерин через ряд промежуточных продуктов (люмистерин, тахистерин) превращается в витамин D2. В 1936 году Брокман выделил активный в отношении рахита препарат из рыбьего жира и назвал его витамином D3. Установлено, что предшественником витамина D3 является не эргостерин, а холестерин. На рис. 14 показано получение витамина D2 и D3.
134
СН3
СН3
УФ
Н3С
|
СН3 |
|
НО |
СН3 СН3 |
НО |
|
Эргостерин |
|
СН3
СН3
УФ
Н3С
НО |
СН3 СН3 НО |
|
7-Дегидрохолестерин |
СН3 СН3
Н2С
СН3
СН3 СН3
Витамин D2 (эргокальциферол)
СН3 СН3
Н2С
СН3 СН3
Витамин D3 (холекальциферол)
Рисунок 14 – Получение витамина D2 и D3
135
Продуценты эргостерина представлены в табл. 12.
Таблица 12 – Содержание эргостерина у микроорганизмов
Микроорганизмы |
Количество эргостерина, % |
|
(на сухое вещество) |
||
|
||
|
|
|
Saccharomyces ellipsoids |
1,2–1,5 |
|
|
|
|
Rhodotorula glutinis |
0,7–0,9 |
|
|
|
|
Candida utilis |
0,4–0,6 |
|
|
|
|
Candida tropicalis |
0,2–0,3 |
|
|
|
|
Aspergilius |
1,2–1,4 |
|
|
|
|
Penicillium Westlingii |
2,2 |
|
|
|
Для получения витамина D2 из дрожжей или мицелия их биомассу гидролизуют в автоклаве, используя на 100 кг дрожжей или грибного мицелия 20 л воды и 10 мл концентрированной соляной кислоты. Гидролиз проводят при температуре 10 °С в течение 20–30 минут. Затем гиролизованную массу обрабатывают спиртом (40–50 мин) при 75–78 °С в специальном коагуляторе. Массу охлаждают до 10–15 °С и фильтруют. Фильтрат концентрируют, отделяя спирт и часть воды, получают концентрат витаминов группы В. Массу, оставшуюся после фильтрации, промывают водой, отгоняют спирт и воду. Полученную массу сушат до влажности 2 % и размельчают. Порошок дрожжей при 78 °С в экстракторе обрабатывают трехкратным объемом спирта-ректификата. После отделения раствора осадок повторно экстрагируют спиртом, который удаляют из экстракта, а осадок сгущают до 70 % содержания сухих веществ. Из 100 кг дрожжей получают 20–25 кг липидного концентрата. Концентрат омыляют щелочью, после чего раствор кристаллизуют при 0 °С и облучают УФ-лучами при 280–230 нм. На выход витамина D2 оказывает влияние длительность облучения УФ-лучами, температура и наличие сопутствующих примесей.
136
4.4. Получение β-каротина
Важное место в обмене веществ у животных занимает -каротин, который в печени превращается в витамин А (ретинол). Ретинол (витамин А – (С20Н30О)) необходим для нормального течения метаболических процессов, в том числе для регуляции роста и развития организма. Обеспечивает нормальную функцию зрения, структурную целостность тканей, повышает резистентность организма к воздействию неблагоприятных факторов окружающей среды. При неполноценном питании и некоторых заболеваниях пищеварительного тракта и печени наблюдается дефицит витамина А (авитаминоз). Ранним признаком последнего является ухудшение сумеречного зрения, снижение аппетита, уменьшение массы тела, снижение неспецифической резистентности организма к инфекциям, нарушения со стороны кожи и др. Кроме того, в последнее время появились сообщения о том, что ретинол связан с регулированием сигнальных путей ядерных рецепторов, что активирует гены в организме человека и животных. Установлено, что витамин А отвечает за активацию ядерного рецептора TR4. Известно, что TR4 влияет на производство сперматозоидов, липидов и липопротеидов, развитие клеток центральной нервной системы и регулирование синтеза гемоглобина в зародыше. Ядерные рецепторы отвечают за активирование генов, обеспечивающих важные биологические процессы в организме. Одновременно, исследователям удалось выделить молекулы веществ, участвующих в транскрипции TR4, а именно, синтезе РНК на матрице ДНК. Полученные данные могут быть использованы для создания нового поколения лекарственных препаратов, полученных биотехнологическим путем.
В организме человека и животных каротины не образуются. Основные источники -каротина для животных – растительные корма; человек получает -каротин также из продуктов животного происхождения. Из ряда растительных объектов (морковь, тыква, облепиха, люцерна) можно выделить -каротин. В начале 60-х годов ХХ века была разработана схема микробиологического синтеза -каротина, которая стала основой промышленного способа его получения. Установлено, что многие микроорганизмы (фототрофные бактерии, актиномицеты, плесневые грибы, дрожжи) синтезируют -каротин. Характерно, что содержание -каротина у микроорга-
137