Материал: Фарм производство БАР
1920 г. – ученые К. Матилл и А. Конклин показали, что в смешанной пище содержится вещество, которое абсолютно необходимо для нормального размножения животных. Активное вещество, предохраняющее от бесплодия, было выделено из масла пшеничных зародышей и из хлопкового масла и названо витамином Е;
1924 г. – американские ученые А. Гесс, Г. Стинбок и М. Вайншток из растительных масел и продуктов питания после облучения их УФлучами с длиной волны 280–310 нм получили активный препарат, предотвращающий развитие рахита у детей. Вещество было идентифицировано с эргостерином и названо витамином D1. В 1936 году ученый А. Виндаус выделил эргостерол из дрожжей и показал, что истинным витамином D является не эргостерин, а продукт его превращения, образующийся при УФ облучении, который был назван витамином D2.
1927–1929 г.г. – американский ученый Сент-Дьерди А. установил структуру витамина С – аскорбиновой кислоты;
1929 г. – установлено, что витамины связаны с ферментами, являясь для них кофакторами. Хопкинс Ф. Г. и Эйкман Х. были удостоены Нобелевской премии за открытие антиневрического витамина (В1 – тиамин) и открытие витамина роста;
1930–1931 г.г. – швейцарский ученый Каррер П. установил, что из β-каротина образуется витамин А;
1933 г. – Каррер П. установил, что вещество рибофлавин идентично витамину В2;
1933 г. – американский ученый, биохимик Р. Вильямс открыл пантотеновую кислоту – витамин В5;
1929–1939 г.г. – датский ученый Дам Х. и американский ученый Дойзи Э. А. открыли витамин К;
1936 г – американский ученый Сент-Дьерди А. из кожуры лимона выделил рутин, названный витамином Р;
1937 г. – американский ученый Эльвегейм К. А. из экстракта печени выделил чистую никотиновую кислоту – витамин РР;
1934 г. – Сент-Дьерди А. получил Нобелевскую премию за открытие витамина В6 – пиридоксина;
1948 г. – американским ученым Дороти Кроуфут-Ходжкин открыт витамин В12.
118
Исследования, направленные на изучение структуры витаминов и их биологического значения продолжаются и сегодня.
Таким образом, витамины представляют собой группу незаменимых органических соединений различной химической природы, необходимых любому организму в ничтожных концентрациях и выполняющих в нем каталитические и регуляторные функции. Недостаток того или иного витамина нарушает обмен веществ и нормальные процессы жизнедеятельности организма, приводя к развитию патологических состояний. Витамины не образуются у гетеротрофов. Способностью к синтезу витаминов обладают лишь автотрофы, в частности растения. Многие микроорганизмы также образуют целый ряд витаминов. В связи с этим синтез витаминов с помощью микроорганизмов стал основой для разработки технологий промышленного производства этих биологически активных соединений.
Благодаря изучению физиологии и генетики микроорганизмов (продуцентов витаминов) и выяснению путей биосинтеза каждого из них создана теоретическая основа для получения микробиологическим способом практически всех известных в настоящее время витаминов. Однако с помощью энзимов целесообразнее производить лишь особо сложные по строению витамины: В2, В12, -каротин (провитамин А) и предшественники витамина D. Остальные витамины либо выделяют из природных источников, либо синтезируют химическим путем. Витамины используются в качестве лечебных препаратов, для создания сбалансированных пищевых и кормовых рационов и для интенсификации биотехнологических процессов.
Необходимо отметить, что в организме человека и животных источником синтеза витаминов являются микроорганизмы кишечника. Так, микроорганизмы синтезируют фолиевую кислоту в количествах, достаточных для удовлетворения потребностей организма в этом витамине. Витамин В12 (кобаламин) также может синтезироваться микрофлорой кишечника при условии доставки с пищей кобальта. Микрофлорой кишечника также синтезируется витамин В3 (пантотеновая кислота) и фолиевая кислота в количествах, достаточных для удовлетворения потребностей организма в этом витамине. Микрофлора кишечника является важным источником
119
биотина (витамин Н), пиридоксина (витамин В6), тиамина (витамин В1), частично обеспечивающая потребность организма человека и животных.
Производство витаминов осуществляется следующими основными путями:
1.Экстракция витаминных препаратов из растительного или жи-
вотного сырья. С этого направления начиналась витаминная промышленность, поскольку первые витаминные препараты были получены именно таким путем. Например, витамин В12 получали из сырой печени крупного рогатого скота, каротин – из моркови. Но в настоящее время доля витаминов, получаемых этим методом, незначительна ввиду очень низкого содержания их в природном сырье и ограниченности сырьевых ресурсов.
2.Химический синтез витаминов. Производство синтетических витаминов занимает, пожалуй, ведущее место в современной витаминной промышленности. Основная номенклатура витаминов представлена веществами, полученными химическим синтезом из химических видов сырья или сочетанием химического синтеза с биосинтезом. Однако такой способ производства витаминов представляет собой сложный, многоступенчатый процесс, сопряженный с большими производственными затратами, что повышает себестоимость продукции и делает конечные продукты слишком дорогими.
3.Биосинтез витаминов. Получение витаминов осуществляют микробиологическим способом с использованием штаммов-продуцентов. Сегодня, основные витамины, используемые в фармации, получены при помощи биосинтеза: рибофлавин, цианокобаламин, аскорбиновая кислота, эргокальциферол, никотиновая кислота и др.
В табл. 10 представлены химические структуры витаминов, используемых в составе лекарственных препаратов.
120
Таблица 10 – Химические структуры витаминов
Витамины |
Химическая структура |
|
|
1 |
2 |
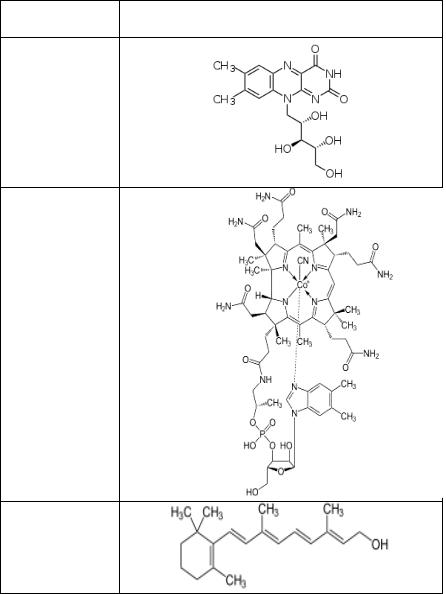
Витамин В2 (рибофлавин)
Витамин В12 (цианокобаламин)
Витамин А (ретинол)
121
Продолжение таблицы 10
1 |
2 |
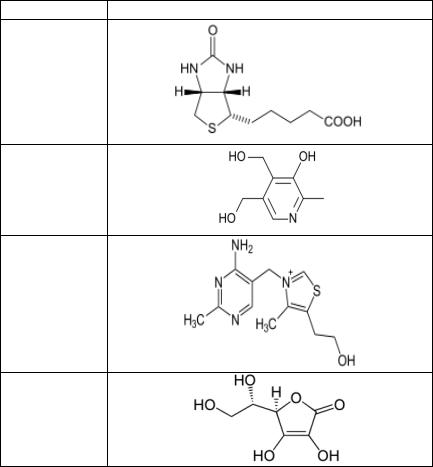
Витамин Н (биотин)
Витамин В6 (пиридоксин)
Витамин В1 (тиамин)
Витамин С (L-аскорбиновая кислота)
122
4.1. Производство витамина В2 (рибофлавин)
Витамин В2 (рибофлавин C17H20N4O6) входит в состав флавиновых ферментов, участвующих в транспорте водорода (тканевом дыхании) и образовании АТФ в митохондриях. Рибофлавин используют для лечения людей с гиповитаминозом, конъюнктивитом, кератитом, вирусным гепатитом А, заболеваниями печени, железодефицитной анемии, лучевой болезни и др.
Вплоть до 30-х годов прошлого столетия рибофлавин выделяли из природного сырья. В наибольшей концентрации он присутствует в моркови и печени трески. Из 1 тонны моркови можно выделить только 1 грамм рибофлавина, а из 1 тонны печени – 6 грамм витамина. В 1935 году обнаружен активный продуцент рибофлавина – гриб Eremothecium ashbyii, способный при выращивании на 1 тонне питательной смеси синтезировать 25 кг витамина В2. Сверхсинтез рибофлавина добиваются действием на дикие штаммы мутагенов, нарушающих механизм ретроингибирования синтеза витамина В2, флавиновыми нуклеотидами, а также изменением состава культуральной среды. Отбор мутантов ведут по устойчивости к аналогу витамина В2 – розеофлавину.
В состав среды для роста продуцентов витамина В2 входят комплексные компоненты – соевая мука, кукурузный экстракт, меласса, сахароза, карбонат кальция, натрия хлорид, гидрофосфат калия, витамины, минеральные вещества. Продуценты витамина В2 выращивают на средах, где в качестве источника углерода используют глюкозу, сахарозу, крахмал, пшеничную муку, а в качестве источника азота используют молочную сыворотку, рыбную и кукурузную муку, казеин и др. Для культивирования продуцента используют биотин, тиамин, инозит, ростовые вещества, содержащиеся в зародыше пшеницы, картофельном соке и автолизате дрожжей. Установлено, что биосинтез рибофлавина продуцентом Eremothecium ashbyii стимулируется липидами. Так, при добавлении в питательную среду кукурузного или соевого масла (0,5–1,0 % отходов масложировых комбинатов) выход рибофлавина увеличивается вдвое. Грибы весьма чувствительны к изменению состава среды и подвержены инфицированию. Перед подачей в ферментер, среду подвергают стерилизации, добавляя к ней ан-
123
тибиотики и антисептики. Готовят жидкую питательную среду и посевной материал культуры дрожжей в разных емкостях – ферментере и посевном аппарате. Культивирование продуцента проводят поверхностным или глубинным способом. Витамин накапливается в клетках гриба-продуцента, либо в виде предшественника – флавина дениннуклеотида, либо в свободном состоянии.
Среда проходит стерилизацию при 120–122 °С в течение 1 часа. Культивирование ведут при оптимальной температуре 28–30 °С и давлении 104 Па при расходе воздуха 1,5–2,0 литра в минуту до начала лизиса клеток и появления спор, которые определяют микроскопически. При биосинтезе рибофлавина начальное значение рН 6,0–7,0; в процессе роста грибов (Eremothecium ashbyii, Ashbyii gossipii) рН снижается до 4,5. Поэто-
му для эффективного синтеза рибофлавина величину рН постоянно поддерживают на уровне 9,5. После окончания процесса ферментации культуральную жидкость вместе с мицелием передают в вакуум-выпарные аппараты, где её нагревают до 80 °С с целью разрушения (термолиза) клеточных структур с одновременным концентрированием.
Вкачестве посевного материала используют споры Eremothecium ashbyii, выращенные на пшене (7–8 дней при 29–30 °С). После стерилизации, жидкий посевной материал подается в ферментер. При процессе ферментации грибов для получения кормового рибофлавина концентрация витамина в культуральной жидкости может достигать 1,4 мг/мл. По завершении процесса ферментации культуральную жидкость концентрируют в вакууме, высушивают на распылительной сушке (до влажности 5–10 %) и смешивают с наполнителями.
В1983 году во ВНИИ генетики микроорганизмов был сконструирован рекомбинантный штамм продуцента Bacillus subtilis, характеризующийся увеличенной дозой оперонов, которые контролируют синтез рибофлавина. Клонированием генов рибофлавинового оперона в одной из созданных плазмид был получен производственный штамм-продуцент витамина В2, способный синтезировать втрое больше по сравнению с Eremothecium ashbyii количество рибофлавина всего за 42 часа ферментации. Работа по получению продуцента проходила в несколько этапов:
124
І этап – конструирование с применением генетико-селекционных методов реципиентного штамма B. subtilis Y6 с нарушенной системой рекомбинации;
ІІ этап – конструирование с применением генетико-селекционных методов рекомбинантной плазмиды, несущей рибофлавиновый оперон штамма B. subtilis 53A с нарушенной негативной регуляцией;
ІІІ этап – конструирование рекомбинантного штамма продуцента ри-
бофлавина B. subtilis 62/pMX30ribО 186.
Известно, что биосинтез рибофлавина B. subtilis подвержен негативному контролю. Имеется два вида мутаций, снимающих этот кон-
троль: мутации в операционной области рибофлавинового оперона ribO и мутации по репрессору биосинтеза рибофлавина ribC. На первом этапе получения резистентного штамма в штамм B. subtilis RK6121 методом генетической трансформации вводят мутации ribС 862 и ribO 186. Затем для увеличения пула предшественника рибофлавина (гуанозин-5-трифосфата) методом мутагенеза in vivo под действием N-метил-N- нитрозонитрогуаницина и ультрафиолета последовательно вводят мутации, определяющие устойчивость к 0,5 мг/мл 8-азагуанина и к 10 мг/мл метионин-сульфоксида. Этот штамм синтезируют до 4 г/л рибофлавина за 48 часов.
Конструирование рекомбинантной плазмиды: к бациллярному век-
тору рМХ30 определяющему устойчивость бацилл к эритромицину и имеющему размер 18,3 т.п.н. (тысяч пар нуклеотидов) присоединяют фрагмент ДНК с рибофлавиновым опероном B. subtilis 53A, содержащим мутацию ribO 186 в операторной области. В результате была получена плазмида, которой присвоено название pMX30ribO 186, обуславливающая устойчивость к 10 мкг/мл эритромицина и имеющая размер 28,6 т.п.н.
Конструирование рекомбинантного штамма B. subtilis
62/pMX30ribO 186: в штамм B. subtilis Y6 методом генной трансформации вводят плазмиду pMX30ribO 186. Полученный продуцент позволяет получить высокий выход рибофлавина: 12,4 г/л за 42 часа аэрации (культивирование при температуре 37–43 °С, аэрация 15 г О2/ч).
Для получения рибофлавина с повышенным выходом, постоянно проводится изучение продуцентов витамина и создание новых рекомби-
125
нантных штаммов, разработка оптимального состава питательных сред и определение условий культивирования.
Так, например, морские дрожжи Candida membranifaciens subsp.
Flavinogenie W14-3, выделенные из вод Восточно-Китайского моря секретируют рибофлавин в среду при росте на ксилозе в течение 24 часов и температуре около 25 °С. Культивирование оптимизировали с использованием 4-х переменных: содержания ксилозы, величины рН, температуры выращивания, а также скорости перемешивания дрожжевых клеток при инкубации. Исследователи добились выхода рибофлавина не менее 22 мг/мл при 54 часах инкубации. Максимальное количество витамина наблюдалось во время нахождения клеток в поздней стационарной фазе.
Рядом исследователей были отобраны мутанты Ashbya gossypii, продуцирующие повышенное количество рибофлавина и способные к эффективному синтезу витамина на среде с апельсиновой кожурой. Такая среда богата маслами, утилизируемыми микроорганизмами, продукты которого активизируют образование рибофлавина. Когда в ферментационной среде отобранных мутантов, солодовый экстракт был замещен апельсиновой кожурой (0,3 %) максимальная продукция витамина была на 180 % выше контроля, выращенного в культуральной среде, содержащей солод.
Проведено изучение метаболических изменений при биосинтезе рибофлавина на примере периодического культивирования сверхпродуцента витамина Bacillus subtilis PK. При разрушении гена оксидазы bd Bacillus subtilis PK обнаружено повышение удельной скорости развития культуры
иувеличение выхода биомассы. У мутанта cyd синтез побочного продукта снижался, и образовывалось больше ацетоина. Метаболические потоки были сокращены и источники углерода расходовались на синтез биомассы
ирибофлавина (повышение на 30 %). Корреляция между выходом биомассы и продуктивностью Bacillus subtilis PK cyd указывает на возможность эффективной генерации энергии для экспоненциального роста сверхпродуцента рибофлавина при периодическом культивировании. Оптимизирован состав питательной среды, а именно источники азота для продукции рибофлавина ccpA мутантом Bacillus subtilis 24A1/pMx45. Оптимальный состав среды: 8 % глюкозы (источник углерода), 2 % дрожжевого порошка, 0,05 % MgSO47H2O и 3 источника азота (0,1 % дрожжевого экстракта,
126
2 % соевой муки, 0,2 % (NH4)2HPO4). В оптимальных условиях выход рибофлавина достигал 5,0 г/л. Установлено, что 8 % глюкозы может быть полностью израсходовано за 60 часов культивирования.
Взаключение хотелось бы отметить, что для выделения рибофлавина
влабораторных и производственных условиях используют культуры различных микроорганизмов (см. табл. 11).
Таблица 11 – Микроорганизмы, являющиеся продуцентами рибофлавина
Микроорганизмы – продуценты |
Выход витамина |
|
(мг, %) |
||
|
||
|
|
|
Clostridium acetobytylicum |
97 |
|
|
|
|
Mycobacterium smegmatis |
58 |
|
|
|
|
Mycocandida riboflavina |
200 |
|
|
|
|
Bacillus subtilis 24A1/pMx45 |
500 |
|
|
|
|
Candida flaveri |
567 |
|
|
|
|
Bacillus subtilis 62/pMX30ribO186 |
1240 |
|
|
|
|
Candida membranifaciens subsp. Flavinogenie W14-3 |
2200 |
|
|
|
|
Eremothecium ashbyii |
2480–6000 |
|
|
|
|
Ashbyii gossipii |
6420 |
|
|
|
Для получения рибофлавина можно использовать химический синтез, в котором в качестве исходных компонентов применяют 3,4-диметиланалин и D-рибозу, полученную микробиологическим путем. Для биосинтеза рибозы используют транскетолазные мутанты: Bacillus Subtilis, Penicillium brevi-compactum и Pseudomonas reptilivora. В питатель-
ных средах для культивирования продуцентов в качестве источника углерода используются глюкоза и крахмал. В среду вносят соли аммония, фосфаты калия, соли магния. В ряде случаев в состав среды вводят дрожжевой
икукурузный экстракт. Например, в случае Bacillus Subtilis D-рибозa начинает накапливаться пропорционально потреблению глюкозы на 1–2 день
изаканчивается на 4-й день. Максимальный выход D-рибозы наблюдается при температуре культивирования 36,5–36,6 °С. Выделение и очистку
127