Материал: Электролитическое рафинирование меди
.4.1 Свойства электролита
а) Плотность электролита ρэл, г/см3, определяется на
основании принципа аддитивности:
ρэл = 0.01(ρ1а1 + ρ2а2 + … + ρiаi), (48)
где ρ1, ρ2, … ρi - плотность компонентов раствора, кг/дм3;, a2,… ai - объемная концентрация компонентов раствора, %.
Плотности компонентов равны: ρCuSO4 = 3.603; ρNiSO4 = 4.010; ρH2SO4 = 1.841;
ρH2O = 1.000 (справочные данные).
Для заданного состава электролита, г/дм3 (45.0 Cu, 10.0 Ni, 160.0 H2SO4):
aCuSO4 = 45.0·159.60·100)/(63.54·3.603·1000) = 3.137;= 10.0·154.76·100/(58.70·4.010·1000) = 0.657;SO4 = 160.0·100/(1.841·1000) = 8.691;O = 100.0 - (3.137 + 0.657 + 8.691) = 87.515 (по разности).
Здесь 159.60, 154.76 - молярные массы сульфатов меди и никеля; 63.54, 58.70 - атомные массы меди и никеля.
ρэл = 0.01(3.603·3.137 + 4.010·0.657 +
1.184·8.691 + 1.000·87.515) = 1.117.
б) Теплоемкость электролита Сэл, кДж/(кг·град), также определяется на
основании принципа аддитивности:
![]() ,(49)
,(49)
где С1, С2, … Сi - удельные теплоемкости компонентов электролита, Дж/(г·К) (табл. 2);, X2, … Xi - массовые доли компонентов электролита, доля ед.
Массовые доли компонентов Xi в электролите:
Xi = mi / ρэл(50)
где: mi - масса i - го компонента в 1 дм3 электролита, г;
![]() - плотность электролита, г/дм3 (1117).
- плотность электролита, г/дм3 (1117).
Таблица 2
Удельная теплоемкость компонентов электролита, Дж/(г·К)
|
Компонент |
Температура, К |
||||||
|
|
293 |
303 |
313 |
323 |
333 |
343 |
353 |
|
CuSO4 |
0.6122 |
0.6249 |
0.6370 |
0.6486 |
0.6596 |
0.6701 |
0.6802 |
|
NiSO4 |
0.8903 |
0.8930 |
0.8957 |
0.8984 |
0.9011 |
0.9037 |
0.9064 |
|
H2SO4 |
1.4052 |
1.4243 |
1.4627 |
1.4821 |
1.5016 |
1.5211 |
|
|
H2O |
4.1851 |
4.1814 |
4.1804 |
4.1816 |
4.1849 |
4.1901 |
4.1970 |
Для заданного состава электролита, г/дм3 (45.0 Cu, 10.0 Ni, 160.0 H2SO4):
![]() = 45.0 · 159.6 / 63.54 = 113.0;
= 45.0 · 159.6 / 63.54 = 113.0;
![]()
![]()
![]()
где: 45.0, 10.0 160 - концентрации компонентов (по заданию);
.6, 154.8 - молярные массы сульфатов меди и никеля;
.54, 58.71 - атомные массы меди и никеля, соответственно;= 113.0 / 1117 = 0.1012;= 26.4 / 1117 = 0.0236;SO4 = 160.0 / 1117 = 0.1432;O = 861.6 / 1117 = 0.7714.
Удельная теплоемкость компонентов электролита (табл. 5) при температуре
Тэл = 336 К, кДж/(кг·град), определяется методом интерполяции:
![]()
![]()
![]()
![]()
Удельная теплоемкость электролита при температуре Тэл = 336 К, кДж/(кг·град):
Cэл = 0.6628·0.1012 + 0.9019·0.0236 + 1.4880·0.1432 + 4.1865·0.7714 = 3.531.
в) Удельная электропроводность электролита κ, См/см, нелинейно зависит от
концентрации его компонентов, ее рассчитывают для электролитов с концентрацией,
г/дм3: меди Cu 30…50, никеля Ni 0…33, серной кислоты S 158…225 при
температуре T 328…348 K по полиному [3]:
κ = 0.04 - 0.2656·Сu - 0.0815·Ni + 0.3513·S +
0.3842·[T-273] + 0.0025·Сu2 + 0.00267·Ni2 -
0.000503·S2 - 0.00407·[T-273]2 + 0.00241·Сu·Ni - 0.001585·Сu·S - 0.00201·Ni·S -
0.001766·Ni·[T-273] + 0.00273·S·[T-273],(51)
где Сu - концентрация ионов меди в растворе, г/дм3 (45); Ni - концентрация ионов никеля в растворе, г/дм3 (10); S - концентрация серной кислоты в растворе, г/дм3 (160); T - температура электролита, К (336).
κ = 0.04 - 0.2656·45 - 0.0815·10 +
0.3513·160 + 0.3842·60 + 0.0025·452 + 0.00267·102 - 0.000503·1602 - 0.00407·602
+ 0.00241·45·10 - 0.001585·45·160 -0.00201·10·160 - 0.001766·10·60 +
0.00273·160·60 = 56.85.
2.5 Электрический баланс электролизной ванны
Баланс напряжения на ванне складывается из следующих величин [4], В:
Uв = Ер + ΔЕа-к + ΔUэл + ΔUшл + ΔUшт + ΔUтэ + ΔUконт (52)
где Ер - напряжение разложения; ΔЕа-к - электродная поляризация; ΔUэл - падение напряжения в электролите; ΔUшл - падение напряжения в шламе; ΔUшт - падение напряжения в катодных штангах; ΔUтэ - падение напряжения в теле электродов; ΔUконт - падение напряжения в контактах.
а) Напряжение разложения Ер определяется по разности термодинамических потенциалов анода и катода:
![]() (53)
(53)
![]()
б) Электродная поляризация ΔЕа-к определяется как разность
перенапряжений анодного и катодного процессов, которые при заданных значениях
плотности тока и температуры могут быть приняты равными соответственно +0.02 В
и -0.02 В, т.е.
ΔЕа-к = ΔЕа - ΔЕк = 0.020 - (-0.020) = 0.040.
в) Падение напряжения в электролите ΔUэл
эл = Rэл · I, (54)
где Rэл - сопротивление электролита, Ом;- сила тока через электролизер,
А.
![]() , (55)
, (55)
где ![]() - удельная электропроводность электролита, См/см (56.85); λ
- расстояние между анодом
и катодом, м;
- удельная электропроводность электролита, См/см (56.85); λ
- расстояние между анодом
и катодом, м;
λ = (ℓмэр - δк - δа)/2 = (0.102 - 0.004 - 0.0385)/2 =
0.02975;
S - сечение электролита, по которому протекает ток между анодом и
катодом, м2:
S = ![]()
где ![]() - число межэлектродных промежутков.
- число межэлектродных промежутков.
![]() , (56)
, (56)
где Sк - рабочая поверхность катодов (матриц) м2:
![]() (57)
(57)
Sк = 2 · 33 · 0.88 · 0.98 = 56.92.
I = 270 · 56.92 = 15368.эл = 9.39 · 10-6 · 15368 = 0.14.
г) Падение напряжения в шламе ΔUшл составляет 10-15% от падения напряжения в электролите [4] и равно, В:
ΔUшл = 0.14 · 0.12 = 0.017.
д) Падение напряжения в контактах ΔUконт составляет 15-17% [4] и равно:
ΔUконт = (0,15 ÷
0,17)·(Σηа,к +
ΔUэл + ΔUшл + ΔUконт), (58)
По данным практики и литературным источникам [2, 6, 7, 8] Σηа,к = 0.080 В. Тогда:
ΔUконт 0.17 · (0.08 + 0.16 + 0.0017+
ΔUконт),
ΔUконт = ![]() = 0,053 В
= 0,053 В
е) Падение напряжения в теле электродов ΔUтэл определяется электрическим
сопротивлением, Ом, тела анода R.та и тела катода Rтк при температуре
электролита
ΔUтэл = Iшт · (R.та + Rтк) (59)
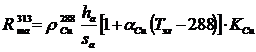 (60)
(60)
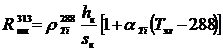 (61)
(61)
где: ![]()
![]() - удельное сопротивление при температуре 288 К, Ом·мм2/м,
титана (0.435) и меди (0,0175);
- удельное сопротивление при температуре 288 К, Ом·мм2/м,
титана (0.435) и меди (0,0175);
αCu , αTi - температурный коэффициент удельного сопротивления, град-1 , меди (0.004) и титана (0.006)
КСu - коэффициент, учитывающий повышение электрического сопротивления черновой меди по сравнению с чистой медью (10);а , hк - высота, м, анода (0.960) и катода (матрицы - 0.980);а , sк - поперечное сечение, мм2, анода (860·38.5) и катода (матрицы - 880·4);
![]() = 0.0175·0.960·[1 + 0.004·(336 - 288)] ·10 / (860·38.5) =
6.05·10-6,
= 0.0175·0.960·[1 + 0.004·(336 - 288)] ·10 / (860·38.5) =
6.05·10-6,
![]() = 0,435·0,980·[1 + 0.006·(336 - 288)] / (880·4) = 1.56·10-4
= 0,435·0,980·[1 + 0.006·(336 - 288)] / (880·4) = 1.56·10-4
ΔUтэл = 466 · (6.05·10-6 + 1.56·10-4) = 0.075.
Электрический баланс ванны (таблица 3) показывает, что основная статья
баланса напряжений - падение напряжений в электролите. Снижение этой величины
является одной из задач для уменьшения удельного расхода электроэнергии при
электрорафинировании меди.
Таблица 3
Электрический баланс электролизной ванны
|
Статьи баланса |
Падение напряжения |
|
|
|
В |
% |
|
Электродная поляризация ΔЕа-к |
0.040 |
12.3 |
|
Падение напряжения в электролите ΔUэл |
0.140 |
43.1 |
|
Падение напряжения в шламе |
0.017 |
5.2 |
|
Падение напряжения в контактах ΔUконт |
0.053 |
16.3 |
|
Падение напряжение в теле электродов |
0.075 |
23.1 |
|
Итого: |
0.325 |
100.0 |
Удельный расход электроэнергии постоянного тока Wуд, кВт·час/т:
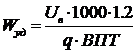 (62)
(62)
где: 1.2 - коэффициент, учитывающий падение напряжения в подводящих шинах от подстанции до серии;- электрохимический эквивалент меди, г/(А·час)(1.186);
ВПТ - выход меди по току на катоде, % (96.8).
Wуд = 0.325 · 1000 · 1.2 / (1.186 · 0.968) = 339.7.
2.6 Тепловой баланс электролизной ванны
.6.1 Статьи прихода тепла
а) Тепло, выделяемое при прохождении электрического тока Q1:
= 3.6 · I · (Uв - ΔUконт), (63)
= 3.6 · 15368 · (0.325 - 0.053) = 15.60·103.
б) Тепло, поступающее с электролитом Q2 - рассчитывается по итогам
составления баланса.
2.6.2 Статьи расхода тепла
в) Потери тепла на испарение воды с зеркала электролита Q3, [1]:
![]() (64)
(64)
где: ![]() - количество воды испаряющейся за 1 час с 1 м2 поверхности
электролита, кг:
- количество воды испаряющейся за 1 час с 1 м2 поверхности
электролита, кг:
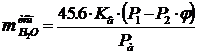 ,(65)
,(65)
где: 45.6 - плотность потока испарения при температуре окружающего воздуха Тв (373 К) в сухой воздух (при Р1 = 0 и Р1 = Р2), кг/(м2·час) [1]
Кв - коэффициент, характеризующий условия отвода пара (0.70 - для медленно движущегося воздуха)
Р1 - давление насыщенного водяного пара в помещении при температуре
электролита Тэл (336 К), Па (1.992 ·104) (табл. 4);
Таблица 4
Давление насыщенного водяного пара
|
Температура, К |
293 |
303 |
313 |
323 |
333 |
343 |
353 |
|
Давление, Па/10^4 |
0.233 |
0.425 |
0.738 |
1.234 |
1.992 |
3.117 |
4.738 |
Значение Р1 для температуры электролита 336 К найдено методом
интерполяции:
![]() ;
;
Р2 - давление насыщенного водяного пара в помещении при температуре окружающего воздуха Тв (293 К), Па (0.233 ·104) (табл. 5);
φ - относительная влажность в цехе, доли ед. (0.70).а - атмосферное давление, Па (1.013 · 105);
![]() ;
;
![]() - удельная теплота парообразования воды при Тэл (336 К),
кДж/кг
- удельная теплота парообразования воды при Тэл (336 К),
кДж/кг
Значение ![]() для температуры электролита 336 К найдено методом
интерполяции (табл. 5).
для температуры электролита 336 К найдено методом
интерполяции (табл. 5).
Таблица 5
Удельная теплота парообразования воды
|
Температура, К |
293 |
303 |
313 |
323 |
333 |
343 |
353 |
|
Удельная теплота, кДж/кг |
2448.2 |
2425.6 |
2403.0 |
2380.0 |
2356.9 |
2333.0 |
2310.0 |
![]()
исп - свободная поверхность зеркала электролита, м2 (2.209, стр. 38).= 6.828 · 2349.7 · 2.209 = 35.44·103.
г) Потери тепла зеркалом электролита лучеиспусканием и конвекцией Q4:
![]() (66)
(66)
где: Fт - теплоотдающая поверхность электролита, м2 (2.209, стр. 38);
К - коэффициент теплопередачи, кДж/(м2·час·град)
![]() (67)
(67)
где αл и αк - коэффициенты лучеиспускания и конвекции;
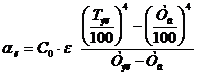 (68)
(68)
![]() (69)
(69)
где Со - коэффициент лучеиспускания абсолютно черного тела, кДж/(м2·час) (20.75);
ε - степень черноты излучающей поверхности, ед. (принимаем 0.96);
С2 - коэффициент, зависящий от расположения поверхности относительно поступающего тепла, кДж/(м2·ч) (9.009 - горизонтальная поверхность, тепло передается снизу; 4.735 - горизонтальная поверхность, тепло передается сверху; 7.123 - вертикальная поверхность);
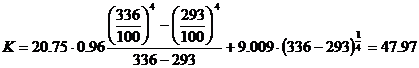 ;
;
Q4 = 47.97 · 2.209 · (336 - 293) = 4.56·103.
д) Потери тепла стенками и дном электролизера Q5 составляют в среднем 0.20 от величины Q3, т.е. Q5 = 0.20 · 35.44·103 = 7.09·103.
е) Потери тепла выступающими частями электродов Q6 составляют в среднем 0.18 от величины Q3 , т.е. Q6 = 0.18 · 35.44·103 = 6.38·103.
ж) Потери тепла с уходящим электролитом, Q7
![]() , (70)
, (70)
где ![]() - масса электролита, уходящего из ванны, кг;
- масса электролита, уходящего из ванны, кг; ![]() - удельная теплоемкость электролита,
уходящего из ванны, кДж/(кг·град) (3.531);
- удельная теплоемкость электролита,
уходящего из ванны, кДж/(кг·град) (3.531); ![]() - температура электролита, уходящего
из ванны, К (принята на 3 градуса меньше заданной температуры электролита, т.е.
333).
- температура электролита, уходящего
из ванны, К (принята на 3 градуса меньше заданной температуры электролита, т.е.
333).
![]() , (71)
, (71)
![]() = 1.05 · 1117 = 1172.9;
= 1.05 · 1117 = 1172.9;
Q7 = 1172.9 · 3.531 · (333 - 273) = 248.49·103.
Суммарный расход тепла ΣQрас:
ΣQрас. = Q3 + Q4 + Q5 + Q6 + Q7, (72)
ΣQрас. = 35.44·103 + 4.56·103 + 7.09·103 + 6.38·103 + 248.49·103 = 301.96·103.
Тепло, поступающее с электролитом, Q2 , определяется из баланса тепла:
Q2 = ΣQрас. - Q1 = 301.96·103 - 15.60·103 = 286.36·103.
Температура поступающего электролита, T3 , К:
![]() ;(73)
;(73)
![]() = 286.36·103 / (1.05 · 1117 · 3.531) = 69,
= 286.36·103 / (1.05 · 1117 · 3.531) = 69,
т.е. ![]() = 273 + 69 = 342 К, т.е. на 6 градусов больше заданной
температуры электролита (336 К).
= 273 + 69 = 342 К, т.е. на 6 градусов больше заданной
температуры электролита (336 К).
Повтор расчетов с ![]() , меньшей заданной температуры электролита на 4 градуса (332
К):
, меньшей заданной температуры электролита на 4 градуса (332
К):