Материал: Электролитическое рафинирование меди
Электролитическое рафинирование меди
Министерство образования и науки Российской Федерации
Государственное образовательное учреждение
высшего профессионального образования
Южно-Уральский государственный университет
Филиал в г. Кыштым
Кафедра
Металлургии
Пояснительная записка к выпускной квалификационной работе
Электролитическое
рафинирование меди
Руководитель работы
проф., докт. техн. Наук
Е.И. Елисеев
Автор работы
студент группы КД-494
С.С. Петров
Кыштым 2009
Задание на выпускную квалификационную работу
Студента Ивановой Марины Михайловны
Группа КД-494
. Тема работы "Электролитическое рафинирование меди" утверждена приказом по университету от "___"__________ 2009 г.
. Срок сдачи студентом законченного проекта работы 3 июня 20091.
. Исходные данные к работе:
данные производственной практики
отчеты о научно-исследовательских работах
материалы периодической печати (журналы "Цветная металлургия", "Цветные металлы").
. Содержание пояснительной записки (перечень подлежащих разработке вопросов):
краткие теоретические основы процесса электролитического рафинирования меди;
металлургический расчет с выполнением материального и теплового балансов;
расчет основных характеристик металлургического оборудования и выбор вспомогательного оборудования;
экономическая часть работы с составлением калькуляции себестоимости продукции и расчетом фонда заработной платы отделения (цеха);
охрана труда.
. Перечень графического материала (с точным указанием обязательных чертежей)
технологическая схема отделения (цеха),
чертеж основного металлургического агрегата,
чертеж наиболее важных элементов агрегата
план отделения (цеха) с расположением оборудования
таблица основных технико-экономических показателей производства
Всего 5 листов формата А1.
. Консультанты по работе с указанием относящихся к ним разделов
|
Раздел |
Консультант |
Подпись, дата |
|
|
|
|
Задание выдал |
Задание принял |
|
Экономика |
Двойнишникова О.Н. |
|
|
|
Охрана труда |
Логунова Э.Р. |
|
|
|
Технология |
Елисеев Е.И. |
|
|
. Дата выдачи задания "___" _____________ 2009 г.
Руководитель _________________(Е.И. Елисеев)
Задание принял к исполнению ___________________ (М.М. Иванова)
Аннотация
Иванова М.М. КД-494. Электролитическое рафинирование меди. - Кыштым: Филиал ЮУрГУ; 2009. 74 с. 9 ил. Библиография литературы - 16 наименований, 6 листов чертежей ф. А1.
Выпускная квалифицированная работа посвящена технологии рафинирования меди в условиях цеха электролиза меди ЗАО "Кыштымский медеэлектролитный завод".
Пояснительная записка содержит расчет основных показателей электролитического рафинирования анодной меди с использованием безосновной технологии для ЗАО "КМЭЗ". Составлены материальный, электрический и тепловой балансы. Рассчитаны основные характеристики оборудования. Технические расчеты выполнены на основе практических данных.
Экономический расчет выполнен по реальным ценам и нормам. Показана эффективность безосновной технологии производства катодной меди.
В работе рассмотрены вопросы безопасности и экологичности производства.
Оглавление
Введение
. Теоретическая часть
1.1 Физико-химические основы электролиза
1.1.1 Поведение анодов при электролизе
1.1.2 Пассивное состояние металлов
1.1.3 Перепассивация металлов
.1.4 Зарождение и рост кристаллов на катоде
1.2 Электролиз водных растворов
1.2.1 Электролиз с растворимым анодом
1.2.2 Электролиз с нерастворимым анодом
.3 Основные сведения по безосновной технологии
2. Технологическая часть
2.1 Технологическая схема участка электролиза меди
.2 Конструкция электролизера
.3 Параметры работы электролизных ванн
.3.1 Состав электролита
.3.2 Температура электролита
.3.3 Циркуляция электролита
.3.4 Плотность тока
.3.5 Межэлектродное расстояние (МЭР)
.3.6 Исходные данные
.3.7 Размеры электролизера
.4 Материальный баланс электролизной ванны
.4.1 Свойства электролита
.5 Электрический баланс электролизной ванны
2.6 Тепловой баланс электролизной ванны
2.6.1 Статьи прихода тепла
.6.2 Статьи расхода тепла
.7 Выбор оборудования
3. Экономическая часть
.1 Расчет стоимости производственных фондов
3.1.1 Производственная мощность объекта и ее использование
.1.2 Расчёт потребного количества оборудования
.1.3 Расчет стоимости производственных площадей
.1.4 Полный расчет стоимости производственных фондов
3.2 Определение численности основных производственных рабочих
3.3 Расчет фонда заработной платы
.4 Расчет себестоимости изготовления катода
3.5 Расчет экономической эффективности и срока окупаемости проектируемого технологического процесса
4. Безопасность и экологичность производства
4.1 Опасности, присутствующие при работе в цехе электролиза
4.1.1 Характеристика веществ, используемых при работе в цехе электролиза меди
.1.2 Электробезопасность
.1.3 Опасности, связанные с перемещением грузов
.2 Вентиляция
.3 Освещение помещений
4.4 Пожарная безопасность
4.5 Экологичность производства
.6 Чрезвычайные ситуации
Заключение
Библиографический
список
Введение
Производства, в основе которых лежит электроосаждение меди, занимают на медеэлектролитных предприятиях особое место. Это связано с тем, что электролитическое рафинирование позволяет не только получать медь с минимальным содержанием примесей, обладающую высокой электропроводностью, но и извлечь благородные и редкие металлы (Аu, Аg, Se, Те) из черновой меди.
Электролитическое получение меди было одним из первых освоенных гидроэлектрометаллургических процессов. По объему производства, числу действующих предприятий и степени изученности электролитическое получение меди в настоящее время занимает ведущее место в гидрометаллургии. Среди цветных металлов медь уступает по уровню потребления только алюминию.
Широкое применение меди в промышленности обусловлено низким электросопротивлением и хорошей теплопроводностью этого металла, что связано с низким содержанием различных примесей (Fе, Ni, Аs, Sb и др.). Вследствие этого более 50% всей меди, являющейся одним из лучших проводников электрического тока, лишь немного уступает серебру, расходуется электротехнической и радиотехнической промышленностью.
Большое техническое применение получили сплавы меди с Zn, Sn, Al, Si, Рb, Ве, Ni, Мn (латуни, бронзы, мельхиор, нейзильбер и др.), которые придают изготавливаемым изделиям необходимую коррозионную стойкость и хорошую теплопроводность. Распространено также применение меди в качестве легирующей добавки в сплаве на алюминиевой основе. Сплавы меди с фосфором (6-8%) используют в качестве припоев.
Всем требованиям, предъявляемым к металлу промышленностью, вполне удовлетворяет медь, полученная путем электролитического рафинирования.
Прочность меди на разрыв, вязкость и другие механические свойства, имеющие решающее значение при обработке, зависят от качества примесей. Удаление вредных примесей из меди - основная задача электролитных цехов.
Электролитическая медь идет на производство кабелей. Проводов и других изделий, применяемых в электротехнике. Прессованные и кованные изделия высокого качества, медные сплавы - также изготавливаются из электролитической меди.
Высокая электропроводность в соединении с большой пластичностью и
хорошими механическими свойствами определяют применение меди в машиностроении.
Потребителями меди являются также гальванотехника, сельское хозяйство (для
борьбы с вредителями растений в виде микроудобрения), металлургическая
промышленность.
1. Теоретическая часть
.1 Физико-химические основы электролиза
.1.1 Поведение анодов при электролизе
При электролизе растворов солей цветных металлов в целях их электроизвлечения или электрорафинирования применяют растворимые и нерастворимые аноды, материал которых выбирают в соответствии с требованиями, предъявляемыми к составу и чистоте катодных осадков.
На аноде могут протекать следующие реакции:
1) ионизация металла
Ме - 2е = Ме2+; (1)
) образование оксида металла
Ме + Н2О - 2е = МеО + 2Н+; (2)
3) выделение кислорода
ОН- - 4е = О2 + 2Н2О (3)
Н2О - 4е = О2 + 4Н+; (4)
) перезарядка ионов с повышением их валентности
Ме2+ - пе = Ме(2+n)+; (5)
5) окисление анионов
2Сl- - 2е = С12, (6)
S2- - 2е = S, (7)
S2- + 4H2O - 8е = SO![]() + 8Н+. (8)
+ 8Н+. (8)
Эти реакции протекают при различных потенциалах, либо в зависимости от конкретных условий процесса (материал электрода, состав электролита, его рН, присутствие ПАВ и т.д.) одновременно при одном потенциале. Ионизация металлов, как правило, протекает с достаточно большой скоростью, подобно разряду ионов этих металлов на катоде, и диффузия катионов от поверхности анода вглубь электролита определяет скорость электродной реакции, а увеличение анодной поляризации ∆Еа не сопровождается установлением предельного тока диффузии.
Кинетика анодного растворения металлов определяется скоростью отвода ионов от поверхности металла в объем электролита, зависящей от гидродинамических условий и концентрации ионов металла у анода и в растворе; она часто осложняется образованием на поверхности анода малорастворимых осадков, гидроксидов и солей металлов.
Увеличение анодной поляризации металла увеличивает скорость его растворения и сопровождается увеличением концентрации катионов в приэлектродном слое. Когда скорость диффузии меньше скорости ионизации металла, нарастает прианодная концентрация соли, вплоть до пересыщения раствора и ее кристаллизации на поверхности анода. Если слой выделяющейся соли сплошной, то анод оказывается изолированным от электролита, что сопровождается резким возрастанием омического сопротивления участка цепи "анод-электролит", уменьшением плотности тока и прекращением растворения металла.
При этом смещение потенциала анода в положительную сторону может быть настолько значительным, что оказывается возможным окисление отдельных анионов электролита и нейтральных молекул растворителя. Механизм ионизации анода зависит от величины приложенного потенциала. Поскольку в анодном процессе могут принимать участие молекулы растворителя, а окисление металла возможно до различной степени окисления, металл может ионизироваться в активном, пассивном и транспассивном состояниях.
Скорость анодного растворения металла в активном (незапассивированном) состоянии определяется уравнением
= iо exp [βF∆E / (R - T)], (9)
где iо - ток обмена; β - число переноса; F - постоянная Фарадея; ∆Е - перенапряжение; R - универсальная газовая постоянная; Т - температура, и зависит от ионного состава раствора, его рН, присутствия комплексов, состояния поверхности растворяющегося металла, наличия на ней ингибирующих соединений.
Если в отдельных стадиях процесса анионы определяют скорость ионизации, то концентрацию анионов учитывают в кинетическом уравнении. Например, ионизация никеля в сульфатных растворах происходит по схеме:
+ ОН- = Ni (ОН)-адс, (10)+ (ОН)-адс - е = Ni (ОН)адс, (11)(ОН) адс + НSO4
- е = NiSO4 + Н2О, (12)
где реакция (12) является лимитирующей стадией, и в этом случае уравнение скорости ионизации включает концентрационную компоненту
= К · [ОН-] · [НSO4-] - ехр [βF∆Е/(R - T)] (13)
В общем случае анодное растворение металла включает те же основные стадии, что и его катодное восстановление, но протекающие в обратном порядке. При этом образование многозарядных ионов включает несколько последовательных одноэлектронных электрохимических промежуточных реакций, каждая из которых протекает со все большим перенапряжением по сравнению с предыдущей.
Ионизация металла происходит в определенном порядке: в первую очередь в
реакции участвуют группы атомов с повышенной свободной энергией (активные
центры), которые составляют незначительную часть поверхностного слоя анода
(10-1 … 10-5%). Процесс протекает тем быстрее, чем больше активных центров
имеет поверхность анода и чем больше дефектов в его кристаллической решетке.
.1.2 Пассивное состояние металлов
Поверхность металла является пассивной (инертной), если она не
подвергается воздействию среды, хотя при данных условиях металл
термодинамически нестабилен. Наступление пассивности сопровождается
самопроизвольным возрастанием поляризации на аноде при одновременном уменьшении
прохождения тока через электрическую цепь. В пассивном состоянии металлы
проявляют иные физико-химические свойства, чем в активном: пассивное железо не
вытесняет медь из раствора ее солей; пассивный ром растворяется с образованием
ионов ![]() (активный - с образованием ионов
Cr3+) и т.д.
(активный - с образованием ионов
Cr3+) и т.д.
Пассивирование металлов обусловлено появлением на их поверхности химически связанного кислорода. Механизм пассивации имеет пленочную природу, в соответствии с которой торможение анодного растворения металла обусловлено образованием на поверхности металлов солевых, оксидных и гидроксидных твердофазных пленок. Такие пленки часто появляются при потенциалах анода, соответствующих электроду второго рода; они малорастворимы и термодинамически устойчивы. По морфологический свойствам различают пленки:
) рыхлые, пористые, с незначительным электрическим сопротивлением. Они появляются в результате кристаллизации малорастворимого осадка и достигают значительной толщины (до 1 мм), например галогениды меди, серебра; сульфаты свинца, никеля, железа; оксиды кадмия, цинка и др;
2) сплошные, плотные, беспористые, с большим электрическим сопротивлением (106 Ом/см2); их толщина составляет около10-4 см. После их возникновения (например, на алюминии, тантале и др.) ионизация анода резко затрудняется либо прекращается.
Пассивирующий оксид является либо продуктом электрохимической реакции:
Ме + mН2О - 2mе = МеnОm + 2mH+, (14)
либо продуктом химического взаимодействия металла с окислителем. Подобные пленки защищают металл от дальнейшего глубокого окисления. Иногда в пассивном состоянии, благодаря повышению анодного потенциала, развиваются другие анодные процессы - выделение кислорода, перезарядка ионов и т.д. - аналогично тому, как они протекают на полностью нерастворимых (например, платиновых) анодах. Это обусловлено способностью тонких пленок оксидов многих металлов проявлять электронную проводимость. Критерии образования защитной пленки:
) объем оксида должен быть не меньше объема металла, пошедшего на его образование;
2) пленка должна быть однородной и иметь высокую адгезию к металлу.
Потенциал анода, выше которого на нем начинается образование оксидного
слоя и переход в пассивное состояние, называют "критическим"
потенциалом (потенциал максимума поляризационной кривой - рис. 1).
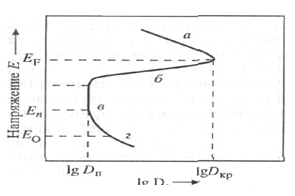
Рисунок 1 - Анодная поляризационная кривая, характеризующая переход металла в пассивное состояние
а - активная область; б - область перехода от активного состояния к
пассивному: в - область пассивации; г - область анодного выделения кислорода Е
F - критический потенциал; Ео - потенциал выделения кислорода