Материал: Диссертация Маленьких В.С(ПРО МОЛЬНОЕ СООТНОШЕНИЕ)

2. РАЗРАБОТКА МАТЕМАТИЧЕСКОЙ МОДЕЛИ УСТАНОВКИ ИЗОМЕРИЗАЦИИ ДЛЯ РАСЧЕТА ТЕХНОЛОГИЧЕСКИХ ПРОЦЕССОВ И ПАРАМЕТРОВ ЕЕ РАБОТЫ
2.1. Постановка задачи рационализации энергоемкого процесса изомеризации
В современной нефтеперерабатывающей промышленности есть не-
сколько различных типов изомеризации бензиновых фракций. Они отли-
чаются друг от друга условиями проведения технологического режима и свойствами применяемых катализаторов. Из-за постоянного роста стоимо-
сти энергоресурсов наиболее популярной является низкотемпературная изомеризация, для которой применяются специальные катализаторы [3].
На установке изомеризации для процесса изомеризации применяется катализатор СИ-2, который по своим характеристикам превосходит суще-
ствующие аналоги. Все существующие катализаторы изомеризации делятся на три типа: высокотемпературные, среднетемпературные и низкотемпера-
турные [46]. Их отличие друг от друга по степени конверсии н-пентанов и н-гексанов «за проход» и по устойчивости к каталитическим ядам. В табли-
це 3 приведено сравнение различных типов катализаторов изомеризации.
Таблица 3 – Сравнение различных типов катализаторов изомеризации
Наименование |
Хлорированные |
СИ-2 |
Аналоги СИ-2 |
|
катализаторы |
|
|
|
|
|
|
Изомеризация: |
65–75 |
70–-75 |
68–72 |
C5( iC5/∑C5),% масс. |
|
|
|
|
|
|
|
Изомеризация: |
24–28 |
28–34 |
20–27 |
С6(2,2-ДМБ)/С6, % масс. |
|
|
|
Допустимое содержание в |
|
|
|
сырье, ррm: |
|
|
|
– S |
<0,5 |
1–5 |
1 |
–N |
<0,1 |
1–2 |
1 |
– Н20 |
<100 |
<20 |
10–20 |
|
|
|
|
41
Окончание табл. 3
Наименование |
Хлорированные |
СИ-2 |
Аналоги СИ-2 |
|
|
катализаторы |
|
|
|
|
|
|
|
|
Октановое число |
|
|
|
|
(ИОЧ), пункты: |
|
|
|
|
– за проход |
81–83 |
84–85 |
80–82 |
|
– рецикл н-С5 |
83–84 |
86–87 |
85–86 |
|
– рецикл С6 |
85–87 |
88–89 |
87–88 |
|
– рецикл Н-С5 и |
89–91 |
91–93 |
90–91 |
|
Н-С6 |
||||
|
|
|
Важно отметить, что при увеличении октанового числа возрастают затраты на циркуляцию невступившего в реакцию сырья. Нужно понимать,
что блок предварительного извлечения из сырья i-C5 окупит себя при со-
держании более 20 % изопентана [26; 36;41]. Применяемые в нефтеперера-
ботке схемы процессов изомеризации показаны на рисунке 4.
В данной работе рассматривается схема установки с предварительным извлечением изопентана и рециклом n-пентана и n-гексана, так как она явля-
ется самой сложной и самой затратной с точки зрения энергоэффективности.
Цель моделирования установки изомеризации заключается в создании виртуальной модели схемы реального процесса для определения основных технологических параметров процесса и определения путей его совершен-
ствования.
42
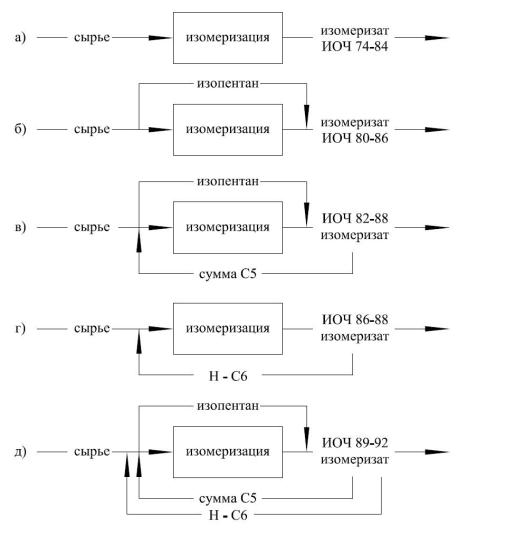
Рисунок 4 – Схемы процессов изомеризации легких бензиновых фракций:
а – схема «за проход»; б – схема с предварительным извлечением изопентана; в – схема с предварительным извлечением изопентана и рециркуляцией нормального пентана; г – схема с рециркуляцией нормального гексана; д – схема с предварительным извлечением изопентана, рециркуляцией нормального пентана и нормального гексана.
2.2. Моделирование термодинамических и физических свойств углеводородов
Моделирование процессов изомеризации решается в системе нели-
нейных одновременно решаемых уравнений. Она включает расчет термоди-
намических параметров всех необходимых потоков, составов и расходов с применением выбранных моделей расчета процессов и свойств.
Каждый элемент системы рассчитывается с помощью наиболее эф-
фективного алгоритма именно для этого элемента. Последовательность рас-
43
чета элементов системы определяется автоматически. «При наличии рецик-
лов создается схема итераций, в которой рецикловые потоки разрываются, и
создается последовательность сходящихся оценочных значений. Эти значе-
ния получаются замещением величин, рассчитанных при предыдущем про-
счете схемы (метод простого замещения) или путем применения специаль-
ных методов ускорения расчета рециклов – Вегштейна и Бройдена» [73].
В условиях, когда неизвестны многие свойства веществ, одним из наиболее эффективных способов расчета термодинамических свойств ве-
ществ в широком диапазоне варьирования параметров (давления, расхода,
температуры) может оказаться уравнение Пенга–Робинсона [45]. Его досто-
инством является то, что оно одно из наиболее точных в области, близкой к критической точке, а также в простоте, так как для его определения требует-
ся всего 2 дополнительных параметра в уравнении (2.1.) а и b.
= |
|
− |
|
, |
(2.1) |
|
− |
(+)+( − ) |
|||||
|
|
|
|
где Р – давление (МПа),
Т – температура (°С),
V – молярный объем (м3/кмоль),
R = 0,0083144 МПа·м3/кмоль·К (кДж/(моль·К)) – универсальная газовая по-
стоянная.
Коэффициенты уравнения (2.1) для чистых веществ определялись из того условия, что на зависимости Р=Р(V) на критической изотерме критиче-
ская точка является точкой перегиба [1; 64].
|
|
2 2 |
|
|
||
= 0,45724 |
|
|
, |
(2.2) |
||
|
||||||
|
|
|
|
|||
|
|
|
|
|
||
|
|
|
|
|||
= 0,0778 |
|
|
, |
|
(2.3) |
|
|
|
|
||||
|
|
|
|
|
||
|
|
|
|
|
||
44 |
|
|
|
|
|
|
= 0,37464 + 1,54724 − 0,26992 2, |
(2.4) |
||
|
|
||
= [1 + (1 − √ |
|
)]2. |
(2.5) |
|
|
|
|
где Тс, Рс – температура и давление в критической точке,
Tr = 0,7· Тс, – ацентрический фактор вещества, являющийся по определе-
нию Питцера мерой отклонения свойств межмолекулярного взаимодействия исследуемого вещества от свойств веществ со сферическими молекулами
(Ar, Kr, Xe, для которых = 0) и может быть определен по формуле Эдми-
стера:
= |
3 |
( |
|
) − 1, |
(2.6) |
|
|
||||
7 |
|
− |
|
|
|
|
|
|
|||
где Tb – нормальная температура кипения при давлении 1 атм (К),
Рс измеряется в атмосферах.
Коэффициент сжимаемости для всего поля термодинамического со-
стояния может быть определен из решения уравнения 3 степени.
3 − (1 − ) 2 + ( − 3 2 − 2 ) − ( − 2 − 3) = 0, |
(2.7) |
||||||
где коэффициенты А и В определяются по формулам: |
|
||||||
А = |
|
, |
|
(2.8) |
|||
2 2 |
|||||||
= |
|
. |
|
(2.9) |
|||
|
|
||||||
|
|
|
|
||||
Коэффициент сжимаемости входит в уравнение состояния реального |
|||||||
газа вещества: |
|
||||||
= |
|
. |
(2.10) |
||||
|
|||||||
|
|
|
|
|
|||
45 |
|
|
|
|
|
||