Материал: Черешнев ВА, Шилов, Черешнева. Экспериментальные модели в патологии
методов трансплантации β-клеток островков Лангерганса у разных видов экспериментальных животных.
Одной из первых моделей, не связанных с хирургическим вмешательством, является аллоксановый диабет. Аллоксан (2,4,5,6 тетраоксипиримидин; 5,6-диоксиурацил) впервые описан Бругнателли
(Brugnatelli) в 1818 г. Вёхлер (Wöhler) и Лиебиг (Liebig) предложили название «аллоксан» при описании его химического синтеза окислени ем мочевой кислоты. Диабетогенное действие этого соединения было открыто много лет спустя (Dunn J.S., Sheehan H.L., McLethie N.G.B., 1943). Было установлено, что введение аллоксана кроликам приводит к развитию специфического некроза островков поджелудочной желе зы. С тех пор экспериментальная модель аллоксанового диабета стала широко использоваться для изучения патогенеза сахарного диабета 1 го типа.
Другой моделью является сахарный диабет, индуцируемый у крыс или мышей введением стрептозотоцина. Стрептозотоцин (2 деокси-2-(3-метил-3-нитрозоуреидо)-D-глюкопираноза) синтезируется Streptomycetes achromogenes и используется в медицине как химиоте рапевтический препарат для лечения злокачественных опухолей под желудочной железы, развивающихся из β-клеток островков Лангер ганса. В дозе 65 мг/кг массы тела у крыс и 190 мг/кг массы тела у мы шей при однократном внутрибрюшинном введении приводит к разви тию у 100% животных тяжелого диабета 1-го типа, связанного с пря мым повреждением β-клеток островков Лангерганса поджелудочной железы. По нашим данным, у крыс диабет протекает более тяжело, чем у мышей, и без введения инсулина приводит к 100% летальности крыс уже через 72 ч после инъекции стрептозотоцина в вышеуказан ной дозе вследствие развития гипергликемии и гиперкетонемии (Ши лов Ю.И. и др., 2013). Уровень глюкозы уже через 24 ч после введения стрептозотоцина крысам в среднем повышается с 5,50±0,15 в контроле до 27,88±2,54 ммоль/л (средняя арифметическая±стандартная ошибка средней; у отдельных животных он увеличивается в этот срок до 52 ммоль/л). Летальность у мышей при введении значительно более вы сокой дозы стрептозотоцина (190 мг/кг) в течение первых 10 суток эксперимента, по нашим данным, составляет 47,9% без введения инсу лина. Средняя концентрация глюкозы на 10-е сутки эксперимента у мышей с сахарным диабетом, по нашим данным, составляет 20,33±0,75, а в контроле – 3,98±0,29 ммоль/л. В течение первых трех суток после введения стрептозотоцина как у крыс, так и у мышей час то развивается выраженная гипогликемия (вплоть до гипогликемиче ской комы и смерти) вследствие массивного выброса эндогенного ин
300
сулина при повреждении β-клеток островков Лангерганса и их дегра нуляции. Для предупреждения развития летальной гипогликемии ре комендуется поить животных в течение этого срока 10% раствором глюкозы вместо воды. Хотя в литературе описаны экспериментальные модели с введением более низких доз стрептозотоцина, наш опыт по казывает, что действие этого антибиотика подчиняется закономерно сти «все или ничего», и при использовании более низких доз препара та даже в сочетании с обогащенной жирами диетой диабет не развива ется при наблюдении за животными в течение нескольких месяцев.
Как стрептозотоцин, так и аллоксан проникают в β-клетки островков Лангерганса через транспортер глюкозы GLUT2 и разру шают их через образование активных форм кислорода и свободных радикалов.
Описаны экспериментальные модели аутоиммунного диабета у инбредных линий крыс с аллелями MHC II класса RT1 B/Du, опреде ляющих генетическую предрасположенность к диабету, при введении им кополимера полиинозиновой и полицитидиловой кислот (поли ИЦ), усиливающего продукцию интерферона-α (IFN-α). Показано, что повышение продукции IFN-α при вирусных инфекциях может способ ствовать развитию аутоиммунных реакций против β-клеток и у людей
сопределенными гаплотипами HLA.
2.Экспериментальные модели спонтанного сахарного диабе-
та у животных. NOD-мыши (англ. nonobese diabetic mice – нетучные диабетические мыши) – одна из наиболее широко исследуемых в на
стоящее время экспериментальных моделей естественно развивающе гося сахарного диабета. Впервые эти животные были получены груп пой S. Makino с соавт. (1980) при скрещивании одной из двух подли ний CTS-мышей, характеризовавшейся развитием полиурии и глюко зурии. У полученных путем направленного скрещивания NOD-мышей симптомы сахарного диабета проявлялись в виде полиурии, полидип сии, гипергликемии, глюкозурии и гиперхолестеринемии. Патоморфо логически развивалась выраженная лимфоцитарная инфильтрация ост ровков Лангерганса, снижение их количества и размера. Подобно са харному диабету типа 1A у человека, при котором для развития ауто иммунного повреждения β-клеток важную роль играет генетическая предрасположенность, связанная с определенными гаплотипами HLA I и II классов, NOD-мыши имеют мутации, связанные с отсутствием молекул, кодируемых локусом I-E комплекса Н-2 (аналог HLA-DR у человека), или с необычной структурой молекул, кодируемых локусом I-A главного комплекса гистосовместимости (аналог HLA-DQ у чело века). Поскольку продукты этих локусов, являясь молекулами гисто
301
совместимости II класса (MHC II класса), участвуют в презентации «чужих» антигенных пептидов Т-хелперам, именно они определяют возможность развития аутоиммунных реакций. Показано, что замеще ние отсутствующего I-E локуса I-E трансгеном предупреждает разви тие сахарного диабета. Сходные результаты получены при замещении дефектного I-A локуса трансгенным I-A геном с другой последова тельностью нуклеотидов. Помимо MHC II класса более чем 15 других генетических локусов участвуют в развитии заболевания, поэтому предрасположенность NOD-мышей к развитию сахарного диабета яв ляется полигеномной.
Развитие сахарного диабета у NOD-мышей связано с развити ем инсулита, который впервые выявляется у них в возрасте 4–5 не дель. К 7-месячному возрасту сахарный диабет развивается примерно
у90% самок и только у 60% самцов. Характерна мононуклеарная ин фильтрация островков Лангерганса, которая связана с аутоиммунной атакой их клеток и которая в конечном итоге приводит к полному раз рушению островков. Инфильтрат содержит Т-лимфоциты, макрофаги, NK-клетки, В-лимфоциты. Развитие аутоиммунных реакций у NOD мышей может быть связано и с дефектами регуляторных Т лимфоцитов, что характерно и для сахарного диабета 1-го типа у чело века. В связи с этим NOD-мыши являются удобным объектом для раз работки новых подходов предупреждения аутоиммунных реакций при диабете 1-го типа. Доказано участие аутоиммунного компонента и в патогенезе повреждения β-клеток в поздние сроки развития стрептозо тоцинового и аллоксанового диабета.
Вотличие от NOD-мышей, предрасположенность которых к развитию сахарного диабета носит полигенный характер, у некоторых линий крыс она является олигогенной. Сахарный диабет, спонтанно развивающийся у крыс BB (от англ. biobreeding rats; впервые получе ны в 1974 г. в Bio Breeding Laboratory), также является моделью са харного диабета типа 1A человека. Крысы BB имеют аутосомную ре циссивную мутацию, которая приводит к развитию выраженной Т лимфопении. Олигогенной является и предрасположенность к диабету
укрыс линии LETL (англ. Long-Evans Tokushima Lean rats), которые подобно крысам BB имеют аллели RT1 B/Du (аллель MHC II класса) с мутацией гена Cbl-b, приводящей к нарушениям проведения Т
клеточных внутриклеточных сигналов.
Одной из подлиний крыс LETL является линия KDP. Сахар ный диабет у крыс KDP развивается в 3–4-месячном возрасте, частота развития заболевания – 70–80% как у самок, так и у самцов. Для этих крыс нехарактерно развитие лимфопении, они имеют общий с крыса
302
ми BB гаплотип молекул главного комплекса гистосовместимости II класса RT1 B/Du. При патоморфологическом исследовании через 120– 220 дней жизни у них выявляется развитие инсулита, а также лимфо цитарная инфильтрация щитовидной железы и почек. Помимо этого у крыс KDP экспрессируется не связанный с главным комплексом гис тосовместимости ген, названный Cblb (англ. casitas B-lineage lym phoma b) и кодирующий убиквитиновую лигазу, которая важна для костимуляции через CD28 активации Т-лимфоцитов. Однако связи аналогов этого гена с сахарным диабетом у человека не выявлено. Сходство частоты развития сахарного диабета у самцов и самок крыс KDP с заболеванием человека указывает на высокую перспективность этой относительно недавно найденной модели для изучения патогенеза сахарного диабета 1-го типа человека.
В 2004 г. выведена новая линия крыс (Lenzen S. et al., 2004) из конгенной линии LEW.1AR1 через спонтанную мутацию, которая обо значена как линия LEW.1AR1/Ztm-iddm. У всех крыс этой линии экс прессируется аллель MHC II класса RT1 B/Du, для них не характерно развитие лимфопении, но развивается повреждение островков Лангер ганса, сходное с аналогичным повреждением у крыс BB и KDP. Са харный диабет 1-го типа развивается у них в возрасте 2–3 месяцев, характеризуется низким уровнем инсулина, гипергликемией, глюкозу рией и кетонурией. Частота развития заболевания около 70% и у са мок, и у самцов. Характерна низкая летальность без терапии инсули ном. Для этих крыс не характерно увеличение аутоантител к глутамат декарбоксилазе и к тирозиновой фосфатазе ICA512 (обозначаемой также как IA-2). Иммуноциты, инфильтрирующие поджелудочную железу, не атакуют щитовидную железу и другие железы.
Сахарный диабет 2-го типа
Главным звеном патогенеза сахарного диабета 2-го типа явля ется нарушение ответа клеток тканей организма на инсулин (инсули норезистентность) как следствие изменения структуры или уменьше ния количества специфических рецепторов для инсулина, изменения структуры самого инсулина или нарушения внутриклеточных меха низмов передачи сигнала с рецепторов инсулина (рис. 35). Нарушение адекватного ответа на нормальные уровни инсулина мышечной и жи ровой ткани, печени приводит к развитию гипергликемии (мобилиза ция глюкозы печенью за счет активации гликогенолиза и глюконеоге неза; нарушение утилизации глюкозы в дихотомическом и апотомиче ском путях, реакциях гликогеногенеза и биосинтетических путях ли пидного обмена), увеличению уровня НЭЖК (активация липолиза в
303
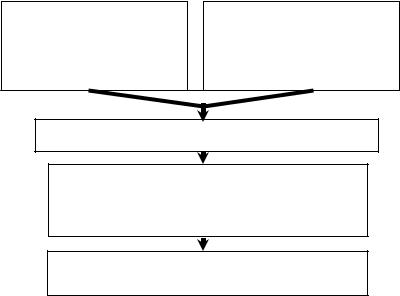
Генетическая |
|
Факторы окружающей среды |
||
предрасположенность |
+ |
и образа современной жизни |
||
Ожирение, дислипопротеидемии, |
Гиподинамия; избыточное, |
|||
мутации генов K |
АТФ |
-каналов |
несбалансированное |
|
β-клеток, глюкокиназы, |
|
и нерегулярное питание; |
||
митохондриальной ДНК и др. |
|
хронический стресс и др. |
||
Инсулинорезистентность
Повышение продукции инсулина Избыточная активация β-клеток
Снижение числа β-клеток, нарушение толерантности к глюкозе, гипергликемия, активация мобилизации липидов, начальные проявления глюкотоксичности
Значительное уменьшение числа β-клеток, выраженные проявления глюкотоксичности с нарастанием гипергликемии и развитием осложнений
Рис. 35. Патогенез сахарного диабета 2-го типа
жировой ткани). Указанные изменения во многом реализуются через повышение продукции контринсулярных гормонов, и их можно рас сматривать как защитно-приспособительные. Вследствие нарушения утилизации глюкозы β-клетками продукция инсулина повышается. В конечном итоге развиваются нарушения функций β-клеток (вначале с отсутствием изменения их количества, а в последующем с его сниже нием). Итак, основными особенностями сахарного диабета 2-го типа являются инсулинорезистентность, гиперинсулинемия, дисфункция β клеток, в то время как уровни инсулина и гликемический контроль варьируют в зависимости от стадии заболевания и способности гипе ринсулинемии компенсировать высокий уровень глюкозы.
Заболевание чаще развивается после достижения 40-летнего возраста, однако в последние годы отмечается увеличение частоты развития сахарного диабета 2-го типа в более молодом возрасте и даже у подростков вследствие повышения частоты ожирения. Сахарный диабет 2-го типа тесно связан с другими метаболическими наруше ниями, в том числе с ожирением, артериальной гипертензией, дисли попротеидемиями, при этом заболевании более быстро и тяжело раз
304