Материал: Черешнев ВА, Шилов, Черешнева. Экспериментальные модели в патологии
ховым(R. Virchow) более100 летназад.
Большинство исследователей, описывавших клеточную эмигра цию еще до открытия молекул клеточной адгезии, отмечали факт значи тельного повышения адгезивных свойств клетокэндотелия, мембранылей коцитов и тромбоцитов. Ю. Конгейм еще в 1882 г. в своих лекциях по об щейпатологиивысказалмнение, что повышение адгезивных свойствэндо телиясвязаносмолекулярнымиизменениями. Характерныиморфологиче скиеизмененияэндотелиямикрососудов, которыенастадиипристеночного стояниялейкоцитовприобретаютвид«булыжноймостовой».
При воспалительной эмиграции лейкоцит должен преодолеть две преграды: эндотелий и базальную мембрану. Слой эндотелия лейкоциты проходят, протискиваясь между эндотелиальными клетками, а базальную мембрану временно растворяют своими протеиназами. Весь процесс пере ходалейкоцитачерезстенкусосудазанимаетот 2 до 12 мининевызывает повреждения стенки сосуда. Главным местом эмиграции лейкоцитов явля ютсяпосткапиллярныевенулы. Приостромвоспалениипреждевсегоэмиг рируют нейтрофилы и значительно позднее – моноциты. Эозинофилы, ба зофилыилимфоцитытакжеспособныкэмиграции. Эмиграциялейкоцитов связанаспоявлениемвочагевоспаленияспециальныхмедиаторов– хемат трактантов. Экзогенными хематтарактантами являются N формилметиониловые пептиды, синтезирующиеся только прокариотами. К наиболее сильным эндогенным хематтрактантам относятся фрагменты ак тивируемого при воспалении комплемента, особенно C5а, лейкотриен В4, факторактивациитромбоцитовикалликреин, атакжеспециализированные на регуляции хемотаксиса лейкоцитов несколько десятков низкомолеку лярных пептидных цитокинов – хемокинов, которые по структуреразделе ны на семейства – -, -, - и -хемокинов. Эмиграция лейкоцитов в очаг воспаленияначинаетсясихадгезиикэндотелиюсосудовмикроциркуляторно го русла. Адгезивность увеличивается в результате повышения экспрессии на мембране эндотелиальных клеток молекул клеточной адгезии (рис. 11). Про хождениелейкоцитовчерезсосудистуюстенку– эторезультатприсущейэтим клеткам способности к движению – локомоции, которая активируется хемат трактантами. Активация через рецепторы к хемоаттрактантам, а также интег риныидругиемолекулыклеточнойадгезииреализуетсячерезцелыйрядвнут риклеточных сигнальных путей, что приводит к реорганизации компонентов клеточного цитоскелета и сократительных белков клетки. Важную роль игра ют полимеризация низкомолекулярного G-актина в F-актин, сшивка нитей микрофиламентов актиногелином (MARCKS) – белком, перекрестно связы вающим актин, в результате чего F-актин переходит в состояние геля. Интег рины и актиновые филаменты взаимодействуют через различные адапторные белки, такиекакталин, которыйзапускаетполимеризациюактинауплазмати-
85
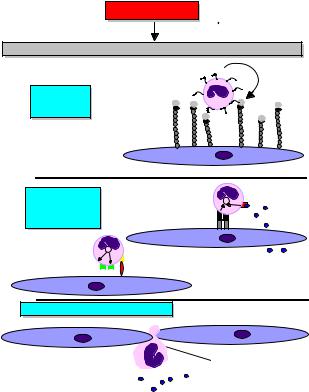
ПОВРЕЖДЕНИЕ
Выброс медиаторов воспаления (цитокины, гистамин, тромбин и др.)
Перекатывание CD15 CD162
Захват, пере- |
|
катывание, |
|
заякоривание |
CD62P |
|
|
|
CD62E |
|
эндотелий |
Активация, рас- |
+ |
пластывание, |
|
прочное прикреп- |
контактная CD62L |
ление |
активация CD31 |
Активация экспрессии +
интегринов  VLA-4
VLA-4
LFA-1/CR3
ICAM -1
 VCAM -1
VCAM -1
хемокины и
 другие хемо-
другие хемо- 
 аттрактанты
аттрактанты
Выход лейкоцита за пределы сосуда
Взаимодействие ICAM -1 и LFA-1 играет ключевую роль. Лейкоциты выходят между соединениями эндотелиальных клеток, где имеет место повышенная экспрессия кадхеринов (в частности, CD144) и CD31. Затем посредством гидролаз они пенетрируют базальную мембрану сосуда и выходят в ткани.
хемокины и другие хемоаттрактанты
Хемотаксис, фагоцитоз, дыхательный  взрыв, экзоцитоз, продукция медиаторов воспаления, ферментов, катионных белков, цитокинов, факторов реорганизации тканей и др.
взрыв, экзоцитоз, продукция медиаторов воспаления, ферментов, катионных белков, цитокинов, факторов реорганизации тканей и др.
Рис. 11. Участиемолекулклеточнойадгезиивклеточнойэмиграциипривоспалении
ческоймембраны. Взаимодействиехематтрактантовсповерхностнымирецеп торамилейкоцитовсопровождаетсяактивациейразличныхнаходящихсявних ферментов, в том числе фосфолипаз А2 и С; локальным гидролизом фосфатидилинозитол-4,5-дифосфата с образованием инозитолтрифос фата и диацилглицерола; увеличением уровня внутриклеточного каль ция; повышением активности протеинкиназы C. В контроле полимери зации актина ведущую роль играют Rho ГТФ-азы, к которым относят ся более чем десять различных ферментов, запускающих различные пути перестройки цитоскелета. В частности, одна из ГТФ-аз этого се
86
мейства – RAC – способна вызывать конформационные изменения
WASP (англ. Wiskott-Aldrich syndrome protein) – белка синдрома Вис котта-Олдрича, контролирующего состояние актина и дефектного при вышеуказанном синдроме. Под действием хемоаттрактантов происхо дит поляризация клеточного цитоскелета, в результате которой моле кулы клеточной адгезии, взаимодействующие с соответствующими лигандами на мембране эндотелия, собираются в виде кластеров на полюсе клетки, контактирующем со стенкой венулы. Выбрасывается содержимое гранул, в том числе протеиназы, способные растворять базальную мембрану сосудов.
Наибольшей функциональной активностью обладают нейтро фильные лейкоциты. Первыми в очаг воспаления приходят полиморф ноядерные лейкоциты, их называют клетками «аварийного реагирова ния» и одноразового пользования.
Моноциты находятся в крови до 3 суток, затем уходят в ткани и находятся в них около 10 дней. Часть их дифференцируется в осед лые тканевые макрофаги, часть находится в неактивном состоянии и может вновь активироваться. Поэтому моноциты называют клетками многоразового пользования. Такая последовательность выхода фор менных элементов крови за пределы сосуда была выявлена И.И. Меч никовым и называется «закон клеточной эмиграции».
Согласно этому закону клеточные реакции при воспалении протекают в три стадии:
1)полинуклеарная (эмиграция нейтрофилов и эозинофилов) –
до 2 суток;
2)мононуклеарная (эмиграция моноцитов и лимфоцитов) – до
5–6 суток;
3)фибробластическая (пролиферация фибробластов и других местных соединительно-тканных клеточных элементов в очаге воспа ления).
Как установлено в последние годы, последовательность эмиг рации определяется динамикой экспрессии на разных типах лейкоци тов различных молекул клеточной адгезии, а также временным пат терном появления их лигандов на эндотелии. Однако в большей степе ни она обусловлена временными параметрами синтеза специализиро ванных цитокинов хемотаксиса – хемокинов.
Выделяют четыре семейства хемокинов – -, -, - и хемокины. Хемокины отличаются более высокой избирательностью действия на отдельные типы лейкоцитов. Установлено, что хемокины (CXC-хемокины)– это хемоаттрактанты преимущественно для нейтрофилов и некоторых лимфоцитов, а -хемокины (CC
87
хемокины)– преимущественно для моноцитов, эозинофилов, базофи лов, Т- и В-лимфоцитов, NK-клеток. Семейство -хемокинов включа ет в себя 17 цитокинов, а -хемокинов – 27 белков; -хемокины (C хемокины) представлены только двумя белками – лимфотактином-α и лимфотактином-β, являющимися избирательными хемоатрактантами для Т-лимфоцитов и NK-клеток. Из -хемокинов (CX3C-хемокины) наиболее изучен фракталкин, синтезирующийся эндотелиальными клетками и привлекающий в очаг воспаления моноциты, NK-клетки и Т-лимфоциты. Среди отдельных хемокинов есть цитокины как с узко направленным, так и с широким спектром активности в отношении различных клеток-мишеней. Как установлено в последние годы, изби рательность действия отдельных хемокинов на разные типы лейкоци тов во многом связана с гетерогенностью рецепторов. К настоящему времени описано 11 типов рецепторов для -хемокинов (CCR1, CCR2, CCR3, CCR4, CCR5, CCR6, CCR7, CCR8, CCR9, CCR10, CCR11), 7 типов для -хемокинов (CXCR1, CXCR2, CXCR3, CXCR4, CXCR5, CXCR6, CXCR7), отдельные типы рецепторов для - (XCR1) и хемокинов (CX3CR1). Некоторые рецепторы хемокинов (D6, CCR11, Duffy) способны связывать лиганды, но не проводят сигнал внутрь клетки, поэтому они рассматриваются как своеобразные ловушки для хемокинов, препятствующие их действию. Таким образом, большое разнообразие синтезируемых в очаге воспаления хемокинов и рецеп торов к ним, неодинаково экспрессирующихся на разных типах лейко цитов, создает условия для узконаправленной регуляции подвижности и активности фагоцитирующих клеток и лимфоцитов.
Важнейшей функцией лейкоцитов в очаге воспаления является фагоцитоз – захват, убийство и переваривание микроорганизмов, а также переваривание продуктов распада тканей и клеток собственного организма.
Входе фагоцитоза различают 4 стадии:
1)стадия приближения фагоцита к объекту;
2)стадия прилипания (адгезии) фагоцита к объекту;
3)стадия поглощения фагоцитом объекта;
4)стадия внутриклеточных превращений поглощен
ного объекта.
Первая стадия обусловлена способностью фагоцитов к хемо таксису. В механизмах распознавания и адгезии фагоцитом объекта (вторая стадия) большую роль играют опсонины – антитела, фрагмен ты комплемента, фибронектин. Значительное усиление фагоцитоза этими молекулами определяется высокоспецифическим связыванием
88
соответствующих комплексов с мембраной фагоцита через соответст вующие рецепторы (рецепторы к Fc-фрагменту иммуноглобулинов, рецепторы к белкам системы комплемента, рецепторы 1-, 2-, 3 семейств интегринов). Помимо этого возможно и первичное распозна вание патогенных агентов через многочисленные паттерн распознающие рецепторы, к которым относятся интенсивно изучае мые Toll-подобные рецепторы (TLR1-TLR13), рецепторы «мусорщи ки» (англ. scavenger receptors – SR-A и MARCO), макрофагальный маннозный рецептор, -глюкановый рецептор и др. (R. Medzitov, С. Janeway, 2000; R. Metzitov, 2003, 2008). Собственно в фагоцитозе и эндоцитозе наибольшая роль принадлежит 3 последним группам ре цепторов. Лигандами паттерн-распознающих рецепторов являются молекулярные структуры, общие для многих патогенных микроорга низмов (патоген-ассоциированные молекулярные паттерны по терми нологии, предложенной Русланом Метжитовым и Чарльзом Джаневэ ем, англ. pathogen-associated molecular patterns – PAMP), а также моле кулы, связанные с повреждением собственных клеток (англ. damageassociated molecular patterns – DAMP). Активация внуриклеточных сигнальных путей через Toll-подобные рецепторы приводит к увели чению экспрессии генов, кодирующих синтез провоспалительных ци токинов, индуцибельной NO-синтазы, антимикробных пептидов, мо лекул главного комплекса гистосовместимости и костимулирующих молекул CD80 и CD86, необходимых для презентации антигенных пептидов Т-лимфоцитам.
Механизм стадии поглощения объекта связан с активной пе рестройкой компонентов клеточного цитоскелета и сократительных белков клетки. Захват осуществляется путем постепенного обволаки вания фагоцитом микробной клетки, т.е. путем прогрессирующего прилипания поверхности фагоцита к поверхности микроба до тех пор, пока весь объект не будет «обклеен» мембраной фагоцита. Вследствие этого поглощаемый объект оказывается внутри фагоцита, заключен ным в мешок, образованный частью мембраны фагоцитирующей клет ки. Этот «мешок» называется фагосомой. Образование фагосомы на чинает стадию внутриклеточных превращений поглощенного объекта внутри фагосомы, т.е. вне внутренней среды фагоцита.
Основная часть внутриклеточных превращений поглощенного при фагоцитозе объекта связана с переходом содержимого цитоплаз матических гранул фагоцитов внутрь фагосомы. В этих гранулах у всех облигатных фагоцитов содержится большое количество биологи чески активных веществ – преимущественно ферментов, которые уби вают и затем переваривают микробы и другие поглощенные объекты.
89