Материал: Боженко Основы квантовой химии

py = −i |
1 |
(Y1,1 − Y1,−1 ) = −i |
1 |
|
1 |
3 |
|
sinθ |
|
|
2 |
2 |
2 |
2π |
|
||||||
|
|
|
|
|
||||||
|
|
|
|
|
1 |
3 |
|
|
|
|
[cosϕ + i sinϕ − cosϕ + i sinϕ ] = 2 |
|
|
|
|
(II.108) |
|||||
|
π sinθ sinϕ |
|||||||||
|
|
|||||||||
Так же можно перейти от комплексных угловых функций для n=2 - Y2,0 , Y2,±1 , Y2,±2 к действительным АО,
обозначаемым как dxy , dxz , dyz , dx2 − y2 , dz2 , соответственно.
Теперь вспомним, что атомные орбитали получаются в результате перемножения угловой и радиальной частей. И выпишем несколько нормированных волновых функций водородоподобного атома:
n l m
1 0 0
2 0 0
2 1 0
2 1 ±1
|
|
|
|
1 |
|
|
|
|
Z |
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
ψ 1s = |
|
|
|
|
|
|
|
|
|
|
e− ρ |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
π |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
a0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
1 |
|
|
|
|
Z |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
− |
ρ |
|
||||||||||||
ψ 2s |
= |
|
|
|
|
|
2 |
(2 − ρ ) e |
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
||||||||||||||||||||||
|
|
|
2π |
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
4 |
|
|
|
|
|
a0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
1 |
|
|
|
|
|
|
Z |
|
2 |
|
|
|
|
|
− |
ρ |
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
ψ 2 pz |
= |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ρ |
e |
|
2 cosθ |
||||||||||||||||||
|
4 |
|
|
2π |
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
a0 |
|
|
|
|
|
|
|
|
|
|
|
|
ρ |
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
Z |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
− |
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|||||||||||||||||
ψ |
2 px |
= |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ρ e |
|
|
|
|
sinθ cosϕ |
|||||||||||
4 |
|
2π |
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
a0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
Z |
|
2 |
|
|
|
|
|
− |
ρ |
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
ψ 2 py |
= |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ρ e |
|
|
2 sinθ sinϕ |
|||||||||||||||
4 |
|
|
2π |
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
a |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0 |
|
|
|
|
|
|
|
|
|
|
|
(II.109) |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
76 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
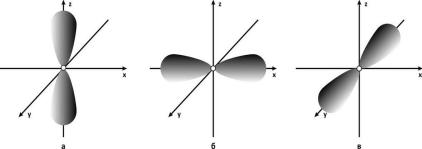
Рис.6. Электронные облака p – орбиталей:
а– 2pz-АО, б – 2px-АО, в – 2py-АО
Вхимических приложениях часто используют графическое изображение волновых функций, причем, как правило, отдельно изображаются радиальная и угловая части. Выделяют только ту часть, которая зависит только от угловых переменных θ и ϕ . Она имеет смысл полного вы-
ражения для АО, в котором условно принимают, что АО является произведением некоторой радиальной функции и определенной функции, зависящей от углов θ и ϕ . Напри-
мер, для 2pz атомной орбитали эта функция имеет следующий вид: ψ 2 pz = f (r) | cosθ | . Ее в учебниках химии изобра-
жают в виде гантели, вытянутой вдоль оси Оz, как это показано на Рис. 6а. На Рис.6б и в показаны 2px и 2py атомные орбитали.
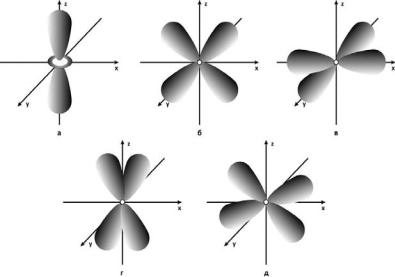
На Рис. 7 приведено схематическое изображение d- АО, точнее их угловых частей. АО с главным квантовым числом 3 называются f – орбиталями. Они выглядят еще сложнее и изображать их графически достаточно трудно.
Здесь необходимо сделать одно важное замечание – широко используемые в химии атомные орбитали: s, p, d и т.д. являются, прежде всего, решениями стационарного уравнения Шредингера для атома водорода и водородоподобных атомов. И, наверное, благодаря тому, что атомы в значительной мере
77
сохраняют свои свойства при образовании молекул, атомные орбитали явились очень плодотворной математической моделью, имеющей глубокое физическое значение при описании физико-химических свойств множества молекул. Не стоит забывать также и то, что, изображенные на Рис. 6 и 7 электронные облака, прежде всего, означают вероятность распределения в пространстве электронной плотности.
Рис.7. Электронные облака d-орбиталей:
а– 3dz2− AO ; б– 3dxz − AO ; в– 3dx2 − y2 − AO ;
г– 3dyz − AO ; д– 3dxy − AO
Принцип Паули
Хорошо известная из курса химии формулировка принципа Паули говорит о том, что в данном атоме или молекуле не может быть двух электронов с четырьмя одинако-
78
выми квантовыми числами. Рассмотрим другую формулировку этого знаменитого принципа, используя некоторые положения квантовой механики. Пусть pˆ jk – оператор переста-
новки k-го и j-го электронов, то есть в результате действия такого оператора данные два электрона меняются местами. Так как электроны неразличимы, то
|
|
|
|
|
p j,k |
H |
= H p j,k |
(II.110) |
|
Поскольку |
pˆ jk |
коммутирует с гамильтонианом, то |
pˆ jk соот- |
|
ветствует постоянной движения и pˆ jk и гамильтониан имеют
общие собственные функции. Введем краткое обозначение
ψ (1,2,...... j,...., k,.....n) ≡ ψ ( j, k) .
Тогда
pˆ j,k ψ ( j, k) = λ ψ ( j, k) = ψ (k, j) , |
(II.111) |
где λ – действительное число, поскольку оператор pˆ jk – эр-
митов. Подействуем оператором перестановки два раза подряд на волновую функцию ψ ( j, k) :
|
|
|
|
|
p j,k ( p j ,k ψ ( j, k )) = p j,k |
(λ ψ ( j, k )) |
= |
||
|
|
|
|
|
λ p j,k ψ ( j, k ) = λ 2 |
ψ ( j, k ) = ψ ( j, k ) |
(II.112) |
||
λ 2 |
= 1 λ = ±1 |
|
|
|
То есть при перестановке двух одинаковых частиц решение стационарного уравнения Шредингера может либо изменять знак, либо нет. Состояния, при которых ψ меняет,
знак называются антисимметричными. Согласно принципу Паули волновые функции систем, состоящих из электронов, являются антисимметричными. В этом и заключается его смысл в квантовой механике.
79

III. КВАНТОВАЯ ХИМИЯ
Приближение Борна-Оппенгеймера
Суть приближения Борна-Оппенгеймера заключается в разделении движения электронов и ядер. Это легко понять, воспользовавшись простыми рассуждениями с точки зрения классической физики. Очевидно, имея намного меньшую массу по сравнению с массой ядер, электроны в молекуле более подвижны по сравнению с ядрами, то есть их движения совершаются в поле практически неподвижных ядер.3 За время заметного смещения ядра электрон успевает много раз пройти вокруг него. Именно такая классическая модель позволяет рассматривать движение ядер и электронов в отдельности. Поскольку приближение Борна-Оппенгеймера является квантово-механическим, его нужно обосновать на языке квантовой механики. Для этого вводится параметр малости или малый параметр
|
m |
1 |
|
|
4 |
|
|||
κ = |
|
|
|
(III.1) |
|
|
|||
|
M |
|
|
|
m – масса электрона, а M – масса ядра.
По этому параметру малости проводится разложение в ряд гамильтониана и волновой функции. Обозначим совокупность координат ядра α через ξα , а смещение ядра пред-
ставим в виде произведения параметра κ и координат ядра
α : ξα = κξα
ˆ ˆ |
ˆ |
2 |
ˆ |
+ |
(III.2) |
Тогда H = H0 |
+ κ H1 |
+ κ |
H2 |
3 Большая часть раздела «Квантовая химия» соответствует [5 и 6]. 80