Материал: Белозеров В.И., Яркин А.Н., Кузина Ю.А. Сборник задач по курсу Техническая термодинамика
6.5. Определить приращение энтропии 3 кг воздуха а) при нагревании его по изобаре от 0 до 400ºC; б) при нагревании его по изохоре от 0 до 880ºC; в) при изотермическом расширении с увеличением объема в 16 раз. Теплоемкость считать постоянной.
6.6. Средняя теплоемкость алюминия сp в интервале температур от 0 до 300ºC равна 0,955 кДж/(кг·К). Определить энтропию 100 кг алюминия при 300ºC, считая, что его энтропия при 0ºC равна нулю.
6.7. 1 кг воздуха сжимается по политропе от 1 бар и 20ºC до 8 бар при n=1,2. Определить конечную температуру, изменение энтропии, количество отведенного тепла и затраченную работу.
6.8. В процессе политропного расширения воздуха температура его уменьшилась от t1=25ºC до t2= –37ºC. Начальное давление воздуха P1=4 бар, количество его m=2 кг. Определить изменение энтропии в этом процессе и конечное давление воздуха, если известно, что количество подведенного к воздуху тепла составляет 89,2 кДж.
6.9. 30 л воды с температурой 90ºC смешиваются с 20 л воды с температурой 15ºC. Определить вызванное этим процессом изменение энтропии. Теплоемкость воды принять равной 4,187 кДж/(кг·К). Считать, что тепловые потери отсутствуют.
6.10. Стальной шар массой 10 кг при 500ºC погружается в сосуд с 18 кг воды, температура которой равна 15ºC. Определить изменение энтропии системы в этом процессе. Считать, что тепловые потери отсутствуют. Теплоемкость принять равной 0,5129 кДж/(кг·К), теплоемкость воды 4,187 кДж/(кг·К).
6.11. Определить энтропию 1 кг газовой смеси, состоящей из азота и аргона, при P1=0,3 МПа и t1=300ºC. Массовые доли азота и аргона: gN2=0,37, gAr=0,63. Газы считать идеальными; принять, что при P0=0,1 МПа и t0=0ºC энтропии азота и аргона равны нулю.
6.12. Определить, насколько увеличится энтропия при смешении 3 кг азота и 2 кг углекислого газа. Газы считать идеальными. Температура и давление газов до смешения одинаковы.
6.13. Определить эксергию воздуха в баллоне. Давление воздуха в баллоне 15 МПА, температура равна температуре среды. Параметры окружающей среды (воздуха): P0=0,1 МПа, t0=15ºC. Объем баллона 40 дм3. Воздух считать идеальным газом.
6.14. Определить эксергию воздуха в баллоне. Известны давление и температура воздуха: P=13 МПа, t=200ºC. Параметры окружающей среды: P0=0,1 МПа, t0=20ºC. Объем баллона 25 дм3. Воздух считать идеальным газом.
6.15. Определить эксергию азота, находящегося в пьезометре экспериментальной установки при P=25 МПа, t=200ºC. Параметры среды: P0=0,1 МПа, t0=20ºC. Объем пьезометра 500 см3. Азот считать идеальным газом.
6.16. Определить эксергию 100 кДж теплоты при температуре 700ºC. Температура среды 0ºC. Определить потерю эксергии этой теплоты, если последняя будет передана тепловому источнику с температурой 500ºC.
6.17. Определить эксергию количества теплоты, которое получается в результате сгорания на воздухе 1 кг топлива с теплотой сгорания Qиp=25,0 МДж/кг; температура горения 1500ºC; температура окружающей среды t0=20ºC; теплоемкость продуктов сгорания принять постоянной.
6.18. Для некоторых горячих источников температура газа, выходящего из земли, доходит до 180ºC (давление атмосферное). Определить эксергию 1 кг газа. Температура среды t0=20ºC. Считать, что газ по своим термодинамическим свойствам является идеальным и идентичен углекислому газу. Определить максимальный термический к.п.д., который имел бы тепловой двигатель, превращающий теплоту этого источника в работу.
6.19. Определить эксергию 1 кг выходящего из подземных источников водяного пара. Температура пара равна 100ºC, давление атмосферное. Температура окружающей среды 10ºC. Принять, что теплота парообразования r=2257 кДж/кг, а теплоемкость воды сp=4,187 кДж/(кг·К).
6.20. В сосуде объемом 300 л заключен воздух при давлении P1=50 бар и температуре t=20ºC. Параметры среды: P0=1 бар, t0=20ºC. Определить максимальную полезную работу, которую может произвести сжатый воздух, находящийся в сосуде.
6.21. В сосуде объемом 200 л находится углекислота при температуре t1=20ºC и давлении P1=100 бар. Температура среды t0=20ºC, давление среды P0=1 бар. Определить максимальную полезную работу, которую может произвести находящаяся в сосуде углекислота.
6.22. Торпеда приводится в действие и управляется автоматически, двигаясь на заданной глубине. Для двигателя торпеды используется имеющийся в ней запас сжатого воздуха. Определить максимальную полезную работу, которую может произвести воздушный двигатель торпеды, если объем сжатого воздуха в ней V1=170 л, давление P1=180 бар, а температура воздуха и морской воды t0=10ºC. Торпеда отрегулирована на движение под уровнем моря на глубине 4 м. Определить также силу, с которой торпеда устремляется вперед, если радиус ее действия должен быть равен 4 км, а потерями можно пренебречь.
6.23. Определить максимальную полезную работу, которая может быть произведена 1 кг кислорода, если его начальное состояние характеризуется параметрами t1=400ºC и P1=1 бар, а состояние среды – параметрами t0=20ºC, P0=1 бар. Представить процесс в диаграммах P-v, T-s.
6.24. В сосуде объемом 400 л заключен воздух при давлении P1=1 бар и температуре t1= –400C. Параметры среды: t0=20ºC, P0=1 бар. Определить максимальную полезную работу, которую может произвести воздух, заключенный в сосуд. Представить процесс в диаграммах P-v, T-s.
7. Вода и водяной пар. Равновесная парожидкостная смесь
1. Основным для анализа обратимых термодинамических процессов является уравнение объединенных первого и второго законов (начал) термодинамики в одной из форм (Tds=dq)
dh=Tds+vdP, (7.1)
du=Tds–Pdv. (7.2)
Дополнительно необходимо знать уравнение состояния рабочего вещества (тела), т.е. зависимость, например, вида F(P, v, T)=0. В общем случае, исключая область, где вещество ведет себя как идеальный газ, аналитические выражения для уравнения состояния отсутствуют. Связь между параметрами состояния задается в виде таблиц термодинамических свойств вещества и построенных на их основе P-v-, T-s-, h-s- диаграмм состояния. Это результаты экспериментальных исследований, и для воды они представлены наиболее полно.
2. Качественно P-v-диаграмма имеет вид, представленный на рис. 7.1.
3. Область правее линии FG – область твердого состояния вещества. Для воды, ввиду ее практической несжимаемости, линия FG почти совпадает с изотермой T = 273,15 К = 0ºC.
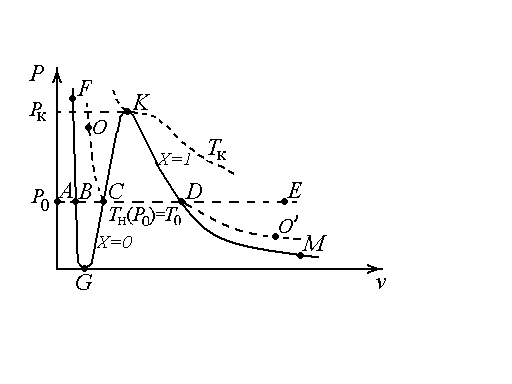
Рис. 7.1. (P, v)-диаграмма состояния вещества:
FGKM – линия фазовых переходов; линия равновесных (насыщенных) состояний вещества;
FG – линия фазового перехода «твердое тело – жидкость»;
GK – линия фазового перехода «жидкость – газ (пар)»; линия начала кипения; нижняя пограничная кривая; линия насыщения жидкости;
KM – линия фазового перехода «пар – жидкость»; линия начала конденсации; верхняя пограничная кривая; линия насыщения пара; сухой насыщенный пар;
точка G – «тройная точка». Для воды это P = 610,8 Па; T = 273,16 К = = 0,01ºC; v = 0,001 м3/кг
Область выше линии FGK – жидкое состояние вещества. Область правее линии KM – газообразное (пар) состояние. В этих областях однофазного состояния термодинамические параметры определяются по соответствующим таблицам или диаграммам состояния. Достаточно задания двух любых параметров состояния (P, v, u, s, h, T).
Замечание 1. При построении таблиц и диаграмм термодинамического состояния воды условно полагается, что u=h=s=0 в тройной точке воды. Поэтому на P-v-диаграмме, например, линия FG совпадает с осью ординат, которая смещается в точку G (рис. 7.1). Значение, например, hк в критической точке при этом принимает конкретное значение 2095,2 кДж/(кг·К).
4. Область двухфазных состояний расположена ниже кривой GKM. В этой области жидкая и паровая фазы смеси находятся в термодинамически равновесном (насыщенном) состоянии.
Каждому давлению насыщения P=Pн<Pк соответствует строго определенная для каждого простого вещества температура насыщения (Tн), причем зависимость Tн от Pн взаимно однозначная. Соответственно, в двухфазной области равновесных состояний изобара P=P0 совпадает с изотермой T=T0=Tн (P0). (На рис. 7.1 изобара ABCDE (P=P0) и изотерма OCDO (T=T0=Tн (P0)) имеют общий отрезок CD).
Значения термодинамических параметров состояния (v, u, h, s) каждой из фаз смеси однозначно определяются заданием только давления или температуры T= Tн (P) смеси. В любой точке изобары-изотермы CD их значения для каждой из фаз одни и те же и равны их значениям на пограничных кривых: на нижней (точка С на GK для P=P0) для жидкости и на верхней (точка D на KM) для пара. Эти значения находят либо по таблицам свойств жидкости и пара на линии насыщения, либо по таблицам свойств жидкости или пара, где они имеют предельные для каждой фазы значения, либо по соответствующим диаграммам состояний. Параметры жидкости на линии насыщения (нижняя пограничная кривая) будем обозначать одним штрихом вверху (a), а параметры пара на линии насыщения (верхняя пограничная кривая) – двумя штрихами вверху (a).
Замечание 2. Задание любого из параметров a или a позволяет по таблицам определить Tн и Pн.
Степень сухости (массовое паросодержание). На изобаре-изотерме термодинамическое состояние каждой из фаз фиксированно и определяется однозначно заданием одного (любого) параметра состояния на линии насыщения (нижней или верхней). Состояние cмеси в точках изобары-изотермы отличаются только массой жидкой (Mж) и паровой (Mп) фаз смеси при сохранении общей ее массы M=Mж+ Mп. С подводом энергии жидкость равновесно переходит в пар, с отводом энергии пар переходит в жидкость.
В силу аддитивности (экстенсивности) объема, внутренней энергии, энтальпии и энтропии для любой из удельных массовых величин смеси (v, u, h, s) имеет место равенство
M·a=Mп·a+ Mж·a, M=Mж+ Mп,
где a – это v, u, h или s.
Отсюда
a=Хa+(1–Х)a=a+(a–a)Х, (7.3)
где Х= Mп/M – степень сухости или массовое паросодержание смеси – основной термодинамический параметр парожидкостной смеси в равновесном состоянии.
Из (7.3) следует, что
![]() . (7.4)
. (7.4)
Поскольку задание значения одного из термодинамических параметров a, a, Tн или Pн определяет значения всех a, a, то дополнительное задание X или, что то же самое, в силу (7.4) значения одного из термодинамических параметров смеси a полностью определяет все термодинамические параметры парожидкостной смеси (v, u, h, s, P, T).
Из уравнений (7.4) и рис. 7.1 следует:
1) на линии X=X(P)=0 Mп=0 и a= a; это жидкость на линии насыщения – нижняя пограничная кривая GK;
2) на линии X=X(P)=1 Mж=0 и a= a; это пар на линии насыщения в отсутствие жидкой фазы (сухой насыщенный пар) – верхняя пограничная кривая KM;
3) все линии 0<X(P)<1 так же, как X=0 и X=1, сходятся в точке K и, не пересекаясь, образуют сетку в двухфазной области. Парожидкостную смесь в этой области называют влажным насыщенным паром. Наличие такой сетки линий X=const на T-s-, h-s-диаграммах позволяет существенно упростить расчеты термодинамических процессов.
Уравнения (7.1), (7.2) на изобаре-изотерме, где P0= Pн=const, T0 = Tн(P0)=const, имеют вид dh= Tнds, du= Tнds– Pнdv. Отсюда следует ряд полезных формул:
h–h=Tн (s–s)=r(Pн), u–u= r – Pн (v–v),
где r – удельная теплота парообразования (Дж/кг), необходимая для перевода 1 кг вещества из состояния «жидкость на линии насыщения» в состояние «сухой насыщенный пар».
h= h+rX;
s= s+(r/Tн )X;
s= s+ r/Tн ;
X=(s– s) Tн /r;
X=( h–h)/r.
(Tн – в кельвинах!)
Замечание 3. Значения X, определяемые по формулам (7.4), являются степенью сухости Mп/M только при 0X1. Если X<0, это значит только, что вещество в жидком состоянии (недогретая до кипения жидкость). Если X>1 – вещество в газообразном состоянии (пар), причем его температура выше температуры насыщения (сухой перегретый пар).