Материал: Біологічна та біоорганічна хімія_Мардашко О.О._ изд. 2008-342 с._ОНМедУ-2012
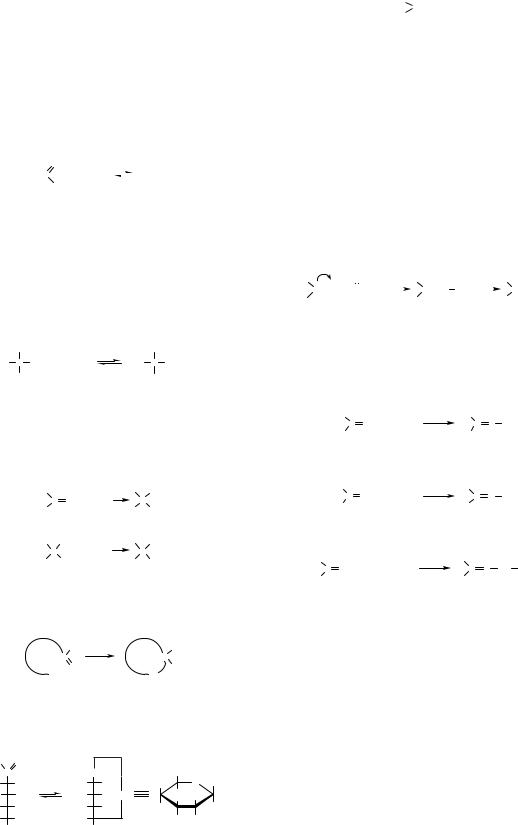
на атомі Карбону, мають високий вміст гідрат- |
4. Взаємодія з амінами. Взаємодія оксосполук із |
||||||||||||||||||||||||||
них форм у водних розчинах. Наприклад, три- |
первинними амінами перебігє за механізмом при- |
||||||||||||||||||||||||||
хлорацетальдегід (хлораль) утворює дуже стійку |
єднання–відщеплення. На першій стадії реакції |
||||||||||||||||||||||||||
гідратну форму — хлоральгідрат, відщепити |
відбувається нуклеофільне приєднання аміну по |
||||||||||||||||||||||||||
воду від якого можна тільки при дії концентро- |
подвійному зв’язку |
С=О карбонільної групи. |
|||||||||||||||||||||||||
ваної сульфатної кислоти. |
Аміни є сильними нуклеофілами, у цьому випад- |
||||||||||||||||||||||||||
3. Взаємодія зі спиртами. Спирти, як і вода, |
ку немає необхідності активувати електрофіль- |
||||||||||||||||||||||||||
оборотно приєднуються до оксосполук, переваж- |
ний центр оксосполук. Первинним продуктом |
||||||||||||||||||||||||||
но альдегідів, з утворенням напівацеталей. У |
приєднання є біполярний іон, що стабілізується |
||||||||||||||||||||||||||
спиртових розчинах альдегідів напівацеталі пе- |
в результаті внутрішньомолекулярного переносу |
||||||||||||||||||||||||||
ребувають у рівновазі з карбонільними сполука- |
протона від атома Нітрогену до атома Оксиге- |
||||||||||||||||||||||||||
ми. Так, в етанольному розчині ацетальдегіду |
ну, перетворюючись на аміноспирт. Однак реак- |
||||||||||||||||||||||||||
утримується близько 30 % напівацеталю (у роз- |
ція не зупиняється на цій стадії. Вже підкреслю- |
||||||||||||||||||||||||||
рахунку на альдегід). |
|
|
|
|
|
|
|
|
|
валося, що сполуки, які містять дві електроноак- |
|||||||||||||||||
|
|
O |
|
|
|
|
|
OC2H5 |
цепторні групи при одному атомі Карбону, |
||||||||||||||||||
|
|
|
|
|
|
|
нестійкі, вони прагнуть до стабілізації шляхом |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
CH3 |
|
C + C2H5OH |
|
|
|
CH3 |
|
C |
|
OH |
|||||||||||||||||
|
|
|
|
|
|
відщеплення однієї з груп у вигляді нейтральної |
|||||||||||||||||||||
|
|
|
|
||||||||||||||||||||||||
|
|
H |
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
H |
||||||||||||||||||||
|
|
|
|
|
|
|
|
термодинамічно стабільної молекули. У цьому |
|||||||||||||||||||
Ацетальдегід |
1-Етоксіетанол |
||||||||||||||||||||||||||
випадку відбувається відщеплення молекули |
|||||||||||||||||||||||||||
|
|
|
(напівацеталь) |
||||||||||||||||||||||||
|
|
|
води від молекули аміноспирту (друга стадія ре- |
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
При взаємодії з другою молекулою спирту в |
акції — елімінування) і утворюється амін (осно- |
||||||||||||||||||||||||||
умовах кислотного каталізу напівацеталі пере- |
ва Шиффа). |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
творюються на ацеталі. Багато які з кетонів у цю |
δ |
+ |
δ - |
|
AN |
|
|
|
|
E |
|
|
|
|
|
||||||||||||
реакцію не вступають, їхні ацеталі одержують |
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
C |
|
O |
+ NH2R |
|
C |
|
NH R |
-H O |
C |
|
N |
|
R |
||||||||||||||
іншими методами. Напівацеталі зазвичай не ви- |
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
||||||||||||
|
|
|
|
|
OH |
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
діляють через їхню нестійкість: |
|
|
|
Амін |
|
|
|
|
|
Основа Шиффа |
|||||||||||||||||
|
OC2H5 |
|
|
|
|
|
OC2H5 |
|
|
АN |
— нуклеофільне приєднання |
||||
|
|
|
Н+ |
|
|
|
|
Е — відщеплення (елімінування) |
|||||||
CH C OH + C H OH |
CH |
3 |
C OC H |
5 |
+ H O |
|
|
|
|
||||||
|
3 |
|
2 |
5 |
|
|
2 |
2 |
|
|
|
|
|||
|
H |
|
|
|
|
|
|
H |
|
|
|
Реакції нуклеофільного |
|||
1-Етоксіетанол |
|
|
|
1,1-Діетоксіетан |
приєднання–відщеплення |
||||||||||
(напівацеталь) |
|
|
|
|
(ацеталь) |
|
R |
|
|
R |
|||||
|
|
|
|
|
|
|
|
|
|
|
O + NH2OH |
|
|||
|
|
|
|
|
|
|
|
|
|
|
C |
-H2O |
C N OH |
||
Таким чином, загальна схема утворення на- |
R' |
|
R' |
||||||||||||
Гідроксил- |
|||||||||||||||
півацеталей і ацеталей з відкритим ланцюгом |
|
Оксим |
|||||||||||||
|
амін |
|
|
||||||||||||
така: |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
OH |
|
|
R |
|
|
R |
|
|
|
|
|
|
|
|
C |
|
|
C |
O + NH2NH2 |
|
C N NH2 |
||
|
|
C |
O + ROH |
|
|
|
|
-H2O |
|||||||
|
|
|
|
|
|
|
|
OR |
|
|
R' |
|
|
R' |
|
|
|
|
|
|
|
|
|
|
|
|
Гідразин |
|
Гідразон |
||
|
|
|
|
|
напівацеталь |
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
OH |
|
|
|
OR |
|
|
|
|
|
|
||
|
|
C |
|
+ ROH |
|
C |
|
|
|
R |
|
|
R |
||
|
|
|
OR |
|
|
|
OR |
|
|
|
|
||||
|
|
|
|
|
|
|
|
C O + NH2NHC6H5 |
|
C N NH C6H5 |
|||||
|
|
|
|
|
|
|
|
|
|
|
-H O |
||||
|
|
|
|
|
|
ацеталь |
|
|
R' |
|
2 |
R' |
|||
|
|
|
|
|
|
|
|
|
|
||||||
Утворення циклічних напівацеталей: |
Фенілгідразин |
Фенілгідразон |
|||||||||||||
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
Альдегід R′ = H |
|
|
||
|
|
|
|
H |
|
|
|
H |
|
|
Кетон R′ ≠ H |
|
|
||
|
|
|
C |
|
|
|
|
C |
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
OH |
|
|
Подібно взаємодії з первинними амінами пе- |
||||
|
|
OH |
|
|
|
|
O |
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
ребігають реакції оксосполук із такими похідни- |
||||
Прикладом утворення циклічних напівацета- |
ми аміаку, як гідроксиламін NH2OH, гідразин |
||||||||||||||
лей є молекула глюкози (формула Коллі — То- |
H2N–NH2, фенілгідразин C6H5NHNH2 та інші |
||||||||||||||
похідні оксосполуки, що утворюються, — окси- |
|||||||||||||||
ленса і Хеуорса). |
|
|
|
|
|
|
|
|
ми, гідразони, фенілгідразони; зазвичай це стійкі |
||||||
|
|
|
|
|
|
|
|
|
|
|
|||||
H |
O |
|
|
H |
OH |
|
|
|
|
|
кристалічні речовини з чіткими температурами |
||||
|
C |
|
|
Н–С–ОН |
|
CH OH |
плавлення, використовуються для ідентифікації |
||||||||
H |
OH |
|
|
C |
OH |
|
|
2 |
|
||||||
|
|
H |
|
|
|
O |
вихідних оксосполук. |
|
|
||||||
HO |
H |
|
|
HO |
H |
O |
|
OH |
|
|
|
|
|||
|
|
|
|
OH |
5. Відновлення оксосполук. Альдегіди віднов- |
||||||||||
H |
OH |
|
|
H |
OH |
|
|
OH |
|
||||||
H |
OH |
|
|
H |
|
|
|
|
OH |
люються в первинні спирти, а кетони — у вто- |
|||||
|
CH2OH |
|
|
CH2OH |
|
|
|
|
ринні. Одним з ефективних відновників оксоспо- |
||||||
|
|
|
|
|
|
|
|
|
|
|
|||||
D-глюкоза |
D-глюкопіраноза |
D-глюкопіраноза |
лук є алюмогідрид літію LiAIH4. Він є постачаль- |
||||||||||||
(формула |
|
(формула |
|
(формула |
ником гідридіонів Н-, які є нуклеофільними час- |
||||||||||
Фішера) |
Коллі — Толенса) |
Хеуорса) |
тинками і приєднуються по подвійному зв’язку |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
24 |
|
|
|
|

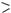 С=О. Для перетворення спочатку утворюється алкоксидіон із спирту, після закінчення відновлення в реакційну суміш додають воду.
С=О. Для перетворення спочатку утворюється алкоксидіон із спирту, після закінчення відновлення в реакційну суміш додають воду.
Альдольна конденсація
Реакції альдольно-кротонової конденсації пере-
бігають з альдегідами та кетонами, у яких атом Карбону, безпосередньо зв’язаний з карбонільною групою, має хоча б один атом Гідрогену. Для розуміння механізму реакції необхідно розглянути вплив карбонільної групи на аліфатичний радикал. Електроноакцепторна карбонільна група викликає поляризацію зв’язків із сусідніми атомами, зокрема зв’язку С-Н в α -атомі Карбону. Атом Гідрогену стає рухливим, виникає СН-кислотний центр. За рахунок цього кислотного центру оксосполука може під дією сильних основ відщепити протон і перетворитися на карбаніон. Негативний заряд у карбаніоні, що утворився, делокалізований за участю альдегідної або кетонної групи:
|
|
|
|
|
|
δ - |
|
|
|
|
|
O |
|
|
|
|
|
δ + O |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|||
R |
|
CH |
|
|
C |
|
R CH |
|
|
|
C + H+ |
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|||||||
|
|
|
|
2 |
|
|||||||
|
|
|
|
|
|
H |
|
|
|
|
|
H |
|
|
H |
|
|
||||||||
Альдегід Карбаніон
Аніон — це сильний нуклеофіл, він реагує з другою молекулою карбонільної сполуки за механізмом нуклеофільного приєднання з утворенням альдолю (альдоль: альд — альдегід; -ол — спирт):
|
|
|
|
O |
|
|
|
|
|
O |
|
|
|
|
|
|
|
O |
O |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
R |
|
CH2 |
|
C + R CH |
|
C |
|
|
|
|
|
R CH2 |
CH CH C + |
|||||||||
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
H |
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
R |
H |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Альдегід |
Карбаніон |
|
|
|
|
Алкоксидіон |
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
O |
|
|||
|
|
|
|
+ H2O |
|
|
|
|
R |
|
CH2 |
|
|
|
|
|
|
CH C |
|
|||
|
|
|
|
|
|
|
|
|
|
|
CH |
|
|
|
H |
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Альдоль
В умовах організму здійснюється альдольна конденсація, наприклад, оксалоацетату (щавлевооцтової кислоти) та ацетилкоензиму А в циклі Кребса, що приводить до утворення цитрату (лимонної кислоти).
COOH |
|
|
|
Цитрат |
|
|
COOH |
|
|
||||||||||
|
|
CHOH |
|
|
O |
синтаза |
|
|
|
|
|
|
|
||||||
|
|
|
CH |
|
|
||||||||||||||
|
|
2 |
+ CH |
|
C |
|
|
|
|
|
|
|
2 |
|
O + HSKoA |
||||
C |
|
O |
3 |
|
|
SKoA |
HO |
|
C |
|
CH2 |
|
C |
||||||
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H КоензимА |
COOH |
|
|
|
|
|
|
|
|
COOH |
||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||
Оксалоацетат Ацетил-КоА Цитрат
OH |
O |
|
|
OH |
|
|
|
OH |
H |
||
O P CH2 |
|
CH2 |
P O |
|
|
CH2 |
O P O |
C O |
|||
|
|
|
|
||||||||
OH |
|
OH |
OH |
|
|
|
C O |
OH + H C OH OH |
|||
|
|
|
|||||||||
|
|
|
|
||||||||
|
|
|
|
OH |
|
|
|
|
CH2 |
OH |
CH2 O P O |
|
|
|
|
|
|
|
|
|
|||
OH |
|
|
|
|
|
|
|
|
|
OH |
|
Фруктозо- |
|
|
Діоксіацетон- |
Гліцеральде- |
|||||||
1,6-бісфосфат |
|
|
|
|
фосфат |
гід3-фосфат |
|||||
Окиснення альдегідів і кетонів. Якісні реакції на виявлення альдегідної групи
Альдегіди і кетони по-різному реагують на дію окисників. Альдегіди легко (значно легше, ніж спирти) окиснюються у відповідні карбонові кислоти. Для їхнього окиснення можна використовувати такі м’які окисники, як оксид срібла та гідроксид міді (ІІ).
Кетони до дії цих окисників інертні. Не окиснюються вони й киснем повітря. Тільки під дією більш сильних окисників кетони вдається окиснити. При цьому відбувається розрив вуглецьвуглецевих зв’язків у вихідній молекулі й утворюється суміш різних продуктів окиснення (кислот і кетонів) з меншою кількістю атомів Карбону, ніж у молекулі вихідного кетону.
Однією з якісних реакцій для виявлення альдегідної групи є реакція «срібного дзеркала» — окиснення альдегіду оксидом срібла. Оксид срібла завжди готують безпосередньо перед дослідом, додаючи до розчину нітрату срібла розчин гідроксиду лужного металу.
AgNO3 + KOH → |
KNO3 + AgOH |
|
2AgOH |
→ |
Ag2O + H2O |
2Ag2O + NH3 |
→ |
[Ag(NH3)2]+OH- |
У розчині аміаку оксид срібла утворює комплексну сполуку — гідроксид діамінсрібла, відому також під назвою реактиву Толенса. Під дією гідроксиду діамінсрібла на альдегід відбувається окисно-відновна реакція. Альдегід окиснюється у відповідну кислоту, а катіон срібла відновлюється в металеве срібло, що дає блискучий наліт на стінках пробірки — «срібне дзеркало».
|
|
O |
|
+OH- |
|
|
|
O |
CH3 |
|
C + |
Ag(NH3)2 |
|
CH3 |
|
C + 2Ag + 4NH3 + 2H2O |
|
|
|
|
||||||
|
|
H |
|
|
|
|
|
OH |
Ацетальдегід |
|
Оцтова кислота |
||||||
Інша якісна реакція на альдегіди полягає в окисненні їх гідроксидом міді (II) (реактив Фелінга). При окисненні альдегіду гідроксид міді (ІІ),
Урослинних клітинах здійснюється біосинтез що має світло-блакитний колір, відновлюється в фруктози за механізмом альдольної конденсації. гідроксид міді (І) жовтого кольору. Цей процес
Упроцесі гліколізу спостерігається альдольне перебігає при кімнатній температурі. Якщо
розщеплення фруктозо-1,6-бісфосфату на дві фосфотріози: гліцеральдегід3-фосфат і діоксіацетонфосфат у присутності альдолази:
підігріти випробуваний розчин, то гідроксид міді (І) жовтого кольору перетворюється на оксид міді (І) червоного кольору.
25

O |
|
O |
CH3 C + 2Cu(OH)2 |
|
CH3 C + |
|
||
H |
|
OH |
Оцеталь- |
Гідроксид |
Оцтова |
|||||
дегід |
міді (ІІ) |
кислота |
|||||
+ H2O + 2CuOH |
|
|
|
CuO |
|
+ H2O |
|
|
|
||||||
|
|
|
|
||||
|
Гідроксид |
Оксид |
|||||
|
міді (І) |
міді (І) |
|||||
Аналітичні реакції для виявлення наявності глюкози в біологічних рідинах використовують здатність глюкози відновлювати в лужному середовищі при нагріванні оксиди срібла та міді. З цією метою застосовують:
1.Реактив Фелінга — іон Cu2+, стабілізований тартратаніоном.
2.Реактив Толенса — аміачний розчин Ag2О.
3.Реактив Троммера — Cu(ОН)2.
Реакція диспропорціонування (дисмутації)
З альдегідами, які не мають α -водневого атома (наприклад, формальдегід, бензальдегід, фурфурол) і тому не здатні зазнавати альдольного ущільнення, під дією лугу відбувається інше перетворення — окисно-відновне диспропорціонування до відповідних спирту та карбонової кислоти (у вигляді солі).
|
CH O |
|
COOK |
CH2OH |
2 |
KOH |
+ |
|
|
|
|
|
||
|
Бенз- |
Бензоат |
Бензиловий |
|
альдегід |
|
калію |
спирт |
|
Реакцію вперше спостерігав Канніццаро (1853). Для альдегідів, які мають α -водневий атом, аналогічний процес здійснив В. Є. Тищенко (1906) під дією алкоголяту алюмінію. У результаті утворюється не суміш спирту з кислотою, а продукт їхньої взаємодії — складний ефір:
CH3 |
|
|
|
AI(OR) |
|
|
|
|
|
|
CH3 |
2 |
C |
|
O |
3 |
CH3 |
|
CH2 |
|
O |
|
C |
|
|
|
|
|
|||||||
H |
|
|
|
|
|
|
|
|
|
|
O |
Етиловий ефір оцтової кислоти
Це перетворення названо реакцією Канніццаро — Тищенко, або складноефірною конденсацією. Воно є наслідком того, що альдегіди за ступенем окиснення займають проміжне положення між спиртами і кислотами, з якими їх пов’язують окисно-відновні переходи, які відіграють важливу роль у процесах метаболізму органічних сполук.
Галоформні реакції
Тригалогенопохідні метану СННаl3 (хлороформ, йодоформ і бромоформ), які мають загальну назву галоформи, одержують дією вільних галогенів на етанол у лужному середовищі. Розглянемо цю реакцію на прикладі одержання йодоформу, оскільки вона застосовується у фарма-
цевтичній практиці для визначення наявності етанолу (йодоформна проба).
CH3 CH2OH + I2 + KOH → |
CHI3 |
+ HCOOK |
Етанол |
Йодо- |
Форміат |
|
форм |
калію |
Реакція перебігає в кілька стадій. Йодноватиста кислота НОІ, що утворюється при розчиненні йоду в лузі, перебуває в рівновазі зі своєю калієвою сіллю КОІ.
I2 + KOH → KI + HOI
Йодноватиста
кислота
HOI + KOH 
 KOI + H2O
KOI + H2O
Гіпойодит
калію
Солі йодноватистої кислоти (гіпойодити) є сильними окисниками і окиснюють етанол в ацетальдегід.
O
CH3CH2OH + KOI |
|
CH3 |
|
C + H2O + KI |
|
|
H
Етанол Ацетальдегід
У молекулі ацетальдегіду атоми Гідрогену метильної групи стають більш реакційноздатними, ніж у молекулі етанолу, і легко заміщаються на йод з утворенням трийодацетальдегіду (йодалю). Під дією лугу йодаль легко перетворюється на йодоформ і сіль мурашиної кислоти (форміат). Йодоформ випадає в осад у вигляді яскраво-жов- тих кристалів і виявляється за характерним запахом.
|
|
O |
3HOI |
O |
KOH |
CHI3 + H |
|
O |
|
CH3 |
|
C |
- 3H2O |
I3C C |
|
|
C |
||
|
|
H |
H |
|
|
|
|
OK |
|
|
|
|
|
|
|
|
|||
Ацет |
|
Йодаль |
|
Йодо- |
Форміат |
||||
альдегід |
|
|
|
форм |
|
|
калію |
||
1.4. СТРУКТУРА, ВЛАСТИВОСТІ ТА БІОЛОГІЧНЕ ЗНАЧЕННЯ КАРБОНОВИХ КИСЛОТ
Карбоновими кислотами називають сполуки, що містять карбоксильну групу –СООН. За кількістю карбоксильних груп карбонові кислоти підрозділяються на монокарбонові, або одноосновні (містять одну групу –СООН), дикарбонові, або двохосновні (дві групи –СООН) тощо. Залежно від будови вуглеводного радикала карбонові кислоти можуть бути аліфатичними, аліциклічними або ароматичними.
Кислотні властивості карбонових кислот
Кислотні властивості карбонових кислот по- в’язані з властивістю атома Гідрогену карбоксильної групи відщеплювати протон:
26

|
|
|
|
|
КАРБОНОВІ КИСЛОТИ |
Декарбоксилювання карбонових кислот |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
Монокарбонові |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Дикарбонові |
Здатність до декарбоксилювання залежить від |
||||||||||||||||||||||||||||||||||||||||||||
CH3 |
|
COOH |
|
|
|
|
Аліфатичні |
HOOC |
|
CH2 |
|
CH2 |
|
COOH |
будови кислоти. Монокарбонові кислоти втра- |
||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
чають СО2 |
важко, тільки при нагріванні їх солей |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||
Оцтова кислота |
|
|
|
|
|
|
|
|
|
|
|
Бурштинова кислота |
|||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
з твердими лугами. |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HOOC COOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Щавлева кислота |
|
|
|
|
|
|
|
|
O |
|
|
|
|
t °Ct |
CH + |
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
|
|
|
|
|
C |
+ |
NaOH |
Na CHO |
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HOOC |
|
|
CH2 |
|
COOH |
3 |
|
|
|
|
ONa |
|
|
|
4 |
2 3 |
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Малонова кислота |
Про введенні в молекули кислот електроноак- |
||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HOOC |
|
CH2 CH2 CH2 COOH |
||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
цепторних замісників –СООН, –NH2 схильність |
|||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Глутарова кислота |
||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
їх до декарбоксилювання підвищується. Тому |
||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
COOH |
щавлева кислота декарбоксилюється вже при |
||||||||||||||||||||||||||
|
|
COOH |
|
|
|
|
|
|
|
Аліциклічні |
|
|
|
|
|
|
|
|
|
|
|
|
|
слабкому нагріванні: |
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CООH |
HOOC—COOH → |
|
HCOOH |
+ CO2↑ |
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
Циклогексан- |
|
|
|
|
|
|
|
|
|
|
|
Циклогексан-1,2- |
|
|
|
|
|
|
-I |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
карбонова кислота |
|
|
|
|
|
|
|
|
|
|
|
|
дикарбонова |
Однак декарбоксилювання будь-яких кислот |
|||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
кислота |
легко здійснюється ферментативним шляхом в |
||||||||||||||||||||||||||||||||||
|
|
COOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
COOH |
організмі. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
Ароматичні |
|
|
|
|
|
|
|
|
|
|
|
|
|
COOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
Бензенова кислота |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Фталева кислота |
Реакції нуклеофільного заміщення |
|||||||||||||||||||||||||||||||||||||||||||||
Рис. 1.6. Класифікація карбонових кислот |
з утворенням ефірів, амідів кислот, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
ангідридів кислот (SN) |
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Вони є найбільш характерними для карбоно- |
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
δ -- |
-M; -I |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
вих кислот. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
δ + O |
|
|
Кислотний центр |
Хімічні властивості карбонових кислот зумов- |
|||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
R |
|
|
C |
|
|
|
|
|
лені наявністю карбоксильної групи. |
|||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
O |
|
|
H +M>-I |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||
Спряження карбоксильної групи здійснюєть- |
|
|
|
|
|
|
δ - |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||
ся за рахунок делокалізації неподіленої пари |
|
|
|
|
|
|
-M; -I |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||
δ + O |
|
Електрофільний центр |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
електронів атома Оксигену гідроксильної групи |
R |
C |
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
O |
|
|
H +M>-I |
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||
й електронів π -зв’язку карбонільної групи, тоб- |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||
то ρ ,π -зв’язку. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Найважливіша група реакцій карбонових |
||||||||||||||||||||||||||||||||
Електронна щільність у ρ ,π -сполученій сис- |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
кислот — це реакції нуклеофільного заміщення. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
темі зміщена в бік електронегативного атома Ок- |
sp2-гібридизований атом Карбону карбок- |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
сигену карбонільної групи. При такій елект- |
сильної групи завдяки електроноакцепторним |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
ронній будові зв’язок О–Н виявляється надто по- |
властивостям атома Оксигену оксогрупи має |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
ляризованим, що зумовлює появу –ОН-кислот- |
частково позитивний заряд, тобто є електрофіль- |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
ного центру. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ним центром. Він може атакуватися нуклеофіль- |
||||||||||||||||||||||||||
Карбонові кислоти значно перевершують за |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
ними частинками, внаслідок чого відбувається |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
кислотністю спирти та феноли. Завдяки повній |
заміщення гідроксильної групи в групі –СООН |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
делокалізації заряду на двох електронегативних |
на іншу нуклеофільну частинку. |
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
атомах Оксигену карбоксилатіон має значно |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||
вищу стабільність. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Реакція етерифікації |
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
При взаємодії карбонових кислот із спиртами |
|||||||||||||||||||||
|
|
|
δ |
-- |
|
|
|
|
|
+ |
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
O- |
в присутності сильних мінеральних кислот утво- |
|||||||||||||||||||||||||||||||||
|
|
|
δ + O |
|
- Н+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
R |
|
|
C |
рюються складні ефіри. |
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||
|
|
R |
C |
|
|
|
|
|
|
|
|
|
|
R C |
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
O |
|
|
H |
|
|
|
|
|
|
|
O- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
O |
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||
|
|
Карбонова |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
кислота |
|
|
|
|
|
|
|
R |
|
C |
R |
|
C |
|
+ R'OH |
|
|
|
|
|
R |
|
C |
+ H2O |
|||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
OR |
|||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Карбоксилатіон |
Оскільки гідроксидіон (–ОН) — міцно зв’яза- |
|||||||||||||||||||||||||||||||||||||||||||
Утворення стабільних аніонів оксикислот та |
на група, то реакції нуклеофільного заміщення в |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
карбоксильній групі відбуваються в присутності |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
амінокислот можливе у фізіологічних умовах, |
кислотних каталізаторів, особливо у тих випад- |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
звідси зрозумілі назви аміно-, оксо-, оксикислот |
ках, коли використовуються слабкі нуклеофільні |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
у біохімії. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
реагенти — спирти. Для активації карбоксиль- |
|||||||||||||||||||||||
|
|
Глютамінова кислота = глутамат |
ної групи застосовують кислотний каталізатор. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
Аспарагінова кислота = аспартат |
Складний ефір утворюється не тільки зі спир- |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
Піровиноградна кислота = піруват |
ту та карбонової кислоти, але й зі спирту та кис- |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
Молочна кислота = лактат |
невмісної неорганічної кислоти (H2SO4, H3PO4). |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||
27

|
|
|
|
|
|
O |
|
|
|
|
|
|
|
O |
|
|
|||
R'OH + HO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH + H2O |
||||
|
|
S |
|
|
OH |
|
|
|
R'O |
|
S |
|
|||||||
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
O |
|
|
|||
|
|
|
|
|
OH |
|
|
|
|
|
|
OH |
|||||||
|
+ |
|
|
|
|
|
|
|
|
|
|
|
|
R'O |
|
|
|
OH + H O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
R'OH |
HO P |
OH |
|
P |
|||||||||||||||
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
2 |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
||||
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
||||||
Численні реакції фосфорилування в біохімії можна розділити на дві групи: до однієї належать реакції, що ведуть до утворення складноефірного зв’язку, до другої — реакції утворення ангідридного зв’язку.
|
|
|
|
|
|
|
OH |
O |
|
OH |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
O |
|
P |
|
OH |
C |
O |
P OH |
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
O |
||
Складний ефір |
Ангідрид |
|||||||||||
У процесі гліколізу бере участь 1,3-бісфосфо- гліцерат, що містить складно-ефірний та ангідридний зв’язки:
O OH
C O |
|
P O |
|
|
|
Ангідридний зв’язок |
|
|
|
|
|||
CHOH |
OH |
|
||||
OH |
|
|||||
|
|
Складно-ефірний зв’язок |
||||
CH2 |
O P O |
|
|
|||
|
||||||
|
|
OH |
|
|||
Ангідриди карбонових кислот можуть містити залишки однакових кислот або бути змішаними.
|
|
O |
|
|
|
|
O |
|
|
|
O |
|
|
|
|
|
|
|
|
|
O |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R + H2O |
||
R |
|
C |
|
|
O H + HO |
|
|
C |
|
|
R |
|
|
|
R |
|
C |
|
|
|
O |
|
|
O |
|
|
C |
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Ангідрид |
|||||||||||||||
|
|
|
O |
|
|
|
|
|
O H |
|
|
|
|
|
O |
|
|
|
|
|
|
O H |
||||||||||||||||
|
|
|
|
O H + HO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
R |
|
C |
|
|
P |
|
|
O H |
|
|
|
R |
|
C |
|
O |
|
P |
|
|
O H + H2O |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Ангідрид |
||||||||||||||||
Перехід карбоксилвмісних сполук в ангідридну форму становить хімічну основу активації жирних кислот, амінокислот, жовчних кислот, необхідних для участі в наступних перетвореннях.
В організмі процес активації карбоксилвмісних сполук здійснюється за рахунок утворення ациладенілатів змішаних ангідридів карбонових кислот і АТФ.
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O- |
|
|
|
O- |
|
|
O- |
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
-O |
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
||||||||||
|
|
|
|
O |
|
|
|
|
P |
|
|
|
O |
|
P |
|
|
O |
|
P |
|
|
|
OCH2 |
O |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
O- |
+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
R |
|
|
C |
|
|
|
O |
|
|
|
O |
|
|
O |
|
|
|
|
|
|
|
|
N |
|
N |
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||
Ацилат |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
АТФ OH OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
O- |
|
|
|
|
|
|
|
|
|
|
N |
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
R |
|
|
C |
|
O |
|
|
P |
|
|
|
|
OCH2 O |
|
|
|
|
|
|
|
|
- |
|
|
|
|
|
|
|
- |
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
O |
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
-O |
|
|
|
|
|
|
O- |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
H |
|
|
|
|
|
|
|
+ |
|
|
P |
|
|
|
O |
|
|
P |
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
O |
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
Ациладенілат Дифосфатіон
Ациладенілат є проміжним продуктом при утворенні тіоефірів жирних кислот (ацил-КоА):
|
|
|
|
|
O |
|
|
|
O- |
O- |
|||
RCOO- + АТФ + KoASH |
|
|
|
|
АМФ + |
-O |
|
|
|
|
|
O- |
|
|
R |
|
C |
+ |
|
P |
O P |
|
|||||
|
|
|
|
||||||||||
|
|
||||||||||||
|
|
|
|
|
SKoA |
|
|
|
O |
O |
|||
|
|
|
|
|
|
|
|
|
|||||
Утворення амідів кислот залежно від ступеня заміщення у атома Нітрогену можуть бути первинними — RCONH2, вторинними — RCONHR′ і третинними — RCONR′R′′.
Амід кислоти
|
|
|
|
|
|
|
|
O |
|
|
|
O + NH3 |
|
|
R |
|
C |
+ H2O |
|
|
|
|
|
||||||
|
|
|
|
|
|
|
NH2 |
|
|
R |
|
C |
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
||
|
|
OH + NH2R |
|
|
|
|
|
|
|
|
|
|
|
R |
|
C |
+ H |
O |
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
NHR |
|
N-заміщений амід (вторинний)
Конденсація Кляйзена характерна для по-
хідних карбонових кислот складних ефірів і тіоефірів:
|
|
|
|
O |
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
||
|
|
2CH3 |
|
C |
|
|
CH3 |
|
C |
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
OC H |
5 |
|
|
|
CH2 |
|
|
O |
|
C2H5 |
|
|||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
O |
|
|
|
O |
|
|
|
O - |
O |
|||||||||
|
|
|
+ CH |
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|||||
CH |
|
C |
|
|
C |
|
|
|
C |
|
CH2 |
|
C |
|
||||||
|
|
|
|
|
|
|
|
|
||||||||||||
3 |
|
OC H |
2 |
|
OC H |
|
|
|
|
|
|
|
|
|
|
|
OC2H5 |
|||
|
|
5 |
|
|
|
|
|
OC2H5 |
||||||||||||
2 |
|
|
2 5 |
|
|
|
|
|||||||||||||
O O
 CH3 C CH2 C OC2H5
CH3 C CH2 C OC2H5
Ацетооцтовий ефір
Процес β -окиснення жирних кислот включає реакцію, зворотну конденсації Кляйзена, в якій коензим А заміщає ацетилкоензим А, і утворюється жирна кислота, що містить на два атоми Карбону менше вихідної.
Будова і властивості дикарбонових кислот
До дикарбонових кислот належать сполуки з двома карбоксильними групами. Це білі кристалічні речовини, які мають більш кислий характер, ніж монокарбонові кислоти. У міру віддалення електроноакцепторних груп (–СООН) одна від одної сила кислоти в ряді помітно зменшується: щавлева — малонова — бурштинова кислоти.
Кислотні властивості. Порівняно з монокар-
боновими кислотами дикарбонові кислоти мають сильніші кислотні властивості. Висока кислотність більш низьких дикарбонових кислот пояснюється сильною електроноакцепторною дією другої карбоксильної групи, яка сприяє делокалізації негативного заряду на аніоні, який утворився після відриву протона.
O |
|
O |
||
HOOC C |
|
|
|
HOOC C + H+ |
|
|
|||
O H |
|
O- |
||
Щавлева кислота |
Гідроксалатіон |
|||
28