Материал: Біологічна та біоорганічна хімія_Мардашко О.О._ изд. 2008-342 с._ОНМедУ-2012

CH3 |
δ + δ - |
CH3 |
|
CH3 |
CH3 |
|||||||
|
|
|
|
|
|
|
|
|
|
|||
H |
C |
|
O |
|
C O |
|
C |
|
O |
C |
|
O |
|
|
|
|
|
||||||||
|
|
|
H3C |
|
|
|
|
|
H3C |
|||
|
|
|
|
H3C |
|
CH2 |
CH |
|||||
|
|
|
|
|
||||||||
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
H3C |
||
Іонний механізм спостерігається, як правило, при розриві полярного ковалентного зв’язку (Карбон-Хлор, Карбон-Оксиген).
Характеристика нуклеофілів і електрофілів
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Органічні іони вступають у подальші пере- |
|||||||||||||
|
зменшення реактивної здатності |
||||||||||||||||||||||||||||
|
творення. При цьому катіони взаємодіють із нук- |
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
леофільними («що люблять ядра») частинками |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(Н2О, NН3, Cl-, Br-, I-, інші аніони кислот тощо), |
|||||||||||||
Класифікація реакцій за спрямованістю |
а органічні аніони — з електрофільними («що |
||||||||||||||||||||||||||||
та результатом. Класифікація реакцій |
люблять електрони») частинками (Н+, катіони |
||||||||||||||||||||||||||||
за механізмом |
|
|
|
|
|
|
|
металів, галогени та ін.). |
|
||||||||||||||||||||
Реакцію можна класифікувати залежно від |
Нуклеофільна частинка (нуклеофіл, N) — це |
||||||||||||||||||||||||||||
частинка, яка має пару електронів на зовніш- |
|||||||||||||||||||||||||||||
того, у скількох молекулах змінюється стан кова- |
ньому електронному рівні. За рахунок цієї пари |
||||||||||||||||||||||||||||
лентних зв’язків під час визначальної кінетики, |
електронів нуклеофіл здатний утворювати новий |
||||||||||||||||||||||||||||
тобто найповільнішої стадії реакції. При такому |
ковалентний зв’язок. |
|
|
|
|
|
|
|
|
||||||||||||||||||||
підході розрізняють реакції мономолекулярні, |
Електрофільна частинка (електрофіл, Е) — це |
||||||||||||||||||||||||||||
бімолекулярні, тримолекулярні, полімолекулярні. |
частинка, яка має незаповнений валентний елек- |
||||||||||||||||||||||||||||
До мономолекулярних реакцій належать ре- |
тронний рівень. Електрофіл надає заповнені ва- |
||||||||||||||||||||||||||||
акції дециклізації, дисоціації, внутрішньомолеку- |
кантні орбіталі для утворення ковалентного |
||||||||||||||||||||||||||||
лярні перегрупування. |
|
|
|
|
|
|
|
зв’язку за рахунок електронів тієї частинки, з |
|||||||||||||||||||||
Бімолекулярні реакції є найхарактернішими |
якою він взаємодіє. |
|
|
|
|
|
|
|
|
||||||||||||||||||||
для органічних сполук, перебігають у розчинах, |
За кінцевим результатом органічні реакції |
||||||||||||||||||||||||||||
допускають наявність двох компонентів у орга- |
поділяються таким чином: |
|
|||||||||||||||||||||||||||
нічній суміші: |
|
|
|
|
|
|
|
|
|
1. Реакції заміщення, S ( від англ. substitution). |
|||||||||||||||||||
|
СН3J + NaOH → |
CH3OH + NaJ |
2. Реакції приєднання, А (від англ. аddition). |
||||||||||||||||||||||||||
|
3. Реакції елімінування, Е (від англ. еlimi- |
||||||||||||||||||||||||||||
Речовину, що зазнала перетворення під час |
nation — відщеплення). |
|
|
|
|
|
|
|
|||||||||||||||||||||
перебігу хімічної реакції, називають субстратом. |
4. |
Реакції перегрупування. |
|
||||||||||||||||||||||||||
5. Окисно-відновні реакції. |
|
||||||||||||||||||||||||||||
Речовину, під дією якої відбувалася зміна в суб- |
|
||||||||||||||||||||||||||||
Враховуючи природу атакуючого реагенту, |
|||||||||||||||||||||||||||||
страті, називають реагентом. Перебіг реакції за- |
|||||||||||||||||||||||||||||
механізми реакції можуть бути такими: SR, SE, SN, |
|||||||||||||||||||||||||||||
лежить від природи субстрату і від природи реа- |
A , A . |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
генту. |
|
|
|
|
|
|
|
|
|
|
|
|
|
E |
N |
|
|
|
|
|
|
|
|
|
|
|
|||
Органічні реакції можна класифікувати і за |
Перебіг реакції залежить від типу ковалент- |
||||||||||||||||||||||||||||
них зв’язків, електронних ефектів у субстраті, |
|||||||||||||||||||||||||||||
механізмом розриву ковалентних зв’язків у реа- |
|||||||||||||||||||||||||||||
гуючих молекулах. Залежно від способів його |
природи атакуючої частинки, зовнішніх фак- |
||||||||||||||||||||||||||||
торів (hν , Р, Т). |
|
|
|
|
|
|
|
|
|||||||||||||||||||||
розриву і будується ця класифікація. |
У живих клітинах перебігає безліч фермента- |
||||||||||||||||||||||||||||
1. Якщо спільна електронна пара ділиться між |
|||||||||||||||||||||||||||||
тивних реакцій, об’єднаних загальним поняттям |
|||||||||||||||||||||||||||||
атомами, то утворюються радикали — частинки, |
|||||||||||||||||||||||||||||
що мають непарні електрони. Такий розрив |
метаболізм. В основі метаболічних шляхів лежить |
||||||||||||||||||||||||||||
зв’язку називається радикальним, |
або гомолітич- |
досить невелике коло хімічних реакцій, знання |
|||||||||||||||||||||||||||
ним: |
|
|
|
|
|
|
|
|
|
|
|
|
|
суті яких створює основу для раціонального при- |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
значення лікарських препаратів. Винятково важ- |
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
А |
|
• |
|
Б |
→ |
А• + Б• |
|
А•, Б • — радикали (R) |
ливим є з’ясування молекулярних механізмів де- |
|||||||||||||||||||
|
|
• |
|
|
|
яких захворювань і значної кількості вроджених |
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
H |
|
|
|
|
|
H |
|
|
|
|
|
|
|
порушень метаболізму. |
|
|
|
|
|
|
|
|||||||
|
•• • |
• |
|
|
→ |
•• • |
H• |
H• |
— радикал Гідрогену |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
H • •C• |
• |
H |
H ••C•• + |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
H |
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
Електрофільне приєднання |
|
|||||||||||
|
Метан |
|
|
Радикал |
|
|
|
|
|
|
|
|
|
до ненасичених сполук (А ) |
|
||||||||||||||
|
|
|
|
|
|
|
метил |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Е |
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
2. Якщо при розриві зв’язку спільна електрон- |
Електронна хмара π -зв’язку алкену піддаєть- |
||||||||||||||||||||||||||||
ся атаці електрофільними реагентами. Тому вели- |
|||||||||||||||||||||||||||||
на пара залишається біля одного атома, то ут- |
ка кількість реакцій алкенів відбувається за ме- |
||||||||||||||||||||||||||||
ворюються іони — катіон та аніон. Такий ме- |
ханізмом електрофільного приєднання, який по- |
||||||||||||||||||||||||||||
ханізм розриву називається іонним, або гетеро- |
значається символом АЕ (від англ. |
аddition |
|||||||||||||||||||||||||||
літичним. |
|
|
|
|
|
→ |
|
|
|
|
|
|
|
electrophіlіc). Реакції електрофільного приєднан- |
|||||||||||||||
|
|
|
|
|
А |
• |
|
• - |
+ |
[Б] |
+ |
|
|
ня — це іонні процеси, які перебігають у кілька |
|||||||||||||||
|
|
|
|
|
• Б |
[А]• |
|
|
|
||||||||||||||||||||
|
Гетеролітичний |
аніон |
катіон |
стадій: |
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
розрив |
|
|
|
|
|
|
|
|
|
|
|
повільно |
|
H+ |
|
|||||||||||||
|
|
|
|
|
|
|
|
→ |
|
+ |
+ |
• |
|
- |
|
|
C C |
+ H+ |
|
|
|
C |
|
C |
|
|
|
C C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
CH3Cl |
CH3 |
•Cl |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
хлористий |
метил- |
хлорид |
алкен |
(Е) |
π |
-комплекс карбкатіон |
||||||||||||||||||||||
|
|
метил |
|
катіон |
|
аніон |
|||||||||||||||||||||||
19
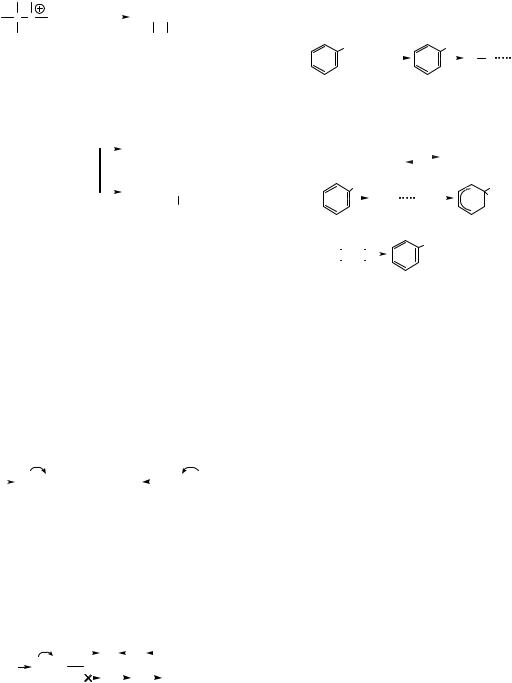
На першій стадії відбувається взаємодія елек- |
У вторинному карбкатіоні відбувається більш |
|||||||||||
трофільної частинки з електронною хмарою π - |
ефективне зниження позитивного заряду за ра- |
|||||||||||
зв’язку. Позитивно заряджена електрофільна час- |
хунок +І-ефекту двох алкільних груп. |
|||||||||||
тинка за рахунок електростатичного притягнен- |
Електрофільне заміщення |
|||||||||||
ня утворює з молекулою алкену π -комплекс. В |
||||||||||||
якості електрофіла найчастіше виступає протон |
в ароматичних сполуках (SЕ) |
|||||||||||
(Н+), джерелом якого є протонвмісні кислоти |
Арени вступають в іонні реакції, які перебіга- |
|||||||||||
НСl, НВr, H2SO4. Потім утворюється ковалент- |
||||||||||||
ють за механізмом електрофільного заміщення, |
||||||||||||
ний зв’язок між протоном та одним із атомів Кар- |
яке позначається символом SЕ (від англ. substi- |
|||||||||||
бону подвійного зв’язку, який отримує позитив- |
tution electrophіlіc). Реакція починається з виник- |
|||||||||||
ний заряд, і вся частинка стає карбкатіоном. |
нення π -комплексу, з якого потім утворюється σ - |
|||||||||||
Карбкатіон — це частинка з позитивним за- |
комплекс, та завершується стабілізацією σ -ком- |
|||||||||||
рядом на атомі Карбону. |
|
|
|
|
|
|
|
плексу за рахунок відщеплення протона. |
||||
На другій стадії процесу карбкатіон взає- |
||||||||||||
Утворення π -комплексу. На першій стадії елек- |
||||||||||||
модіє з аніоном Х- і утворює з ним σ -зв’язок за |
трофільна частинка притягується до π -електрон- |
|||||||||||
рахунок пари електронів аніона. |
|
|
|
|
|
|
|
ної хмари арену й утворює з ним комплекс. Аро- |
||||
|
|
|
|
|
|
|
|
|
|
|
||
|
швидко |
|
|
Н |
|
Х |
матична система при цьому не порушується. Ця |
|||||
|
|
|
|
стадія перебігає швидко. |
||||||||
C C + Х– |
|
|
|
|
|
|
|
|
|
|||
|
|
C |
|
C |
|
|
||||||
|
|
|
|
|
||||||||
(N)
Якщо початковий алкен несиметричний, тобто атоми Карбону при подвійному зв’язку відрізняються ступенем заміщення (наприклад, пропен СН3–СН=СН2), то із двох можливих продуктів реакції переважно утворюється тільки
один:
2-Бромпропан
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
CH |
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
HСНC |
|
|
CH |
|
CH + HBr |
|
|
|
|
|
Br |
H |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||
3 |
3 |
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
Пропен |
|
CH3 |
|
|
CH |
|
CH2 |
|
|
|
|
||||
|
|
|
|
||||
|
|
|
|
H |
|
Br |
|
1-Бромпропан (не утворюється)
Уцьому випадку напрямок реакції визначається закономірністю, встановленою російським хіміком В. В. Марковніковим (1869).
Правило Марковнікова: при приєднанні моле-
кул типу НХ (HCl, HBr, HOH) до несиметричних алкенів атом Гідрогену приєднується до більш гідрогенізованого атома Карбону подвійного зв’язку.
Такий напрямок реакції пояснюється двома факторами.
Устатичному, тобто нереагуючому, стані в несиметричному алкені під впливом замісника електронна щільність зміщується до одного з атомів Карбону:
|
|
δ + |
δ - |
|
|
δ - |
|
δ + |
|
CH3 |
|
CH |
|
CH2 |
Cl |
|
CH |
|
CH2 |
|
|
|
|
||||||
+І-ефект (–СН3)-група |
–І-ефект (СІ) |
||||||||
|
Пропен |
|
|
Хлоретен |
|||||
Упропені місцем атаки буде атом С-1 із частково негативним зарядом, який виникає під дією +І-ефекту метильної групи.
Удинамічному стані, тобто у процесі реакції, із двох можливих карбкатіонів буде утворювати-
ся більш стійкий вторинний карбкатіон.
|
|
|
|
Вторинний+карбкатіон |
||||||||||
|
δ + δ - |
|
|
CH3 |
|
CH |
|
|
CH3 |
|||||
|
+ |
|
|
|
|
|||||||||
|
Н+ |
|
|
|
|
|
|
|
|
|
|
|||
CH3 |
CH |
|
CH2 |
|
CH3 |
|
|
|
|
|
+ |
|||
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
Первинний карбкатіон |
||||||||||
H |
|
H |
δ + |
δ - |
|
+ CI2 |
AlCI3 |
Cl |
CI |
AlCI3 |
|
|
|
||||
Бензен (Арен) π -комплекс
Роль каталізатора (АlCl3, FeCl3) полягає в поляризації нейтральної молекули галогену з утворенням із неї електрофільної частинки:
Cl–Cl + AlCl3 |
|
|
|
|
ClCl3+[AlCl4]– |
|||||
|
|
|
|
|||||||
|
|
|
||||||||
|
H |
δ + |
δ - |
|
|
|
|
H |
||
|
|
|
|
|
|
+ CI + |
||||
|
|
Cl |
|
CI |
AlCI3 |
|
|
|||
|
|
|
|
|
||||||
π -комплекс |
Карбкатіон (σ -комплекс) |
||||||
|
|
|
|
|
|
||
+ |
|
|
- |
|
|
ClHI |
|
AlCI |
4 |
|
|
+HCI + AlCI |
|||
|
|
||||||
|
|
|
|
3 |
|||
Комплекс- |
Хлор- |
||||||
ний аніон |
бензен |
||||||
Утворення σ -комплексу. На цій повільній ста-
дії відбувається утворення ковалентного зв’язку між електрофільною частинкою (Сl-) та одним з атомів Карбону бензенового кільця. Зв’язок утворюється за рахунок двох електронів кільця, при цьому атом Карбону з sр2-гібридизованого стану переходить в sр3. Ароматична система при цьому порушується, молекула бензену перетворюється на карбкатіон.
Відщеплення протона. Порушення ароматич-
ності енергетично невигідне, тому структура σ -комплексу менш стійка, ніж ароматична. Для відновлення ароматичності відбувається відщеплення протона від атома Карбону, зв’язаного з електрофілом. При цьому два електрони повертаються в π -систему, тим самим відновлюється ароматичність.
Вплив замісників на реакційну здатність аренів (SЕ)
Якщо в бензеновому кільці є замісник, то він порушує рівномірний розподіл електронної щільності в кільці, і виникає положення з підвищеною та зниженою електронною щільністю. Наступні замісники прагнуть вступити в положення з підвищеною щільністю. Таким чином, замісники в бензеновому кільці визначають напрямок реакцій заміщення.
20

Усі замісники поділяються на два типи. Замісники І роду (електронодонорні) збільшу-
ють електронну щільність і спрямовують реакції заміщення переважно в орто- та пара-положен- ня. До них належать такі групи (знизу вказані електронні ефекти, які спостерігаються під впливом цієї групи):
–СН3 |
–ОН –NН2 |
Сl |
Вr |
+I |
+M, –I +M, –I |
+M, –I |
+M, –I |
Неподілена пара гетероатомів (О, N, S) цих груп вступає в спряження із π -електронною системою бензенового кільця. Такий тип спряження називається ρ ,π -спряженням (мезомерний ефект). Під впливом електронодонорних замісників (+Мефект) відбувається перерозподіл електронної щільності в бензеновому кільці з деяким її зосередженням в орто- і пара-положеннях.
H
 O
O
δ - |
|
δ - |
–ОН-група справляє |
|
|||
|
|||
|
+Мефект та –І-ефект, але |
||
|
|
||
|
|
|
+Мефект превалює
δ -
Фенол
Замісники II роду (електроноакцепторні) спрямовують наступне заміщення переважно в мета- положення. До них належать такі групи:
–NО2 |
–СООН |
–ССl3 |
–М, –I |
–М, –I |
–I |
Електроноакцепторні замісники справляють Мефект і знижують електронну щільність у спряженій системі. Електронна щільність бензенового кільця в цілому знижується, однак у мета-поло- женні — в меншому ступені, тому наступне заміщення спрямовується в це положення.
H O
C
δ - δ -
Бензальдегід
Нуклеофільне заміщення насиченого атома Карбону (SN)
Взаємодія спиртів із карбоновими кислотами відбувається за механізмом нуклеофільного заміщення (SN). В якості нуклеофіла виступає молекула спирту, котра атакує атом Карбону карбоксильної групи кислоти, яка, у свою чергу, несе частковий позитивний заряд.
|
|
|
δ - |
|
|
|
|
|
|
|
|||
|
δ + O |
|
|
|
|
|
|
|
|||||
CH3OH + CH3 |
|
C |
|
|
|
|
|
CH3O |
|
C |
|
CH3 + H2O |
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|||||||||
|
|
|
HОН |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
O |
||||||||
Метан Оцтова Метилaцетат кислота
Гідроксигрупа має:
+М(ОН) — позитивний мезомерний ефект
 δ - –І(ОН) — негативний індуктивний ефект
δ - –І(ОН) — негативний індуктивний ефект
δ + O R C
OН
Електрофільний центр
Карбонова
кислота
У нуклеофільних реакціях похідних карбонових кислот необхідний кислотний аналіз, що веде до появи більш повного позитивного заряду на атомі Карбону, що полегшує атаку нуклеофілам.
|
|
O |
+ |
OH |
|||
R |
|
C + H+ |
|
R |
|
C |
|
|
|
|
|||||
|
|
X |
|
|
|
|
X |
|
|
|
Похідне |
|
|
Активована |
|
||||||||
|
|
карбонової |
молекула похідної |
||||||||||||
|
|
|
кислоти |
карбонової кислоти |
|||||||||||
+ |
OH |
|
|
OH |
|
|
|
|
O |
||||||
|
|
|
|
|
|
|
|
|
|
||||||
R |
|
C |
+ Y- |
|
R |
|
C |
|
Y |
- |
R |
|
C |
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
||||||||||
|
|
|
X |
|
|
|
|
|
|
- X |
Y |
||||
|
|
|
|
|
X |
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||
Нуклеофіл
Радикальне заміщення насиченого атома Карбону (SR)
При взаємодії алканів із галогенами (хлором, бромом) під впливом УФ-випромінювання або високої температури утворюється суміш продуктів від монодо полігалогензамісних алканів.
CH4 + 5Cl2 hυ  CH3Cl + CH2Cl2 + CHCl3 + CCl4
CH3Cl + CH2Cl2 + CHCl3 + CCl4
Ініціювання. На цій стадії відбувається розпад молекули хлору на два вільних радикали:
• |
hυ |
|
|
|
|
Cl • Cl |
|
2Cl• |
Ріст ланцюга. Радикал хлору атакує зв’язок С–Н у молекулі метану, зв’язок при цьому розривається гомолітично, утворюються радикал Гідрогену та нейтральна молекула НСl:
Cl• + |
|
|
hυ |
|
|
• |
|
|
• |
||
H • |
CH3 |
|
H • Cl + H3C• |
||
Радикал Метан |
|
Метил- |
|||
хлору |
|
|
|
|
радикал |
У метильному радикалі атом Карбону знаходиться в стані sр2-гібридизації, тобто має плоску будову. На вільній р-орбіталі знаходиться один електрон. Висока реакційна здатність метильного радикалу пояснюється прагненням до утворення ковалентного зв’язку за участю цього електрона й доступністю для взаємодії р-орбіталі.
Н3С• + |
• |
→ |
• |
+ Cl• |
Сl • Cl |
H3C • Cl |
Хлорметан
Радикал хлору знову атакує молекулу метану, далі повторюються описані вище реакції. У результаті одержують суміш продуктів різного ступеня хлорування — хлорметан СН3Сl, ди-
21
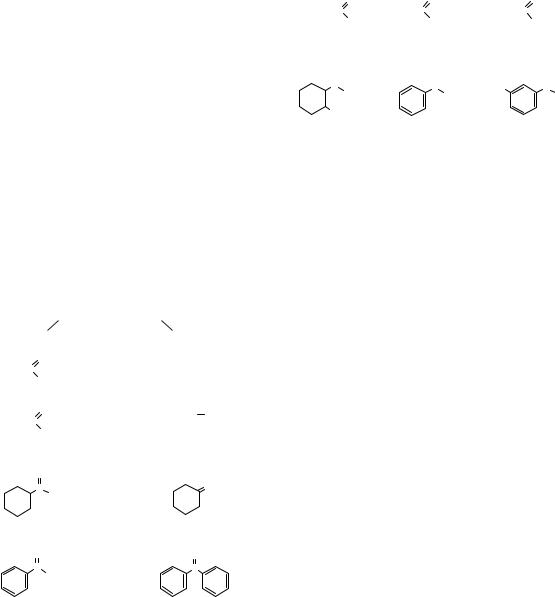
хлорметан СН2Сl2, трихлорметан СНСl3 та тетрахлорметан. Процеси такого типу називаються ланцюговими, оскільки один вільний радикал хлору міг би ініціювати хлорування всіх молекул метану, які знаходяться у реакційному середовищі.
Обрив ланцюга. Послідовні реакції росту ланцюга можуть перерватися, якщо відбудеться зникнення вільного радикала.
Cl• + Cl• → |
• |
Cl |
Cl • |
1.3. БУДОВА ТА ВЛАСТИВОСТІ АЛЬДЕГІДІВ І КЕТОНІВ
Органічні сполуки, у молекулі яких є карбонільна група 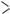 C=O, називають карбонільними
C=O, називають карбонільними
сполуками, або оксосполуками. Карбонільні спо-
луки діляться на дві великі групи — альдегіди і кетони.
Альдегіди містять у молекулі карбонільну групу, обов’язково зв’язану з атомом Гідрогену, тобто альдегідну групу –СН=О.
Кетони містять карбонільну групу, зв’язану з двома вуглеводневими радикалами, тобто кетонну групу.
Залежно від будови вуглеводневих радикалів альдегіди і кетони бувають аліфатичними, аліциклічними й ароматичними. У молекулі кетону радикали можуть бути однаковими або різними. Тому кетони, як і прості ефіри, діляться на симетричні й несиметричні. Приклад змішаного кетону
— метилфенілкетон (оцетфенон) С6Н5СОСН3.
ОКСОСПОЛУКИ
Альдегіди Кетони
|
|
|
|
O |
|
|
|
|
O |
||||
R |
|
|
C |
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
H |
|
R |
|
C |
|
R |
|||
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
CH3 |
|
|
|
C CH3 |
|||
CH3 |
|
|
C |
Аліфатичні |
|
||||||||
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
H |
|
|
|
|
|
O |
|||
Ацетальдегід Ацетон
O |
|
|
C |
Аліциклічні |
O |
H |
|
Циклогексанкарбальдегід Циклогексанон
O |
|
O |
C |
Ароматичні |
C |
H |
|
|
Бензальдегід |
|
Бензофенол |
Номенклатура та ізомерія
У назвах аліфатичних альдегідів за замісною номенклатурою наявність альдегідної групи (за умови, що вона є старшою) відображається суфіксом -аль. Основою служить назва родона-
чального вуглеводню (головного вуглецевого ланцюга). Нумерація головного ланцюга починається з атома Карбону альдегідної групи. У деяких альдегідів зберігаються й тривіальні назви, утворені від назв кислот, на які альдегіди перетворюються при окисненні, з додаванням слова «альдегід».
Назви аліциклічних альдегідів походять від назви відповідного карбоциклу (при цьому атом Карбону альдегідної групи не нумерується) з додаванням закінчення -карбальдегід, а ароматичних альдегідів — від родоначальної структури ряду — бензальдегіду.
|
|
O |
|
|
O |
|
|
|
|
O |
H |
|
C |
CH3 |
|
C |
CH3 |
|
CH2 |
|
C |
|
|
|
|
|||||||
|
|
H |
|
|
H |
|
|
|
|
H |
Метаналь |
Етаналь |
Пропаналь (пропіо- |
||||
(формальдегід) (оцетальдегід) |
новий альдегід) |
|||||
|
O |
O |
|
O |
||
|
|
|
|
|
|
|
|
C H |
|
C H |
Br |
|
C H |
CI |
|
|
|
|
|
|
2-Хлорциклогексан- |
Бенз- |
3-Бромбенз- |
||||
карбальдегід |
альдегід |
|
альдегід |
|||
Назви аліфатичних кетонів дають, взявши за основу головний вуглецевий ланцюг, до складу якого входить атом Карбону кетонної групи, з додаванням суфікса -он. Нумерацію головного ланцюга починають із того кінця, ближче до якого перебуває кетонна група.
Для назви кетонів, особливо ароматичних, використовується радикально-функціональна номенклатура. У цьому випадку в назві перераховуються за алфавітом радикали, зв’язані з карбонільною групою, з додаванням слова «кетон». Деякі кетони мають також тривіальні назви (ацетон, бензофенон та ін.).
CH3 |
|
C |
|
CH3 |
CH3 |
|
C |
|
CH2 |
|
CH3 |
||
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
O |
|
|
|
|
||||
Пропанон |
|
Бутанон |
|||||||||
(диметилкетон) |
(метилетилкетон) |
||||||||||
(Ацетон) |
|
|
|
|
|
|
|||||
C6H5 |
|
C |
|
C6H5 |
C6H5 |
|
C |
|
CH2CH2CH3 |
||
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|||
|
|
O |
|
|
O |
||||||
Дифенілкетон |
Пропілфеніл- |
||||||||||
(бензофенон) |
|
|
|
кетон |
|||||||
Реакції нуклеофільного приєднання (АN)
Альдегіди та кетони, завдяки електрофільному центру, здатні вступати у взаємодію з нуклеофільними реагентами. Для оксосполук найбільш характерні реакції, що перебігають за механізмом нуклеофільного приєднання, їх позначають сим-
волом AN (від англ. addition nucleophilic). Залеж-
но від характеру нуклеофільного реагенту, що приєднується по подвійному зв’язку С=О, альдегіди і кетони перетворюються на різноманітні сполуки.
22

Нуклеофіл N атакує електрофільний центр молекули оксосполуки — атом Карбону карбонільної групи — і приєднується до нього за рахунок своєї пари електронів. Водночас відбувається гетеролітичний розрив π -зв’язку С=О, і пара електронів, що утворювала цей зв’язок, переходить до атома Оксигену, створюючи на ньому негативний заряд. Таким чином, у результаті приєднання нуклеофільного реагенту оксосполука перетворюється на алкоксидіон. Ця стадія реакції перебігає повільно.
Алкоксидіон є сильною основою. Тому він легко взаємодіє з будь-якою, навіть слабкою, кислотою (наприклад з молекулою води). Друга стадія реакції, що перебігає швидко, полягає в стабілізації алкоксидіона шляхом приєднання протона із середовища. У результаті реакції атом Карбону оксогрупи переходить із sp2- в sp3-гіб- ридний стан.
Реакцію нуклеофільного приєднання можна представити в загальному вигляді такою схемою:
δ + δ - |
|
|
|
|
|
|
|
|
|
|
|
|
OH |
Реакція нуклеофільного |
|||||
C |
|
|
O + H+X - |
|
|
|
|
|
|
|
C |
||||||||
|
|
|
|
|
|
|
|
|
приєднання |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
X |
|
δ + δ - |
повільно |
|
|
|
|
|
O- |
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
C |
|
|
O + X- |
|
|
|
|
|
|
C |
|
|
X- — нуклеофіл |
||||||
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
X |
|
|
|
|
|||
|
|
|
|
|
|
|
швидко |
|
|
|
|
|
|
|
|
||||
C |
|
|
O- + H+ |
|
|
|
C |
|
|
OH |
Продукт приєднання |
||||||||
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
X |
|
|
|
|
|
|
|
|
|
|
X |
|
|
|
|
||||
Атака нуклеофіла перебігає тим легше, чим більша величина часткового позитивного заряду на атомі Карбону. Істотний вплив на величину δ + чинять вуглеводні радикали і замісники в них. Оскільки алкільні радикали виявляють +І- ефект, тобто є електронодонорами, то аліфатичні альдегіди практично завжди більш активні в реакціях нуклеофільного приєднання, ніж аліфатичні кетони, які мають два вуглеводневих радикали. Електроноакцепторні замісники підсилюють електрофільність атома Карбону, отже, підвищують реакційну здатність оксосполуки. Електронодонорні замісники, навпаки, знижують її:
АЛЬДЕГІДИ
|
|||||||||||||||||||
|
|
CI |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
δ + O |
|
|
|
|
δ '+ O |
|
|
δ ''+ O |
||||||
|
|
|
|
|
|
|
|
|
|
||||||||||
CI |
|
C |
|
C |
|
|
H |
|
C |
CH3 |
|
C |
|||||||
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
H |
|
|
|
|
|
H |
|
|
|
|
H |
||
|
|
CI |
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
Трихлоретаналь |
|
|
Метаналь |
|
|
Етаналь |
|||||||||||||
|
|
|
|
|
|
|
|
|
КЕТОНИ |
|
|
|
|
|
|||||
|
|
||||||||||||||||||
|
|
|
CH3 |
δ '''+ |
|
|
CH3 |
|
|
CH2 |
δ ''''+ |
||||||||
|
|
|
|
|
|
||||||||||||||
|
|
|
|
||||||||||||||||
|
C |
|
O |
|
C |
|
O |
||||||||||||
|
|
|
|
||||||||||||||||
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
Пропанон |
|
|
|
|
|
Бутанон |
||||||||||
|
|
|
δ + |
δ′ + |
δ′′ + δ′′′ + δ′′′′ + |
||||||||||||||
Зменшення реакційної здатності оксосполук
В ароматичних альдегідах і кетонах карбонільна група перебуває в сполученні з бензеновим кільцем, виявляючи –I- і –Мефекти. Вона відтягує на себе електронну щільність бензенового кільця, що приводить до зниження величини δ + на атомі Карбону карбонільної групи. Цим пояснюється нижча реакційна здатність ароматичних оксосполук порівняно з аліфатичними. Ароматичні альдегіди, як правило, більш реакційноздатні, ніж змішані й тим більше ароматичні кетони.
Oδ + |
Oδ '+ |
Oδ ''+ |
C H |
C CH3 |
C |
Бензальдегід |
Оцетфенон |
Бензофенон |
|
δ + δ′ + δ′′ + |
|
Зменшення реакційної здатності оксосполук
До найважливіших реакцій нуклеофільного приєднання належать реакції оксосполук із ціанідами, водою та спиртами, аміаком і амінами,
атакож із деякими іншими реагентами.
1.Взаємодія з ціанідами металів. При взає-
модії оксосполук із солями ціановодневої кислоти (ціанідами) утворюються гідроксинітрили.
Гідроксинітрили — це сполуки, які містять у молекулі гідроксильну групу та ціаногрупу.
Сама ціановоднева кислота HCN мало дисоційована. Тому реакцію проводять у лужному середовищі, де утворюється ціанідіон, що є активною нуклеофільною частинкою.
Нуклеофіл
|
|
|
|
|
|
|
|
|
|
CN |
|
|
|
|
|
|
|
|
|||
|
|
|
|
O |
|
|
|
H2O |
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
- |
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
CH3 |
|
C |
+ -CN |
|
|
CH3 |
|
C |
|
O |
|
- OH - |
|
CH3 |
|
|
|
CHCN |
|||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
H |
|
|
|
|
|
|
H |
|
|
|
|
|
OH |
||||||
Ацет |
Ціанід |
|
|
|
|
|
|
|
|
|
2-Гідрокси- |
||||||||||
альдегід |
-іон |
|
|
|
|
|
|
|
|
пропанонітрил |
|||||||||||
За допомогою цієї реакції можна подовжити вуглецевий ланцюг вихідної сполуки на один атом Карбону; продукти реакції — гідроксинітрили — служать вихідними сполуками для синтезу гідроксикарбонових кислот.
2. Взаємодія з водою. Альдегіди й у значно меншому ступені кетони оборотно приєднують воду, утворюючи гідрати:
|
O |
|
|
|
|
|
|
OH |
|||
|
|
|
|
|
|
|
|
|
|
|
|
CH C |
+ H O |
|
|
|
CH |
|
|
C |
|
OH |
|
|
|
|
|
|
|
||||||
3 |
2 |
|
|
|
|
3 |
|
|
|
|
|
|
H |
|
|
|
|
|
|
H |
|||
|
|
|
|
|
|
|
|
||||
Ацетальдегід |
|
|
Гідрат ацетальдегіду |
||||||||
Стан рівноваги у цій реакції залежить від реакційної здатності карбонільної сполуки. Формальдегід у водному розчині гідратований на 100 %, ацетальдегід — на 51 %, у водному розчині ацетону гідратна форма практично відсутня. Галогеновані в α -положенні альдегіди і кетони, у яких більший частковий позитивний заряд
23