Материал: Біологічна та біоорганічна хімія_Мардашко О.О._ изд. 2008-342 с._ОНМедУ-2012

Таблиця 1.1. Функціональні групи та класи
|
|
|
|
|
|
Функціональна |
|
Загальна |
|||
|
|
|
|
|
|
Клас |
формула |
||||
|
|
|
|
|
|
|
|
|
група |
||
|
|
|
|
|
|
|
|
|
|
класу |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
–F, –CI, –Br, –I |
Галогенопохідні |
R–HaI |
|||||||||
–(Hal) — галогени |
|
|
|||||||||
–ОН — гідроксильна |
Спирти, феноли |
R–OH |
|||||||||
–OR — алкоксильна |
Прості ефіри |
R–OR |
|||||||||
–SH — тіольна |
Тіоли |
R–SH |
|||||||||
|
|
|
|
|
|
|
|
|
|
(меркаптани) |
|
–NH2 — аміно- |
Аміни |
R–NH2 |
|||||||||
|
|
|
|
|
|
|
O |
— нітро- |
Нітросполуки |
R–NO2 |
|
|
|
|
|
|
N |
|
O |
||||
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
O — карбонільна |
Альдегіди, |
R–CH=O |
|||||
|
|
|
|
|
|
|
|
|
|
кетони |
|
|
|
|
C |
O |
— карбо- |
Карбонові |
R–CO–R′ |
||||
|
|
|
OH |
ксильна |
кислоти |
|
|||||
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH — сульфо- |
Сульфокислоти |
R–SO3H |
|
|
|
|
|
|
S |
|
|
||||
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
вуглеводнів, отримані введенням у них функціональних груп.
Функціональна група — це атом або група атомів невуглецевого характеру, які визначають приналежність сполуки до певного класу
(табл. 1.1).
Ознакою, за якою органічні сполуки належать до тих чи інших класів, є природа функціональної групи. Наприклад, якщо в етані СН3–СН3, що належить до класу вуглеводнів, замінити один з атомів Гідрогену на гідроксильну групу ОН, то отримана сполука етанол СН3–СН2ОН належатиме до класу спиртів; якщо ж в етан ввести замість атома Гідрогену атом Хлору, то отримана сполука хлоретан СН3–СН3Сl належатиме до класу галогенопохідних.
Сполуки можуть містити не одну, а кілька функціональних груп. Якщо ці групи однакові, то сполуки називаються поліфункціональними (наприклад, хлороформ, гліцерин). Сполуки, що містять різні функціональні групи, називаються
гетерофункціональними. Їх можна одночасно віднести до кількох класів (наприклад, молочну кислоту можна розглядати як кислоту і як спирт, а коламін — як амін і як спирт).
CHCl3 |
CH |
|
CH |
|
CH |
||||||
|
|
||||||||||
|
|
|
2 |
|
|
|
|
|
|
|
2 |
|
|
|
|||||||||
|
OH |
|
OH OH |
||||||||
Хлороформ |
|
|
Гліцерин |
||||||||
CH3 CH COOH |
H2NCH2 |
|
CH2OH |
||||||||
|
|||||||||||
OH |
|
|
|
|
|
|
|
|
|
|
|
Молочна кислота |
|
|
Коламін |
||||||||
Номенклатура, або спосіб найменування сполук, є «хімічною мовою», що служить для передачі будови сполук. Першими в органічній хімії з’явилися тривіальні (від лат. trivialis — звичайний) назви. Їх давали речовинам, структура
яких навіть не була відома. Тривіальні назви вказували або на джерело їхнього виділення (так, сечовина вперше була виявлена в сечі), або на деякі помітні властивості (наприклад, назви речовин гліцерин, глюкоза, гліцин пов’язані з їхнім солодким смаком (від грецьк. glykys — солодкий). Тривіальні назви поширені серед природних сполук — амінокислот, вуглеводів, алкалоїдів, стероїдів. Ці назви зручні своєю лаконічністю, але вони не можуть бути об’єднані в систему.
Сучасна номенклатура має бути систематичною та міжнародною, щоб фахівці всього світу могли відобразити в назві структуру сполуки й, навпаки, за назвою однозначно уявити структуру. До того ж, сучасна номенклатура має бути придатною для комп’ютерної обробки. Сьогодні визнана систематична номенклатура ІЮПАК (IUPAC — Міжнародна спілка теоретичної та прикладної хімії). Щоправда, для складних за структурою сполук систематичні назви бувають іноді занадто громіздкими, тому для зручності в систематичній номенклатурі допускається вживання деяких найбільш усталених тривіальних назв. Номенклатурні правила ІЮПАК видані англійською мовою. При перекладі на українську мову вони адаптовані з урахуванням її особливостей та традицій української термінології.
Серед варіантів систематичних номенклатур, рекомендованих ІЮПАК, найпоширенішою є
замісна номенклатура. Сама назва номенклату-
ри показує, що в сполуці виділяється якась основа, у якій зроблене заміщення атомів Гідрогену на інші атоми або групи. У систематичній номенклатурі ІЮПАК використовують кілька найважливіших номенклатурних термінів: родоначальна структура, замісник, характеристична група.
Родоначальна структура — це структура, що лежить в основі названої сполуки. Для ациклічних сполук за родоначальну структуру приймається головний вуглецевий ланцюг, а для карбоциклічних і гетероциклічних — цикл.
Назви головних вуглецевих ланцюгів або циклів формуються на основі номенклатури вуглеводнів. Так, у молекулі спирту CH3CH2CH2OH головний вуглецевий ланцюг складається з трьох атомів Карбону, і відповідно родоначальна структура називатиметься «пропан», а в молекулі кислоти СН3СООН головний вуглецевий ланцюг складається з двох атомів Карбону, тому назва родоначальної структури — «етан». Втім, для зазначеної кислоти допустима і тривіальна назва «оцтова кислота».
Замісник — це будь-який атом або група атомів, що заміщають атом Гідрогену в родоначальній структурі.
Характеристична група — це функціональна група, пов’язана з родоначальною структурою.
Замісниками у родоначальній структурі можуть бути як функціональні групи (див. табл. 1.1), так і вуглеводневі радикали. Вуглеводневі радикали — це залишки вуглеводнів, які містять на один атом Гідрогену менше. Назви радикалів походять від назв відповідних вуглеводнів шля-
9
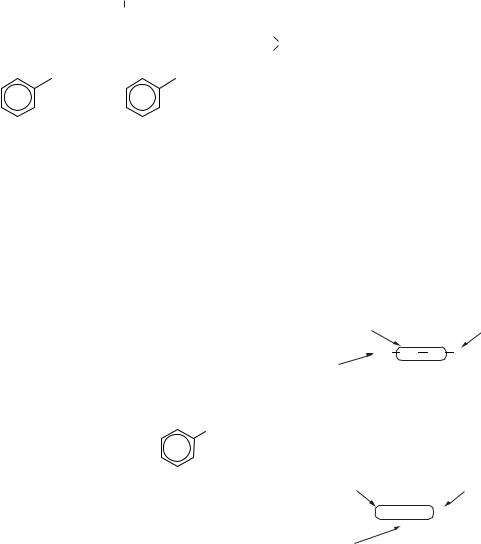
хом заміни суфіксу -ан на -іл, наприклад, метил
— СН3–, етил — СН3СН2–. Однак із пропану утвориться вже два радикали: пропіл та ізопропіл. Слід звернути увагу, що радикал С6Н5–, утворений з бензену, називається феніл, а не бензил. Бензильним називається радикал С6Н5СН2–, утворений з толуену (толуолу).
|
CH3 |
CH– |
CH3CH2CH2– |
CH3 або (CH3)2CH– |
|
Пропіл |
|
Ізопропіл |
|
|
CH2– |
Фенол Бензил
Як утворюється систематична назва сполуки? У замісній номенклатурі — це складне слово, яке містить назву родоначальної структури. Назви замісників позначаються префіксами (приставками) і суфіксами.
Для побудови назви, в першу чергу, визначають тип характеристичної групи (якщо вона наявна). Коли характеристичних груп у сполуці кілька, то виділяють старшу з них. Для характеристичних груп прийнято порядок по убуванню старшинства. Потім визначають родоначальну структуру, до якої обов’язково входить старша характеристична група. Деякі характеристичні групи, а саме: галогени, нітро- і алкоксигрупи, відображуються в загальній назві тільки у вигляді префіксів, наприклад, бромметан, етоксіетан, нітробензен.
NO2
CH3Br– CH3CH2OCH2CH3
Бромметан Етоксіетан Нітробензен
Більшість характеристичних груп може входити до загальної назви у вигляді як суфікса, так і префікса. Старша характеристична група відображується суфіксом, решта (нестарші) — префіксами. Якщо сполука монофункціональна, то характеристична група, для якої передбачений суфікс, завжди виконує роль старшої, вона відображується в назві суфіксом (наприклад, пропанол СН3СН2СН2ОН, етанова кислота СН3СООН) (табл. 1.2).
У гетерофункціональних сполуках тільки одна з характеристичних груп — старша — позначається суфіксом. Всі інші замісники позначаються префіксами та наводяться за алфавітом. При цьому потрібно вказати місце розташування замісників у вуглецевому ланцюзі. Для цього слід попередньо провести нумерацію атомів родоначальної структури. Вуглецевий ланцюг нумерується з одного з її кінців так, щоб старша характеристична група дістала найменший номер. Цифри, які вказують положення замісників, став-
Таблиця 1.2
Префікси та суфікси для позначення деяких характеристичних груп
Характерис- |
Префікс |
Суфікс |
|
тична група |
|||
|
|
||
|
|
|
|
–(С)ООН |
– |
-ова кислота |
|
–СООН |
Карбокси- |
-карбонова кислота |
|
–SO3H |
Сульфо- |
-сульфокислота |
|
–(C)H=O |
Окси- |
-аль |
|
–CH=O |
Форміл- |
-карбальдегід |
|
C=O |
Оксо- |
-он |
|
–OH |
Гідрокси- |
-ол |
|
–SH |
Меркапто- |
-тіол |
|
–NH2 |
Аміно- |
-амін |
|
–NO2 |
Нітро- |
– |
|
–OR |
Алкокси- |
– |
|
F, Cl, Br, I |
Фтор-, хлор-, |
|
|
(Hal) |
бром, йод |
– |
|
|
(галоген-) |
|
|
|
|
|
лять перед префіксами та після суфікса. Цифри від букв відділяються дефісами (рисками), а цифри від цифр — комами.
Так, коламін має систематичну назву 2-амі- ноетанол, а не 2-гідроксіетанамін, оскільки гідроксильна група старша за аміногрупу:
Родоначальна |
Старша характери- |
структура: етан |
стична група: -ол |
2 1
H2N CH2 CH2 OH
Нестарша характерис- 2-Аміноетанол (триві-
тична група: альна назва — коламін) аміно-
З цієї же причини систематична назва молочної кислоти — 2-гідроксипропанова кислота. Тут карбоксильна група старша за гідроксильну:
Родоначальна |
|
|
|
|
|
|
|
|
Старша характе- |
структура: |
|
|
|
|
|
|
|
|
ристична група: |
пропан |
3 |
2 |
|
1 |
1 |
|
-ова кислота |
||
|
|
|
|
|
|
|
|
||
Нестарша ха- |
CH3 |
|
|
CH |
|
COOH |
|
||
|
|
|
|||||||
|
|
|
|
||||||
|
|
|
OH |
|
|
|
|
||
рактеристична |
2-Оксипропанова кислота (триві- |
||||||||
група: окси- |
альна назва — молочна кислота) |
||||||||
Для закінчень -ова кислота й -аль немає необхідності вказувати положення функціональної групи (в атома С-1), тому що вони завжди розміщуються на початку ланцюга. Дуже часто опускається й цифровий показник для закінчення -ол, якщо група ОН перебуває в крайнього атома Карбону (наприклад пропанол СН3СН2СН2ОН), хоча коректніша назва цього спирту — пропанол-1 (щоб відрізнити його від ізомеру — пропанолу-2).
За наявності двох, трьох, чотирьох і т. д. однакових замісників або кратних зв’язків використовують помножувальні префікси ди-, три-, тетра- і т. д., наприклад етанол-1,2, трихлоретаналь.
HOCH2CH2OH |
Cl3C–CH=O |
Етандіол-1,2 (тривіальна |
Трихлоретаналь (триві- |
назва — етиленгліколь) |
альна назва — хлораль) |
10
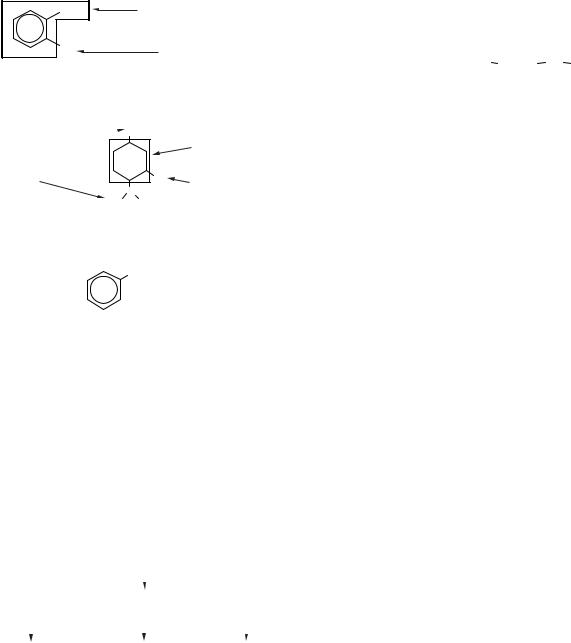
Для трихлоретаналю вказувати положення атомів Хлору не потрібно, тому що при розташуванні одного з атомів Хлору при атомі С-1 сполука вже не міститиме характеристичної групи
–СН=О, тобто не належатиме до класу альдегідів. У карбоциклічних сполуках нумерацію починають від того атома Карбону, при якому перебуває старша характеристична група. Якщо при цьому неможливо застосувати однозначну нумерацію, то цикл нумерують так, щоб замісники мали найменші номери. Розглянемо назви циклічних структур на прикладах ментолу та
саліцилової кислоти.
|
|
|
|
|
Родоначальна структура |
|
6 |
|
COOH |
|
|
із старшою характерис- |
|
|
|
|
тичною групою: бензойна |
|||
5 |
1 |
|
|
|||
|
|
|
|
|
кислота |
|
|
|
|
|
|
|
|
4 |
2 |
|
|
|
|
|
3 |
OH |
|
|
|
Нестарша характе- |
|
|
|
|
|
|
|
ристична група |
2-Оксибензенова кислота (тривіальна |
||||||
|
назва — саліцилова кислота) |
|||||
|
|
|
|
CH3 |
Родоначальна струк- |
|
|
|
|
|
тура: циклогексан |
||
Вуглеводневі ра- |
|
5 |
|
|||
4 |
6 |
|
||||
дикали: ізопропіл, |
|
|
||||
3 |
|
1 |
|
|||
метил |
|
2 |
|
|||
|
|
OH |
||||
|
|
|
|
CH |
Характеристична |
|
|
|
|
H3C |
|
CH3 |
група: -ол |
|
2-Ізопропіл-5-метилциклогексанол |
|||||
|
(тривіальна назва — ментол) |
|||||
|
|
|
|
CH2COOH |
||
Фенілоцтова (або фенілетанова) кислота
У разі наявності в структурі сполуки одночасно відкритого ланцюга та циклу за родоначальну структуру приймається та, де міститься характеристична група (або старша з них). Наприклад, у фенілоцтовій кислоті родоначальною структурою вважається ланцюг із двох атомів Карбону, тому що в ній міститься карбоксильна група.
Таким чином, загальне правило складання повної назви сполуки можна представити у вигляді такої схеми:
|
|
|
Назва сполуки |
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Префікси |
|
Родоначальна |
Суфікс |
|||||
|
структура |
|||||||
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Вуглеводневі |
|
Головний лан- |
|
Тільки |
||||
радикали та |
|
цюг, основна цик- |
|
старша |
||||
нестарші |
|
лічна або гетеро- |
|
характе- |
||||
характеристичні |
|
циклічна |
|
ристична |
||||
групи |
|
структура |
|
група |
||||
|
|
|
|
|
|
|
|
|
Зворотне завдання — написання структури за систематичною назвою — є зазвичай простішим. Спочатку зображують родоначальну структуру — відкритий ланцюг або цикл, потім нумерують атоми Карбону і розставляють замісники. На закінчення дописують атоми Гідрогену таким чином, щоб кожний атом Карбону мав валентність чотири.
Розглянемо це на прикладі побудови формули 2-амінопентандіової кислоти (тривіальна назва — глутамінова кислота).
Головний вуглецевий |
1 |
2 |
3 |
4 |
5 |
||||||||
ланцюг і нумерація |
|
C—C—C—C—C |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Розташування замісників |
1 |
2 |
|
3 |
|
4 |
|
5 |
|||||
(дві групи СООН) і |
HOOC |
|
|
C |
|
C |
|
C |
|
COOH |
|||
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
група NH2 у атома С-2 |
|
|
|
|
|
NH2 |
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Доповнення атомами |
HOOC CH |
|
|
|
CH2 |
CH2 |
COOH |
||||||
|
|
||||||||||||
Гідрогену |
|
|
|
|
|
|
|
||||||
NH2 |
|
|
|
|
|
||||||||
Цілком очевидно, що уявити структуру тільки за тривіальною назвою — завдання дуже складне.
Крім замісної номенклатури інколи викорис-
товується радикально-функціональна номенкла-
тура, що є також варіантом систематичної номенклатури ІЮПАК. Частіше вона застосовується для галогенопохідних, спиртів, амінів і простих ефірів. Для деяких класів сполук, наприклад, карбонових кислот і альдегідів, ця номенклатура незастосовна.
Назва сполуки за радикально-функціональ- ною номенклатурою складається з двох елементів
— назви вуглецевого радикала та назви характеристичної (функціональної) групи або відповідного класу сполук. Нижче наведено приклади назв за радикально-функціональною номенклатурою.
CH3l |
CH3CH2CH2OH |
Метилйодид |
Пропіловий спирт |
CH3CH2OCH2CH3 |
CH3CH2NH2 |
Діетиловий спирт |
Етиламін |
Теорія будови органічних сполук
О. М. Бутлерову вдалося створити логічно завершену теорію будови органічних сполук, яка і донині є науковою основою органічної хімії. Ця теорія базується на матеріалістичному підході до реальної молекули і виходить із можливості пізнання її будови експериментальним шляхом. О. М. Бутлеров при встановленні будови речовин надавав основного значення хімічним реакціям. Теорія будови О. М. Бутлерова не тільки пояснювала вже відомі факти, її наукове значення полягало в прогнозуванні існування нових органічних сполук.
11

Основні положення теорії будови органічних сполук:
1)атоми в молекулах з’єднані між собою хімічними зв’язками відповідно до їх валентності;
2)атоми в молекулах органічних речовин з’єднуються між собою в певній послідовності, що визначає хімічну будову молекули;
3)властивості органічних сполук залежать не тільки від кількості та природи атомів, що входять до їх складу, але й від хімічної будови молекул;
4)у молекулах існує взаємний вплив атомів
—як зв’язаних, так і безпосередньо не зв’язаних між собою;
5)хімічну будову речовини можна визначити в результаті вивчення її хімічних перетворень і, навпаки, за будовою речовини можна охарактеризувати її властивості.
Важливим наслідком теорії будови був висновок, що кожна органічна сполука повинна мати одну хімічну формулу, яка відображає її будову. Для зображення будови органічних сполук використовують формули будови (структурні формули).
Структурна (графічна) формула — це зобра-
ження послідовності зв’язків атомів у молекулі. У структурних формулах органічних сполук кожний хімічний зв’язок позначається рискою між хімічними символами атомів, що зв’язуються. Наприклад, для метилового спирту (метанол) можна представити лише одну можливу послідовність зв’язків з урахуванням валентності атомів, що зв’язуються, у вигляді такої формули:
H
H C O H
H
Метанол (або скорочено — СH3OH)
Для спрощення формул і прискорення їхнього написання зв’язки (риски) між атомами Карбону та Гідрогену звичайно опускаються і символи атомів Гідрогену пишуться разом із символами атомів Карбону, з якими вони зв’язані.
Якщо для сполуки CH4O можливий єдиний варіант послідовності зв’язку атомів, то для сполуки С2Н6О таких варіантів може бути два. Інакше кажучи, одному хімічному складу відповідатимуть дві різні органічні сполуки, що відрізняються будовою, тобто послідовністю зв’язку атомів. Такими сполуками будуть етиловий спирт (рідка речовина) і диметиловий ефір (газоподібна речовина), що відрізняються фізичними й хімічними властивостями.
|
|
H |
|
H |
|
|
H |
|
|
|
H |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
C |
|
C |
|
O |
|
H |
H |
|
C |
|
O |
|
C |
|
H |
||||
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
H |
|
|
H |
|
|
|
H |
||||||||||
СH3СH2OH |
СH3OСH3 |
||||||||||||||||||||
Етиловий спирт |
Диметиловий ефір |
||||||||||||||||||||
(т. кип. — 78 °С) |
(т. кип. — 24 °С) |
||||||||||||||||||||
На цьому прикладі можна легко переконатися в прояві дії одного з основних положень теорії будови — залежності властивостей речовин не тільки від складу сполуки, але й від будови молекул. Цей приклад ілюструє сутність властиво-
го органічним сполукам найважливішого явища
— ізомерії, тобто можливості існування кількох речовин із різними властивостями, які мають при цьому той самий склад та однакову молекулярну масу. Явище ізомерії відоме давно (1830), але воно не могло бути пояснене на той час жодною з існуючих теорій. Тільки теорія будови О. М. Бутлерова дала явищу ізомерії просте та вичерпне пояснення. Крім того, теорія будови змогла відповісти на питання, чому в ізомерів при зміні будови відбувається зміна хімічних властивостей. Це пояснюється тим, що зміна будови, тобто послідовності зв’язування атомів, позначається переважно на зміні характеру взаємного впливу атомів у молекулі.
Вчення про взаємний вплив атомів у молекулі в подальшому було розвинене учнем О. М. Бутлерова — В. В. Марковніковим. Воно активно розвивалося, сповнювалося новим змістом, і в сучасній органічній хімії питання взаємного впливу атомів у молекулі є центральними при розв’я- занні найважливіших проблем, пов’язаних з оцінкою реакційної здатності органічних сполук.
Ізомерія органічних сполук
Важливий вплив на реакційну здатність сполук чинить їх будова. Ще Берцеліус (1830) запропонував новий термін «ізомерія» для сполук, які за однакового хімічного складу й однакової молекулярної маси виявляли різні властивості. Грунтовніше розуміння структури ізомерних сполук належить О. М. Бутлерову, який сформулював основні принципи сучасної структурної теорії (1861).
Ізомери — це хімічні сполуки ідентичних молекулярних мас і однакового складу, але різної будови, що визначає їх різні фізико-хімічні властивості.
У 70-х роках ХІХ ст. теорія будови доповнилася теорією просторового розміщення атомів у молекулі — стереохімічною теорією (ВантГофф, Ле Бель).
Всі ізомери поділяються на два великі класи —
структурні та просторові (рис. 1.1).
|
|
|
|
|
|
|
|
|
|
Ізомери |
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Структурні |
|
|
|
|
|
|
|
|
Стереоізомери |
|
||||||||||||
|
|
ізомери |
|
|
|
|
|
|
(просторові ізомери) |
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Ізомери |
|
|
|
Ізомери |
|
|
|
Конфор- |
|
Конфігу- |
||||||||||||||
вуглецево- |
|
|
поло- |
|
|
|
маційні |
|
раційні |
|||||||||||||||
го скелета |
|
|
ження |
|
|
|
ізомери |
|
ізомери |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
кратних |
|
|
положен- |
|
|
|
Цис-, транс-, |
|
|
Оптичні |
||||||||||||||
|
ня гетеро- |
|
|
|
|
|
||||||||||||||||||
зв’язків |
|
|
|
атома |
|
|
|
син-, анти- |
|
|
ізомери, |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
(геомет |
|
енантіомери, |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ричні |
|
|
діастерео- |
||||||
|
|
|
|
|
|
|
функціо- |
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
ізомери) |
|
|
мери |
||||||||||||
|
|
|
|
|
|
|
нальних |
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
груп |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
Рис. 1.1. Класифікація ізомерів |
|||||||||||||||||||
12
Структурними називаються ізомери з різним |
|
|
|
|
С3Н6О |
|
|
|
|
|
|
|||||||||
порядком сполучення атомів. |
|
|
|
|
|
|
|
|||||||||||||
Просторовіізомери відрізняються положенням |
CH3 CH2 C O |
|
|
O |
||||||||||||||||
атомів у просторі при однаковому порядку їх спо- |
|
|
|
|
|
CH3 |
|
|
|
|
CH3 |
|||||||||
|
|
|
|
H |
|
C |
|
|||||||||||||
|
|
|
|
|
|
|||||||||||||||
лучення. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
І. Структурна ізомерія |
|
|
|
|
|
|
Пропаналь (альдегід) |
Пропанон (кетон) |
||||||||||||
Причини утворення структурних ізомерів |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||
поділяють таким чином: |
|
|
|
|
|
|
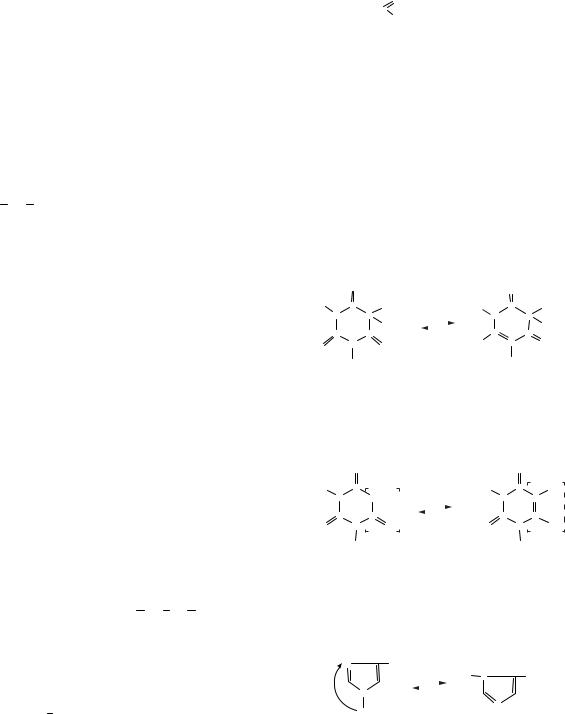
Особливим випадком ізомерії між класами є |
|||||||||||||
1. Ізомерія ланцюга (вуглецевого скелета) по- |
таутомерія (динамічна ізомерія). Це явище по- |
|||||||||||||||||||
лягає в тому, що речовини одного складу розріз- |
лягає в тому, що два або кілька структурних |
|||||||||||||||||||
няються порядком зв’язку атомів, які утворюють |
ізомерів за певних умов легко взаємно перехо- |
|||||||||||||||||||
скелет молекули. |
|
|
|
|
|
|
дять з переносом будь-якої рухливої групи та |
|||||||||||||
Найчастіше це спостерігається у вуглеводнів |
відповідним перерозподілом електронної щіль- |
|||||||||||||||||||
із відкритим ланцюгом, якщо n≥ 4: |
|
|
|
|
|
ності. |
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
Таутомерія, пов’язана з перенесенням атома |
|||||||||||
|
|
|
|
|
|
CH3 |
|
Гідрогену (або протона), є прототропною тау- |
||||||||||||
CH3 CH2 CH2 CH3 |
1 |
2 |
|
|
3 |
томерією. Вона спостерігається для сполук із |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
CH3 |
|
|
CH |
|
CH3 |
відкритим ланцюгом і циклічних. |
|||||||||||
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||
н-Бутан 2-Метилпропан
Кількість ізомерів такого типу дуже швидко збільшується зі зростанням кількості n атомів Карбону.
n |
Кількість ізомерів |
4 |
2 |
5 |
3 |
6 |
5 |
7 |
9 |
15 |
4347 |
2. Ізомерія положення:
а) Ізомерія положення функціональних груп зумовлена тим, що при одному вуглецевому скелеті функціональна група зв’язана з різними вуглецевими атомами Карбону:
|
|
Cl |
|
3 |
2 |
1 |
||||
1 |
2 |
|
|
3 |
CH3 |
|
CH2 |
|
CH2Cl |
|
CH3 |
|
|
CH |
|
CH3 |
|
|
|||
|
|
|||||||||
Кільцево-ланцюгова прототропна таутомерія
а) лактимлактамна:
|
O |
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
C |
C2H5 |
|
|
Н |
|
|
|
C |
C2H5 |
|
|
|
|
|
|
|
||||||
|
N |
C |
|
|
|
N |
C |
||||
|
|
C2H5 |
|
|
|
|
|
|
|
|
C2H5 |
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|||
|
C |
C |
|
|
HO |
C |
C |
||||
O |
N |
O |
|
|
|
|
|
N |
O |
||
H |
|
|
|
|
|
|
H |
|
|||
|
|
|
|
|
|
|
|
|
|
||
Лактамна форма |
|
|
Лактимна форма |
||||||||
Люмінал (фенобарбітал)
б) кето-енольна:
|
O |
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
H |
C |
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
H |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
N |
|
CH2 |
|
|
|
|
|
N |
|
C |
||||||||
|
|
|
|
|
||||||||||||||
C |
|
C |
|
|
|
|
C |
|
C |
|||||||||
|
|
|
|
|
||||||||||||||
O |
N |
|
|
O |
|
|
|
|
O |
N |
|
|
OH |
|||||
|
H |
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
2-Хлорпропан 1-Хлорпропан
CH3 |
|
|
CH |
|
CH2CI |
|
|
||||
|
|
|
|
|
H2N CH2 CH2 COOH |
|
|
|
|
|
|
|
|
NH2 |
|||
α -Аланін β -Аланін
б) Ізомерія положення кратних зв’язків:
4 |
3 |
2 |
1 |
4 |
3 |
2 |
1 |
1 |
|||||
CH3 |
|
CH2 |
C |
|
CH |
CH3 |
|
C |
|
C |
|
CH3 |
|
|
|
|
|||||||||||
|
|
|
|
|
|||||||||
|
|
|
|||||||||||
Кето-форма |
Енольна форма |
Барбітурова кислота
в) азольна таутомерія молекули імідазолу:
N 3 |
|
4 |
CH3 |
|
|
|
||||
2 |
1 |
5 |
|
|
|
|
H N |
1 |
5 |
CH3 |
|
|
|
|
|
|
2 |
|
|||
|
N |
|
|
|
|
|
|
4 |
|
|
|
|
|
|
|
|
|
3 |
|
||
N
H
Бутин-1 |
Бутин-2 |
4-Метилімідазол |
5-Метилімідазол |
||||||
в) Ізомерія положення гетероатомів у лан- |
ІІ. Стереоізомерія (просторова ізомерія) тра- |
||||||||
цюзі: молекули однакового атомного складу ма- |
диційно поділяється на конфігураційну та кон- |
||||||||
ють різні функціональні групи (належать до |
фірмаційну (див. рис. 1.1). |
|
|||||||
різних класів): |
|
|
|
|
|
1. Конфігураційна ізомерія поділяється на гео- |
|||
|
|
|
С2Н6О |
метричну (цис-, транс-) та оптичну ізомерію. |
|||||
|
Розташування атомів відносно певних пло- |
||||||||
CH3 |
|
CH2OH |
CH3 |
|
O |
|
CH3 |
щин, які проходять через певні зв’язки, назива- |
|
|
|
|
|||||||
Етанол |
Диметиловий ефір |
ють конфігурацією молекули. |
|||||||
а) Цис-, транс-ізомерія алкенів зумовлена на- |
|||||||||
(спирт) |
(простий ефір) |
явністю в молекулі подвійного зв’язку (π -зв’язку) |
|||||||
13