Материал: Біологічна та біоорганічна хімія_Мардашко О.О._ изд. 2008-342 с._ОНМедУ-2012
та різним положенням замісників відносно площини π -зв’язку. Більшість алкенів можуть існувати у вигляді цис- і транс-ізомерів.
Наприклад, бутендіова кислота
HOOC CH CH COOH
CH COOH
відома у двох формах цис- і транс-:
H |
|
|
C |
|
COOH |
H |
|
C |
|
COOH |
|||
|
|
|
|
|
|||||||||
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
COOH |
HOOC |
|
C |
|
|
H |
|||
|
|
|
|
|
|||||||||
цис-форма |
транс-форма |
||||||||||||
Малеїнова кислота |
Фумарова кислота |
||||||||||||
У цис-ізомері (малеїнова кислота) два об’ємних замісники — карбоксильні групи (-СООН)
—розташовані по один бік площини π -зв’язку,
а у транс-ізомері (фумарова кислота) ці замісники розташовані по різні боки площини π - зв’язку.
Фотоізомеризація цис-, транс-алкенів має важливе фізіологічне значення. Порушення світлового перетворення фумарової кислоти на малеїнову при дефіциті ферментів спричинює важко виліковне шкірне захворювання — псоріаз.
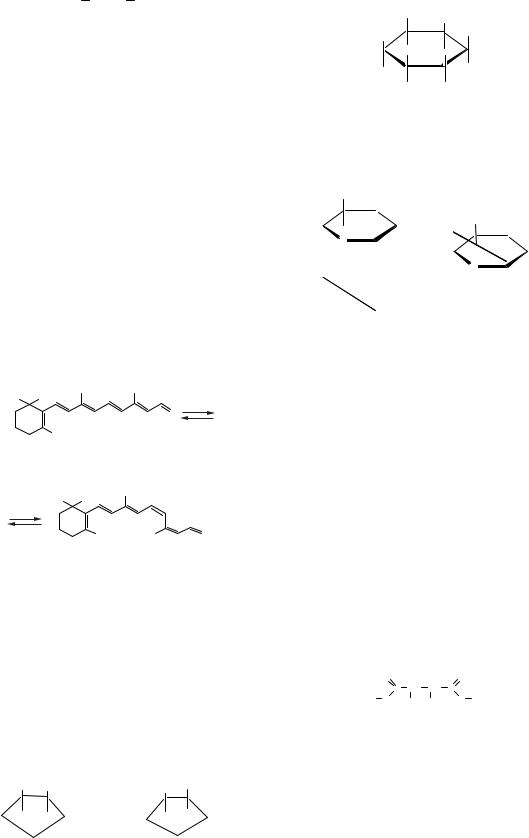
Цис-, транс-фотоізомерія лежить в основі фоторецепції. Одного кванту видимого світла достатньо для того, щоб молекула транс-ретиналю
—сполуки, яка знаходиться у зоровому рецепторі, перетворилася на цис-ретиналь.
CH3 |
CH3 |
H3C CH3 |
|
O
CH3
Транс-ретиналь
H3C CH3 CH3
СН3 |
H3C |
O |
|
Цис-ретиналь
Це, в свою чергу, зумовлює каскад послідовних біохімічних перетворень, у результаті чого формується відповідний нервовий імпульс.
Для циклоалканів характерна просторова ізомерія, пов’язана з різним розташуванням замісників відносно площини циклу. При їхньому розміщенні по одну сторону площини циклу утворюється цис-ізомер; при розміщенні по різні сторони площини циклу — транс-ізомер.
Цис- і транс-ізомери циклоалканів — це самостійно існуючі сполуки. Вони не можуть взаємно перетворюватися, бо для такого перетворення був би необхідний розрив кільця.
CH3 CH3 |
CH |
|
3 |
CH3
Цис-1,2-диметил- Транс-1,2-диметил- циклогексан циклогексан
Прикладом біохімічно значущого явища цис-, транс-ізомерії циклоалканів є молекула інозиту, що має набір із 8 геометричних ізомерів, однак у природі найбільш розповсюджений один із них — моноінозит.
OH
OH
OH
OH
OH OH
Моноінозит
Молекула кокаїну спричинює у 85 раз сильнішу наркотичну дію, ніж молекула його стереоізомеру — псевдококаїну.
CH3OOC |
|
OCOC6H5 |
|
|
|
|||||||
|
N |
|
|
|
CH3OOC |
|
OCOC6H5 |
|||||
|
|
|
|
|
||||||||
|
|
|
|
|
N |
|
|
|||||
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
||
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
Кокаїн (транс-ізомер) Псевдококаїн (цис-ізомер)
Особливим випадком ізомерії є син-анти-ізо-
мерія, яка аналогічна цис-транс-ізомерії, але по-
в’язана з розміщенням замісників відносно C=N– або –N=N–-зв’язку.
Наприклад, для оксиму бензенового альдегіду відомі дві форми:
|
|
N |
|
|
OH |
|
|
N |
|
|
OH |
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
C6H5 |
|
C |
|
H |
H |
|
C |
|
C6H5 |
||
|
|
|
|
||||||||
анти-форма син-форма
б) Одним із видів просторової ізомерії єоптич-
на ізомерія.
Якщо плоскополяризований промінь світла спрямувати на розчини деяких сполук або на деякі кристали, то після його виходу з розчину площина поляризації може відхилитися вправо або вліво. Сполуки, які відхиляють площину поляри-
зації, дістали назву оптично активних сполук. Луї Пастер, вивчаючи під мікроскопом змішану калійамонійну сіль винно-кам’яної кислоти (1860),
O O
C СН СН C
K O OH OH O NH4
виявив кристали двох типів, які відрізняються між собою тільки розміщенням площин поляризації світла, тобто вони відносяться один до одного як предмет і його відбиття в плоскому дзеркалі. Такі кристали були оптично активними, але відхиляли плоскополяризований промінь у різних напрямках.
ВантГофф і Ле Бель незалежно і майже водночас (1874) виявили, що всі оптично активні речовини відомої будови містять у своїх молекулах
14

хоча б один атом Карбону, зв’язаний з чотирма різними групами. Такі атоми називають хіральними. Оптичну активність має, наприклад, 2-гідроксипропанова (молочна) кислота.
H |
|
|
СН C* |
COOH |
|
3 |
|
|
OH |
|
|
Молочна кислота |
|
|
С* — хіральний атом (від грец. χδιροζ |
(хірос) |
|
—рука).
Більшість оксикислот (молочна, яблучна, вин-
на) мають хіральний атом (Карбону), внаслідок чого для них характерна оптична ізомерія.
За наявності в молекулі хірального атома Карбону можливе існування двох оптичних ізомерів (енантіомерів), що належать до різних генетичних рядів (D- i L-) і співвідносяться між собою як предмет і несумісне з ним дзеркальне відображення.
Е. Фішер (1891) і Розанов (1906) запропонували користуватися як моделями порівняння D (+) і L (–) гліцериновими альдегідами (від лат. dexter
— правий, laevus — лівий).
Амінокислота треонін має два центри хіральності, отже, повинна мати 4 ізомери (22).
|
|
|
|
|
|
|
CH3 |
|
|
* |
CH |
*CH COOH |
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
OH NH2 |
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
Треонін |
|
|
|
|
|
|
|
|
||||
|
COOH |
|
|
|
COOH |
|
COOH |
|
|
COOH |
||||||||||||||
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
||||||||||||||||||
H |
|
|
NH2 |
|
NH2 |
|
|
|
H |
|
|
|
|
NH2 |
|
|
H |
|
H |
|
|
|
NH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HO |
|
H |
|
|
|
2 |
|||
HO |
|
|
H |
|
H |
|
|
|
OH |
|
|
|
|
|
|
H |
|
|
|
OH |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|||||||||||||||||||
|
CH3 |
|
|
|
CH3 |
|
|
|
|
|
|
CH3 |
|
|
CH3 |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
дзеркало |
|
|
|
|
|
|
|
|
|
|
|
дзеркало |
|
|
|
|
|||||
|
І |
|
ІІ |
|
|
|
|
|
|
ІІІ |
|
|
|
IV |
||||||||||
D-треонін L-треонін |
|
|
L-ало-треонін D-ало-треонін |
|||||||||||||||||||||
|
||||||||||||||||||||||||
|
|
Енантіомери |
|
|
|
|
|
|
|
|
|
|
Енантіомери |
|
|
|
|
|||||||
Енантіомери І і ІІ мають однакові фізичні та хімічні властивості, але протилежні знаки обертання площини поляризації світла. Аналогічно енантіомери ІІІ та IV (від. грецьк. allos — інший) відрізняються тільки знаком кута обертання. D-треонін (І) та L-ало-треонін (ІІІ) є парою діа-
стереомерів.
H C O |
|
H |
C O |
|
|||
|
|||
|
|
||
H C* OH |
|
HO |
C* H |
|
|||
CH2OH |
|
|
CH2OH |
|
|
||
|
|
||
дзеркало |
|
||
D (+) гліцериновий |
|
L (–) гліцериновий |
|
альдегід |
|
альдегід |
|
Так, D-молочна кислота конфігурації І, одержана при бродінні сахарози за присутності
Bacillus acidi laevolactici, належить до D-ряду і є лівообертаючою, а м’ясомолочна (+) кислота конфігурації ІІ, виділена з м’язів, належить до L-ряду і є правообертаючою. Знак обертання не має прямого зв’язку з конфігурацією.
HO |
C O |
HO |
C O |
H |
C* OH |
HO |
C* H |
|
CH3 |
|
CH3 |
І |
|
|
ІІ |
Енантіомери молочної кислоти
У 1951 р. рентгеноструктурно було доведено, що вибір моделі гліцеринового альдегіду був вірним.
Суміш певної кількості ліво- і правообертаючих ізомерів не має оптичної активності і називається рацематом. Кількість оптичних ізомерів для даної сполуки залежить від кількості хіральних атомів Карбону і визначається формулою:
X = 2n,
де n — кількість хіральних атомів Карбону. Якщо n>1, то підвищується і кількість можли-
вих стереоізомерів. Такі ізомери відрізняються конфігурацією у деяких (але не у всіх) центрів і називаються діастереоізомерами.
Номенклатура оптичних ізомерів
D-, L-система позначення конфігурації має обмежене застосування, використовується переважно в хімії вуглеводів і амінокислот. Щодо інших класів сполук D-, L-система часто не дає однозначних результатів. Іноді буває неможливо співвіднести конфігурацію сполук із D- або L-гліцериновим альдегідом. Наприклад, неясно, як зіставити кисневмісні замісники в гліцериновому альдегіді з атомами галогенів у молекулі бромфторхлорметану.
|
CI |
|
CI |
||
|
|
||||
Br |
|
F |
F |
|
Br |
|
|
||||
|
H |
|
H |
||
|
|
||||
|
|
||||
дзеркало Енантіомери бромфторхлорметану
Тому була запропонована більш універсальна номенклатурна система позначення конфігурації центрів хіральності — R-, S-система (від лат. rectus — правий, sinister — лівий). В основі її лежить принцип старшинства замісників, пов’язаних із центром хіральності. Старшинство замісників визначається атомним номером елемента, безпосередньо пов’язаного з центром хіральності,
— чим він більше, тим старше замісник. Так, у молекулі бромфторхлорметану замісники розташовуються за убуванням у такому порядку:
35Br > 17CI > 9F > 1H.
У складніших випадках старшинство груп, які оточують центр хіральності, визначають за другим, третім і більш далекими шарами атомів. Звичайно таке потрібно в ситуаціях, коли з центром хіральності зв’язані замісники, які мають у першому шарі атоми Карбону. Наприклад, група –СН2ОН старша за групу
–СН2СН3.
15

а б
Рис. 1.2. R-, S-система:
а — R-конфігурація; б — S-конфігурація
Після встановлення старшинства замісників молекулярну модель сполуки розташовують у просторі так, щоб наймолодший замісник (у нашому і в багатьох інших випадках — це атом Гідрогену) не потрапляв у поле зору спостерігача. Якщо старшинство трьох інших замісників убуває за годинниковою стрілкою, то центру хіральності приписують R-конфігурацію (рис. 1.2, а), якщо проти годинникової стрілки — S-конфігурацію (рис. 1.2, б).
2. Конформаційна ізомерія
Ізомери, які взаємоперетворюються при обертанні навколо простого зв’язку, називаються ро-
томерами, конформерами або конформаційними ізомерами (ізомери, що утворюються внаслідок вільного повороту навколо σ -зв’язків). Оскільки енергетичні бар’єри між такими ізомерами незначні, розділити їх практично неможливо, але виявити в суміші фізико-хімічними методами дослідження можна.
а) σ -зв’язок допускає вільне обертання атомів навколо зв’язку, яке однак може гальмуватися об’ємними замісниками. Кожний із можливих варіантів називається конформацією. Вільне обертання ілюструють проекційні формули Ньюмена:
H |
H |
H |
|
H |
H |
H |
|
H |
|
H |
H |
H H H |
|||||
H |
|
H |
|
H |
|
|||
|
H |
H |
|
|
H |
|||
|
H |
|
H H |
H H |
H |
|||
|
|
|
|
|
||||
Загальмована Заслонена Конформації стану
Переважне перебування молекул природних і фізіологічно активних сполук у певній конформації означає набування або втрату цими сполуками відповідних властивостей. Наприклад, ацетилхолін є передавачем нервових імпульсів.
|
|
|
H |
|
|
|
H |
|
H |
+ |
|
H |
+ |
||
CH COO |
|
|
N(CH3)3X- |
NH COO |
|
|
N(CH3)3X- |
|
|
|
|||||
3 |
|
|
|
2 |
|
|
|
H H |
|
H H |
|
||||
Ацетилхолін Карболхолін
Ця функція здійснюється в тій конформації, в якій два об’ємних замісники — СН3СОО– та –N+(CH3)3 — максимально віддалені один від одного. Дефіцит ацетилхоліну спричинює параліч. Синтетичний аналог ацетилхоліну карбохолін має таку ж просторову будову та властивості, а тому може тимчасово виконувати функцію ацетилхоліну в тих чи інших клітинах.
б) Найвідомішими конформерами є конформаційні ізомери циклогексану. На одномірній потенціальній кривій подане співвідношення між окремими формами:
«крісло» «твіст-кон- |
скручена |
«ванна» |
формація» |
«ванна» |
|
Конформації циклогексану
Найстабільнішою є форма «крісла», другому мінімуму відповідає форма скрученої ванни («твіст-форма») (рис. 1.3).
Е 
37,7–46,0 |
22,2 |
28,9 |
кДж/моль |
кДж/моль кДж/моль |
|
Конформаційна координата
Рис. 1.3. Енергетика конформаційних перетворень циклогексану
Електронна структура атома Карбону в органічних сполуках
У періодичній системі елементів Д. І. Менделєєва Карбон розташований у головній підгрупі IV групи, його порядковий номер 6 (6C). Звичайно в органічних сполуках атом Карбону має валентність чотири. Виходячи з електронної структури атома Карбону в основному стані, можна дійти висновку про його двохвалентність, тому що на зовнішньому електронному шарі перебувають два неспарених електрони. Тому для опису чотирьохвалентного стану вдаються до уявлення про збудження атома Карбону та гібридизацію його атомних орбіталей.
Електронна структура атома Карбону
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2s2 2p |
|
1 |
2p |
1 |
2p |
0 |
|
|
|
2s1 2p |
1 |
2p |
|
1 2p |
|
1 |
|||||||||||||
|
|
|
|
|
|
|
|
x |
|
|
y |
z |
|
|
|
|
|
|
|
x |
|
|
y |
|
|
|
z |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1s2 |
|
|
|
|
|
|
|
|
|
1s2 |
|
|
|
|
|
|
|
|
|
|||||||||||||
|
Основний стан |
|
|
|
Збуджений стан |
|
||||||||||||||||||||||||||
Атомна орбіталь — це частина простору, в якій імовірність знаходження електрона максимальна.
s-орбіталь має сферичну форму, а р-орбіталь
— форму об’ємної вісімки, певним чином орієнтованої в просторі (рис. 1.4).
При збудженні атома Карбону один із двох електронів 2s-підрівня переходить на вільну орбіталь 2р-підрівня. Це можливо й у зв’язку з неве-
16

z
|
|
y |
|
інних орбіталей. За формою вони також являють |
|
|
|
|
собою об’ємні вісімки. Відмінність їх від sp3- |
||
|
|
|
|
||
|
|
|
|
гібридних орбіталей в тому, що більша лопать |
|
|
|
x |
|
об’ємної вісімки в них трохи коротша. Sp2- |
|
|
|
|
|
гібридні орбіталі лежать в одній площині й спря- |
|
|
|
|
|
мовані під кутом 120° одна до одної, тобто їхні |
|
|
s |
|
|
вершини утворюють рівнобічний трикутник. |
|
|
|
|
Одна р-орбіталь залишається вільною, не- |
||
|
|
|
z |
||
z |
z |
|
гібридизованою. Вона зберігає форму правиль- |
||
y |
|
||||
|
|
y |
ної об’ємної вісімки й розташовується перпенди- |
||
y |
|
|
|||
|
|
|
кулярно площині, в якій лежать три sp2-гібридні |
||
|
|
|
|
||
x |
|
x |
x |
орбіталі. |
|
|
В sp-гібридизації беруть участь одна s- і одна |
||||
|
|
xy |
|
||
|
|
|
р-орбіталь. У результаті утворюються дві рівно- |
||
|
|
xz |
|
||
уz |
|
|
цінні гібридні орбіталі, що мають форму об’ємних |
||
|
|
|
|||
px |
py |
|
pz |
вісімок із ще коротшою великою лопаттю. Вони |
|
|
розташовуються під кутом 180° одна до одної, |
||||
|
|
|
|
||
Рис. 1.4. Атомні s- і р-орбіталі |
|
тобто на одній прямій, і спрямовані в протилежні |
|||
|
|
|
|
сторони від ядра атома. |
|
|
|
|
|
Дві р-орбиталі, які не беруть участь у гібриди- |
|
ликою різницею в енергії 2s- і 2р-підрівнів. Такий |
зації, зберігаютьформуправильнихоб’ємнихвісімок |
||||
атом Карбону в збудженому стані має вже чоти- |
і розташовуються взаємно перпендикулярно. |
||||
ри неспарених електрони: один на 2s- і три — на |
|
||||
2р-орбіталях. |
|
|
|
|
|
Для обгрунтування рівноцінності чотирьох |
|
||||
валентностей атома Карбону використовують |
1.2. КЛАСИФІКАЦІЯ ХІМІЧНИХ |
||||
опис його електронної структури із залученням |
|||||
РЕАКЦІЙ. РЕАКЦІЙНА ЗДАТНІСТЬ |
|||||
поняття гібридизації. Такий опис базується на |
|||||
АЛКАНІВ, АЛКЕНІВ, АРЕНІВ, |
|||||
уявленні про те, що після змішання орбіталей |
|||||
СПИРТІВ, ФЕНОЛІВ, АМІНІВ |
|||||
відбувається утворення нових, гібридних орбіта- |
|||||
лей, рівноцінних за енергією (рис. 1.5). |
Вивчення взаємозв’язку між будовою і влас- |
||||
При цьому гібридизацію слід розуміти як ма- |
|||||
тематичну, квантово-механічну модель, а не як |
тивостями різних природних і лікарських сполук |
||||
якийсь фізичний процес. Залежно від кількості |
довело, що їхня біологічна активність значною |
||||
орбіталей збудженого атома Карбону, що беруть |
мірою визначається просторовим розміщенням |
||||
участь у гібридизації, можливі три її види. |
атомів і молекул, які входять до складу цих спо- |
||||
В sp3-гібридизації беруть участь чотири орбі- |
лук. Комплементарність лежить в основі проце- |
||||
талі — одна s- і три р-орбіталі — з утворенням |
су гідролізу харчових продуктів під впливом фер- |
||||
чотирьох рівноцінних гібридних орбіталей. Sp3- |
ментів (структурна відповідність конфігурацій |
||||
гібридні орбіталі мають форму об’ємної вісімки, |
ферменту і субстрату), процесу синтезу нових спе- |
||||
у якої одна з лопатей значно більша за інші. |
цифічних для даного організму біополімерів (мат- |
||||
Ці орбіталі розташовуються в просторі одна |
ричні синтези білків і нуклеїнових кислот), захис- |
||||
відносно одної під кутом 109,5°. Якщо з’єднати |
них (імунних) реакцій організму та ін. |
||||
вершини цих орбіталей, то утвориться об’ємна |
Механізми дії лікарських засобів на організм |
||||
фігура — тетраедр. Атом Карбону в sp3-гібрид- |
людини (на відповідні рецептори клітинних мем- |
||||
ному стані прийнято називати тетраедричним. |
бран) також зумовлені просторовою будовою |
||||
В sp2-гібридизації беруть участь одна s- і дві |
цих сполук і відповідних їм рецепторів. Визначен- |
||||
р-орбіталі з утворенням трьох гібридних рівноц- |
ня просторового розміщення атомів у молекулах |
||||
|
|
|
|
органічних сполук, що мають біологічну ак- |
|
|
z |
|
|
тивність, полягає в послідовності виявлення їх |
|
|
y |
|
будови, конфігурації та конформації. |
||
|
|
|
|||
|
|
x |
|
Будову біологічно активних сполук знахо- |
|
|
|
|
дять на основі елементного аналізу (вміст C, H, |
||
|
|
|
|
||
|
|
|
|
N, O, S, P тощо). Просторова конфігурація моле- |
|
|
|
|
|
кул біологічно активних речовин визначається |
|
pz |
pz |
|
pz |
гібридизацією електронних орбіталей атомів, які |
|
|
беруть участь в утворенні хімічних зв’язків. |
||||
|
|
|
py |
||
|
|
90° |
В органічних сполуках атом Карбону може |
||
109,5° |
|
90° |
|||
|
90° |
перебувати у трьох валентних станах — їм відпо- |
|||
|
|
||||
120° |
|
px |
px |
відають sp3-, sp2-, sp-гібридизація. В усіх випад- |
|
|
|
|
|
ках тип зв’язку однаковий — ковалентний непо- |
|
|
|
|
|
лярний або малополярний. Перебіг будь-якої |
|
sp3 |
sp2 |
|
sp |
хімічної реакції супроводжується розривом ста- |
|
Рис. 1.5. Види гібридизації атома Карбону |
рих і встановленням нових зв’язків. Напрямок |
||||
реакції визначається величиною зміни вільної |
|||||
17
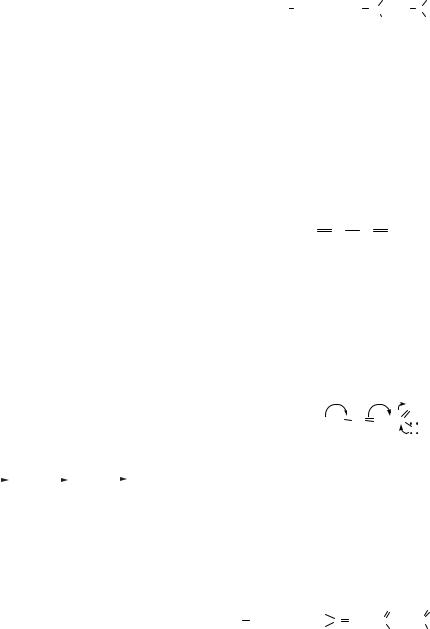
енергії Гіббса (∆ G), швидкість процесу — швидкістю найповільнішої лімітуючої стадії. Оскільки розрив ковалентного зв’язку потребує значної витрати енергії, то часто перша стадія є найповільнішою, через що швидкість органічних реакцій набагато менша, ніж швидкість іонних реакцій.
Природа хімічного зв’язку передбачає і механізм взаємного впливу атомів, безпосередньо не зв’язаних між собою. Електронні орбіталі можуть зміщуватись у молекулі так, щоб електрони «обслуговували» не тільки пару атомів, які утворюють зв’язок, а також інші атоми. Потрібно враховувати, що електронні орбіталі не мають меж і, відповідно, можуть перекриватись і впливати одна на одну через простір (ефект поля). Значною мірою взаємодія через простір відбувається в тому випадку, якщо атоми достатньо зближені, оскільки взаємодія ослаблюється пропорційно квадрату відстані.
Здатність молекули до тих чи інших типів перетворень визначається насамперед розподілом і рухливістю електронів, що залежить від таких факторів:
1.Статична поляризація зв’язків.
2.Динамічна поляризація зв’язків. Ідеальний ковалентний зв’язок може існува-
ти тільки між однорідними атомами або групами атомів. Якщо атоми характеризуються різною електронегативністю, то зв’язок між ними завжди буде полярним.
Зміщення електронної щільності по ланцюгу σ -зв’язку називається індуктивним ефектом і позначається літерою І.
Індукційний ефект передається по ланцюгу зі згасанням. Напрямок зміщення електронної густини всіх σ -зв’язків позначається прямими стрілками.
σσσ+ |
σσ+ |
σ+ |
|
σ− |
|
|
CH3 |
|
CH2 |
|
CH2 |
|
Cl |
|
|
|
||||
|
|
|
|
+ІС3Н7 |
–ІСl |
|
σσ , σσσ — поступове зменшення частки початкового заряду.
Індукційний ефект позначається стрілкою за σ -зв’язком, який сполучає атоми, у бік атома з більшою електронегативністю.
Індукційний ефект насиченого С–Н-зв’язку умовно дорівнює нулю: І = 0.
Електроноакцепторні замісники, тобто атом або група атомів, які зміщують електронну густину σ -зв’язку від атома Карбону, виявляють не-
гативний індуктивний ефект (–І-ефект).
Електронодонорні замісники, тобто атом або група атомів, які зміщують електронну густину до атома Карбону, виявляють позитивний індук-
тивний ефект(+І-ефект).
Негативний індукційний ефект мають усі без винятку ненасичені групи; зі збільшенням кількості кратних зв’язків величина –I-ефекту зростає.
Нижче подані замісники, розміщені за зменшенням –I-ефекту:
−NO2 > −C≡ N > −F > −Cl > −Br > −I >
> −COOR > −OH > −NH2 > H
Позитивний ефект мають усі алкільні замісники, величина +I-ефекту зростає зі збільшенням ступеня розгалуження ланцюга:
|
|
CH3 |
|
CH3 |
|
CH3 < |
|
C2H5 < CH |
< C |
|
CH3 |
|
|
||||
|
|
CH3 |
|
CH3 |
|
Електронне зміщення у спряжених системах за участю електронів кратних зв’язків чи неподілених електронних пар називають ефектом спря-
ження, або мезомерним ефектом (± М) за раху-
нок делокалізації р-орбіталей, які належать двом чи більше π -зв’язкам або π -зв’язкам і р-орбіталям неподілених пар електронів, які розділені одним простим зв’язком.
Спряження, або мезомерія (від грецьк. mesos
— середній) — вирівнювання зв’язків і зарядів у реальній молекулі порівняно з ідеальною.
CH2 CH CH CH2 Ідеальна молекула Бутадієн-1,3
CH2

 CH
CH

 CH
CH

 CH2 Реальна молекула
CH2 Реальна молекула
Мезомерний ефект у бутадієні-1,3 здійснюється за рахунок ππ -взаємодії.
Графічно мезомерний ефект зображується у вигляді зігнутої стрілки від подвійного зв’язку до одинарного і передається всій системі спряжених зв’язків.
Наприклад,
π,π -взаємодія
δ + |
δ + |
O |
|
||||||
H2C |
|
CH CH CH |
|
|
C |
O |
|
H |
ρ,π -взаємодія |
|
|
||||||||
|
|
|
|
||||||
|
|
|
|
|
|
|
|
||
Позитивний мезомерний ефект мають усі елек-
тронодонорні замісники, які здатні відштовхувати електронну густину у напрямку сусіднього подвійного зв’язку:
–NH2 > –OH > –OCH3 > –Cl > –Br
Негативний мезомерний ефект мають усі елек-
тронноакцепторні замісники, які притягують до себе π -електрони сусіднього подвійного зв’язку.
|
|
|
|
|
|
O |
O |
||||
NO2 > |
|
C |
|
N > C O > |
|
C > |
|
C |
> |
|
CONH2 |
|
|
||||||||||
|
|
|
|
|
|||||||
|
|
||||||||||
|
|
|
|
|
|
OR |
OH |
||||
Таким чином, у молекулі під впливом індукційного поля і мезомерних ефектів замісників відбувається формування реакційних центрів із надлишком або нестачею електронної густини. Молекула стає підготовленою для перебігу хімічної реакції за тим чи іншим механізмом.
Інколи основний вплив на реакційну здатність молекули створюють просторові ефекти, коли підхід атакуючої частинки до реакційного центру утруднений через великі за об’ємом замісники, що оточують реакційний центр.
При цьому швидкість реакції різко знижується або реакція взагалі не відбувається. Наприклад, зміна швидкості реакції приєднання за карбонільною групою нуклеофільних реагентів залежно від зв’язаних із нею замісників.
18