|
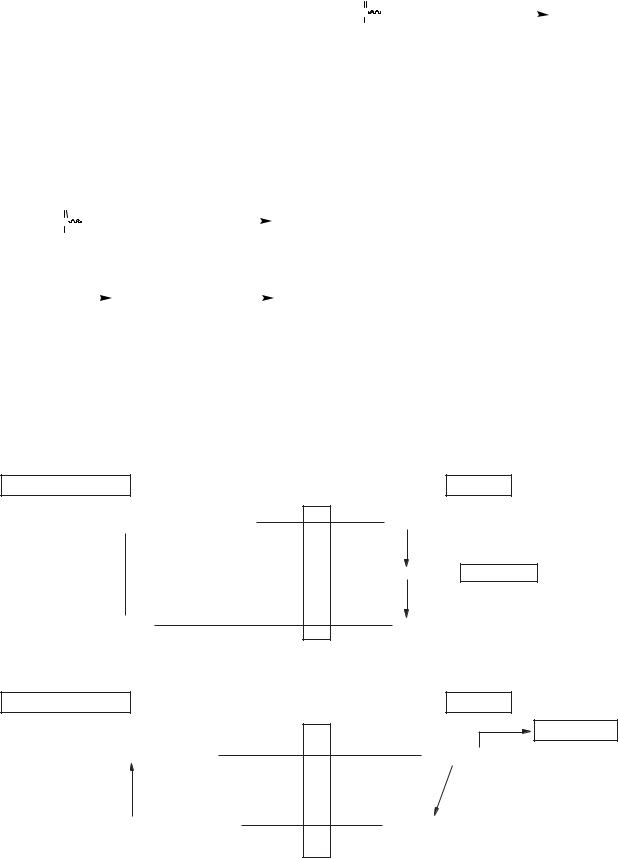
Синтез ненасичених вищих жирних кислот на |
випадку гліцерол-3-фосфат утворюється з діоксі- |
|
початкових етапах відбувається аналогічно син- |
ацетонфосфату — проміжного продукту гліколі- |
|
тезу насичених вищих жирних кислот, і лише на |
тичного розпаду глюкози. Так, при зниженні |
|
заключному етапі насичена жирна кислота пе- |
вмісту глюкози в жировій тканині (при голоду- |
|
ретворюється на ненасичену (рис. 10.6). |
ванні) утворюється незначна кількість гліцерол- |
|
|
|
|
|
|
|
3-фосфату, вивільнювані в ході ліполізу вільні |
|
|
|
|
|
|
|
жирні кислоти не можуть використовуватися на |
|
|
|
|
|
|
|
ресинтез триацилгліцеролів, тому вони залиша- |
|
|
Пальмітил-КоА |
|
|
|
|
|
|
ють жирову тканину. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Елонгаза |
|
+ Малоніл-КоА |
2) Фосфорилування гліцеролу до гліцерол-3- |
|
|
фосфату. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ НАДФН + Н+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Гліцерол фосфорилується АТФ за участю фер- |
|
|
|
|
|
|
|
менту гліцеролкінази. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Стеарил-КоА |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Гліцеролкіназа |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
OH |
|
|
CH2 |
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Десатураза |
+ НАДФН + Н+ + О2 |
|
CHOH |
|
|
+ АТФ |
|
|
CHOH |
|
OH |
|
|
|
|
|
|
|
|
|
|
-АДФ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
- НАДФ+ - 2Н |
O |
|
CH2 |
|
OH |
|
|
|
|
|
|
|
CH2 |
|
O |
|
P |
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Гліцерол |
|
|
Гліцерол-3-фосфат |
|
|
Олеїл-КоА |
|
|
|
|
|
|
|
|
|
|
|
|
|
При цьому фосфорилуванню може піддавати- |
|
|
|
|
|
|
|
|
Рис. 10.6. Схема синтезу ненасичених |
ся гліцерол, що всмоктався після гідролізу ліпідів |
|
|
жирних кислот |
|
у кишечнику, і той гліцерол, що утворився в ре- |
|
|
|
|
|
|
|
зультаті ліполізу. Гліцерол-3-фосфат таким шля- |
|
Ацетил-КоА-карбоксилаза є лімітуючим фер- |
хом інтенсивно поповнюється в печінці. У жи- |
|
ровій тканині основним шляхом утворення гліце- |
|
ментом біосинтезу вищих жирних кислот, пози- |
рол-3-фосфату є відновлення діоксіацетонфосфа- |
|
тивним модулятором якого є цитрат. Нагрома- |
ту, тому що в цій тканині дуже слабка активність |
|
дження цитрату в мітохондріях відбувається |
ферменту гліцеролкінази і висока — гліцерофос- |
|
внаслідок збільшення вмісту АТФ, який блокує |
фатдегідрогенази. Тому основним шляхом синте- |
|
ізоцитратдегідрогеназу, чим сприяє виходу цит- |
зу гліцерол-3-фосфату є перший. Гліцерол-3-фос- |
|
рату з мітохондрій у цитоплазму і перетворенню |
фат, що утворився, використовується для біосин- |
|
останнього на оксалоацетат та ацетил-КоА, |
тезу триацилгліцеролів і фосфоліпідів, однак час- |
|
який у цитоплазмі використовується для біосин- |
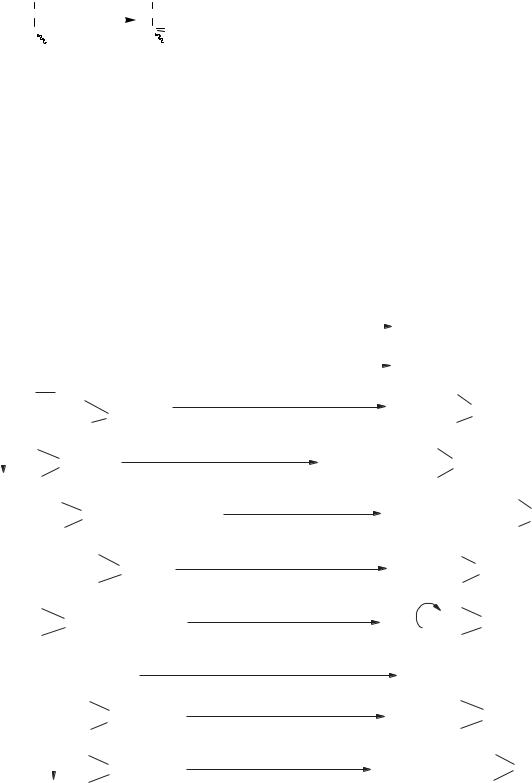
тина його під впливом ферменту фосфатази гідро- |
|
тетичних процесів (перш за все, синтезу вищих |
лізується до гліцеролу і фосфорної кислоти: |
|
жирних кислот і холестеролу). Негативними мо- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
дуляторами активності ацетил-КоА-карбоксила- |
|
CH2 OH |
|
|
|
Фосфатаза |
|
CH2 |
OH |
|
зи є кінцеві продукти синтезу, тобто вищі жирні |
|
|
|
|
|
|
OH |
|
|
+ НОН |
|
|
|
|
|
|
|
|
|
|
|
|
CHOH |
|
|
|
CHOH |
|
|
|
|
|
|
|
|
кислоти. Активність ацетил-КоА-карбоксилази |
|
|
|
|
|
|
|
|
|
|
- Н3РО4 |
|
|
|
|
|
|
|
|
|
|
|
|
CH2 O |
|
Р |
O |
|
CH2 |
ОН |
|
знаходиться під гормональним контролем, оскіль- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ки інгібується шляхом фосфорилування за учас- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Гліцерол-3-фосфат |
|
|
|
Гліцерол |
|
тю цАМФ-залежних протеїнкіназ, які, у свою |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
чергу, активуються адреналіном, глюкагоном й |
Біосинтез триацилгліцеролів |
|
|
|
|
|
|
інгібуються інсуліном. Крім того, синтез фермент- |
|
|
|
|
|
|
ного білка ацетил-КоА-карбоксилази збільшу- |
Біосинтез триацилгліцеролів перебігає в 3 ета- |
|
ється при надмірному споживанні вуглеводів і |
|
пи (рис. 10.7): |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
зменшується при голодуванні або споживанні |
І етап — взаємодія гліцерол-3-фосфату з 2 мо- |
|
великої кількості ліпідів. |
|
|
|
|
|
|
|
лекулами ацил-КоА з утворенням фосфатидної |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
кислоти. Каталізує реакцію фермент гліцерол-3- |
|
Утворення гліцерол-3-фосфату |
фосфатацилтрансфераза. |
|
|
|
|
|
|
|
|
|
|
|
ІІ етап — дефосфорилування фосфатидної кис- |
|
Цей процес може відбуватися двома шляхами: |
|
лоти до 1,2-діацилгліцеролу за участю ферменту |
|
1) Відновлення діоксіацетонфосфату до гліце- |
фосфатидатфосфатази. |
|
|
|
|
|
|
|
|
|
|
|
рол-3-фосфату. |
|
|
|
III етап — сполучення третьої молекули ацил- |
|
Каталізує реакцію гліцерофосфатдегідрогена- |
КоА з 1,2-діацилгліцеролом з утворенням три- |
|
за, коферментом якої є НАД+: |
|
ацилгліцеролу. Каталізує реакцію діацилгліце- |
|
|
|
|
|
|
|
ролацилтрансфераза: |
|
|
|
|
|
|
|
|
|
|
|
|

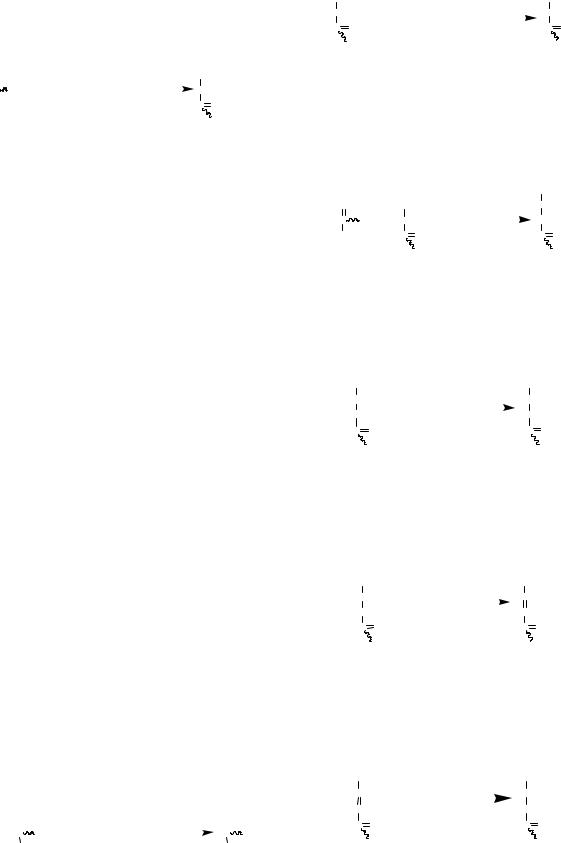

 Цитрат
Цитрат  НАДН + Н
НАДН + Н

 Цитрат
Цитрат Ацетил Карнітин
Ацетил Карнітин