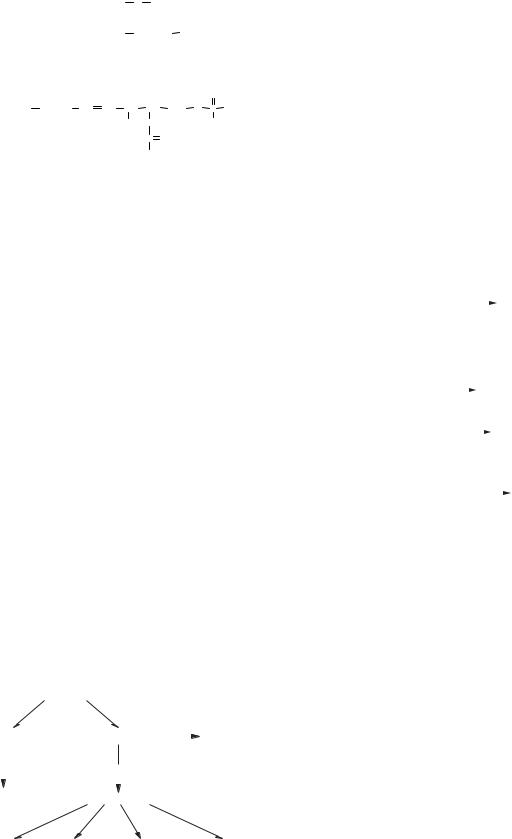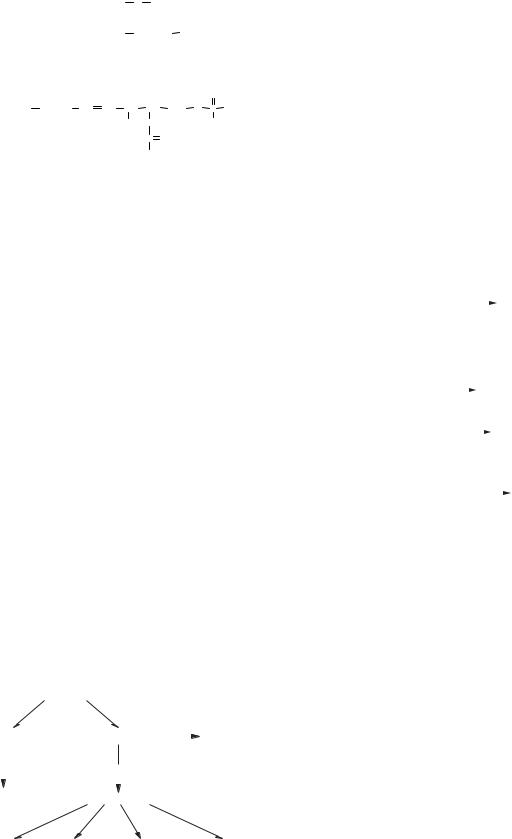|
|
|
|
|
CH2 |
|
|
OH |
+ ATФ |
|
H2C |
|
OH |
|
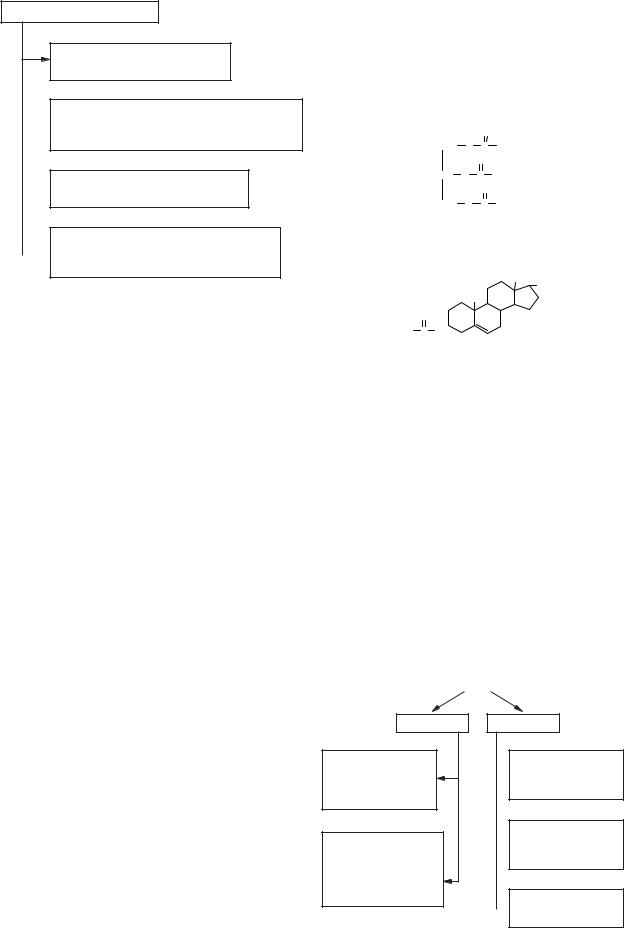
Окиснення жирних кислот |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
OH |
|
|
HC |
|
OH |
|
Для жирних кислот, що входять до складу |
|
|
|
|
|
- AДФ |
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
OH |
|
|
|
H C |
|
|
O |
|
P O |
|
|
|
|
|
|
|
|
|
|
|
|
ліпідів організму, а також надходять в організм |
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
з їжею, характерні кілька шляхів метаболізму: |
|
|
Гліцерол |
|
|
Гліцерол-3-фосфат |
|
|
|
|
1. Окиснення до СО2 і Н2О з утворенням АТФ. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Гліцерофосфат, що утворився, проникає в |
Вільні жирні кислоти спочатку окиснюються до |
|
ацетил-КоА, який далі окиснюється в ЦТК до |
|
мітохондрії. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
СО2 і Н2О. У ході цього окиснення вивільняється |
|
2. Окиснення гліцерол-3-фосфату в мітохонд- |
|
енергія, причому близько 40 % її акумулюється в |
|
ріях клітини до діоксіацетонфосфату. Каталізує |
АТФ. Жирні кислоти є основним субстратом для |
|
реакцію гліцерофосфатдегідрогеназа, кофермен- |
енергетичного обміну в печінці. |
|
том якої є ФАД: |
|
|
|
|
|
|
|
|
|
|
|
|
2. Утворення кетонових тіл. Надлишок аце- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
тил-КоА, що утворився при окисненні жирних |
|
CH2 |
|
|
OH |
|
|
|
|
+ ФАД |
CH2 |
OH |
кислот і не використаний печінкою, перетво- |
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
C |
|
O |
|
рюється на кетонові тіла — ацетоацетат і |
|
|
CH |
|
|
|
OH |
|
|
|
|
|
|
OH |
|
|
|
|
|
|
- ФAДН2 |
|
|
|
|
|
|
|
O P |
|
|
|
|
|
|
|
O P O |
β -гідроксибутират, які переносяться кров’ю в інші |
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
O |
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
OH |
тканини, де використовуються для окиснення в |
|
Гліцерол-3-фосфат |
|
Діоксіацетонфосфат |
ЦТК. Кетонові тіла можна розглядати як транс- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
портну форму легкодоступних субстратів. Висо- |
|
Діоксіацетонфосфат дифундує з мітохондрій у |
кодиференційовані тканини (міокард, мозок) |
|
цитозоль. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
поглинають ацетоацетат і гідроксибутират із |
|
3. Ізомеризація діоксіацетонфосфату в цито- |
крові, тому вони в крові практично не виявля- |
|
золі клітини в гліцеральдегід-3-фосфат і перетво- |
ються і не виводяться з сечею. Однак це відбу- |
|
рення його гліколітичним шляхом на піровино- |
вається тільки при високоефективному функціо- |
|
градну кислоту (піруват). Піруват піддається |
нуванні ЦТК. При різних патологічних проце- |
|
окисному декарбоксилюванню до ацетил-КоА, |
сах, що супроводжуються зниженням надхо- |
|
який окиснюється в циклі трикарбонових кислот |
дження кисню в тканини і порушенням функції |
|
до СО2 і Н2О. Слід підкреслити, що подібний |
циклу трикарбонових кислот, ацетоацетат на- |
|
шлях окиснення поєднаний з переносом протонів |
копичується в тканинах, декарбоксилюється до |
|
із цитоплазми, де їхнє нагромадження призво- |
ацетону, вміст кетонових тіл у крові збільшуєть- |
|
дить до ацидозу, у мітохондрії, де вони викорис- |
ся, вони потрапляють у сечу і розвивається ке- |
|
товуються у тканинному диханні. |
тонемія і кетонурія. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3. Біосинтез холестеролу і жирних кислот. |
|
Біологічна роль процесу окиснення гліцеролу |
Частина ацетил-КоА, що утворився з жирних |
|
кислот (й із глюкози) використовується на біо- |
|
1. У процесі окиснення гліцеролу вивільняєть- |
|
синтез холестеролу, з якого утворюються жовчні |
|
ся енергія, частина якої резервується в АТФ. При |
кислоти. |
|
цьому в результаті окиснення ФАДН2, що утво- |
4. Біосинтез ліпопротеїнів плазми крові. Жирні |
|
рюється в мітохондріях у гліцерофосфатдегідроге- |
кислоти використовуються в синтезі ліпідної ча- |
|
назній реакції, у ланцюзі дихальних ферментів |
стини ліпопротеїнів плазми крові. Ліпопротеїни |
|
синтезуються 2 молекули АТФ. На етапах окис- |
функціонують як переносники ліпідів у жирову |
|
нення гліцеральдегід-3-фосфату до пірувату син- |
тканину, де вони нагромаджуються у вигляді |
|
тезується 5 молекул АТФ. Із них 3 молекули ут- |
триацилгліцеролів. |
|
ворюються при окисненні в ланцюзі дихальних |
5. Утворення вільних жирних кислот плазми |
|
ферментів НАДН+Н+, отриманого в гліцеральде- |
крові. Вільні жирні кислоти зв’язуються з сиро- |
|
гідфосфатдегідрогеназній реакції, і по 1 молекулі |
ватковим альбуміном і далі доставляються кро- |
|
АТФ при перетворенні 1,3-бісфосфогліцеролової |
в’ю в серце й скелетні м’язи; ці органи викорис- |
|
кислоти на 3-фосфогліцеролову кислоту, а також |
товують жирні кислоти як основний енергетич- |
|
фосфоенолпірувату на піруват. Окиснення |
ний матеріал. |
|
НАДН (утворюється в піруватдегідрогеназній |
6. Частина жирних кислот використовується |
|
реакції) у ланцюзі дихальних ферментів дає 3 мо- |
на біосинтез різних тканинних ліпідів. |
|
лекули АТФ, а окиснення ацетил-КоА в ЦТК — |
Теорія біологічного окиснення жирних кислот |
|
12 молекул АТФ. Загалом при окисненні 1 моле- |
була запропонована в 1904 р. німецьким біохімі- |
|
кули гліцеролу до СО2 і Н2О синтезуються 22 мо- |
ком Францем Кноопом і дістала назву теорії |
|
лекули АТФ, із них одна витрачається в гліце- |
β -окиснення, оскільки окиснення жирної кислоти |
|
ролкіназній реакції, тобто загальний баланс ста- |
і розрив її молекули відбувається у атома Кар- |
|
новить 21 молекулу АТФ. |
|
|
|
|
|
|
бону, що перебуває в β -положенні. Цей процес |
|
2. Гліцерол-3-фосфат може використовувати- |
перебігає переважно в мітохондріях печінки, ске- |
|
ся на біосинтез нейтральних жирів і фосфогліце- |
летних м’язів і серця. Причому у печінці жирні |
|
ролів. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
кислоти окиснюються переважно до ацетоаце- |
|
3. Утворені з гліцеролу діоксіацетонфосфат і |
тил-КоА і ацетил-КоА, а в скелетних м’язах і |
|
гліцеральдегід-3-фосфат можуть використовува- |
серці — до СО2 і Н2О. До 50 % жирних кислот |
|
тися на біосинтез вуглеводів (глюкози). |
крові поглинаються печінкою. |