|
— елонгація припиняється, коли глікогенсин- |
Гормональна регуляція метаболізу глікогену |
|
таза не контактує з глікогеніном; |
У м’язах адреналін стимулює глікогеноліз і |
|
— взаїємодія синтаза-глікогенін лімітується |
|
гальмує глікогенез шляхом: |
|
розміром гранул глікогену. |
|
|
|
— активації глікогенфосфорилази за рахунок |
|
|
|
|
|
|
|
|
|
|
Мобілізація глікогену |
її цАМФ-залежного фосфорилування; |
|
Глюкоза, депонована у формі глікогену, ви- |
— інгібування глікогенсинтетази за рахунок |
|
її цАМФ-залежного фосфорилування; |
|
вільняється за участю глікогенфосфорилази у |
|
вигляді глюкозо-1-фосфату. Цей фермент каталі- |
— підвищення проникності мембран м’язових |
|
клітин для глюкози, яка використовується для |
|
зує фосфороліз кінцевих 1,4-глікозидних зв’язків |
|
глікогену до того моменту, поки на ланцюгах, |
синтезу глікогену; |
|
що виходять із місця розгалуження (α -1,6-гліко- |
— зменшення внутрішньоклітинного рівня |
|
зидні зв’язки), не залишиться близько 4 залишків |
цАМФ за рахунок активації її розщеплення фос- |
|
глюкози. Інший фермент α -1,6→ |
1,4-глюкантранс- |
фодіестеразою. |
|
фераза переносить трисахаридний фрагмент з |
У печінці глюкагон стимулює глікогеноліз і |
|
гальмує глікогенез за механізмом, аналогічним дії |
|
одного ланцюга на інший, α -1,6-ділянка розга- |
|
луження стає доступною для аміло-α -1,6-глюко- |
адреналіну в клітинах м’язів. |
|
зидази, яка гідролітично розщеплює α -1,6-гліко- |
Інсулін підвищує активність ферментативних |
|
зидні зв’язки, відщеплюючи глюкозу. Утворений |
реакцій синтезу глікогену. |
|
глюкозо-1-фосфат за участю фосфоглюкомутази |
Активація за участю цАМФ |
|
перетворюється на глюкозо-6-фосфат. Подальша |
|
Аденілатциклаза активується гормоном адре- |
|
доля глюкозо-6-фосфату в м’язах і печінці різна. |
|
наліном за допомогою β -адренергічних рецеп- |
|
Голодування призводить до зникнення гліко- |
торів, локалізованих у клітинній мембрані |
|
гену в печінці. Однак при ритмічному харчуванні |
|
м’язів. У печінці аденілатциклаза активується |
|
кожна молекула глікогену може існувати довго: |
глюкагоном, що діє на глюкагонові рецептори. |
|
спочатку молекули глікогену зменшуються за ра- |
цАМФ утворюється з АТФ під дією аденілатцик- |
|
хунок розщеплення периферійних гілок, а після |
лази. Підвищення концентрації цАМФ активує |
|
чергового прийому їжі знову виростають до попе- |
протеїнкіназу. Ця кіназа каталізує фосфорилу- |
|
редніх розмірів. Аналогічні процеси відбуваються |
вання неактивної кінази фосфорилази, що, у |
|
й у м’язовій тканині, але тут вони значною мірою |
свою чергу, шляхом фосфорилування активує |
|
визначаються режимом м’язової роботи. |
фосфорилазу b, яка переходить у фосфорилазу а. |
|
|
|
|
|
|
|
|
|
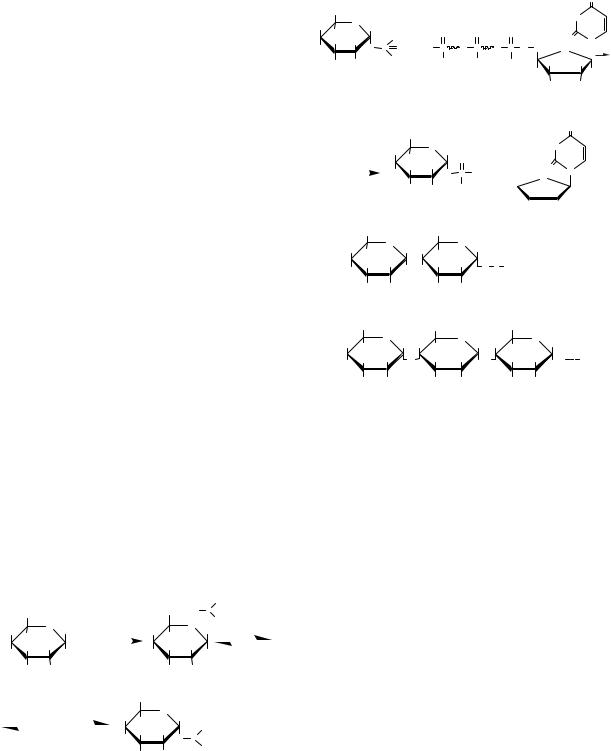
Регуляція глікогенолізу і глікогенезу |
Фосфорилаза b перетворюється на фосфорилазу |
|
Провідну роль у регуляції синтезу і розпаду |
а за допомогою фосфорилування залишку сери- |
|
глікогену відіграють глікогенсинтаза і глікоген- |
ну кожної субодиниці. Ця ковалентна модифіка- |
|
фосфорилаза. Кожний із цих ферментів існує в |
ція фосфорилази b каталізується кіназою фосфо- |
|
двох формах, здатних до взаємоперетворення, які |
рилази. |
|
розрізняються активністю (рис. 9.5–9.6). Зміни |
Фосфорилаза а дезактивується за допомогою |
|
активності відбуваються в результаті фосфорилу- |
гідролізу фосфосеринового залишку кожної суб- |
|
вання і дефосфорилування (ковалентна модифі- |
одиниці під дією протеїнфосфатази. |
|
кація ферменту), а також алостеричного механіз- |
М’язова фосфорилаза b активна тільки в при- |
|
му регуляції активності ферменту. |
сутності високих концентрацій АМФ, що діє ало- |
|
|
|
|
|
|
|
стерично, зв’язуючись з фосфорилазою b і зміню- |
|
|
|
+АТФ |
|
|
|
ючи її конформацію; АТФ діє як негативний ало- |
|
|
|
|
|
|
|
стеричний ефектор, на відміну від АМФ. |
|
|
|
цАМФ-залежна кіназа фосфорилази |
|
|
|
|
|
Глюкозо-6-фосфат також інгібує фосфорила- |
|
|
|
|
|
|
|
|
Фосфорилаза b |
Фосфорилаза a |
|
зу b, з’єднуючись із ділянкою зв’язування для |
|
(неактивна) |
(активна) |
АМФ на ферменті. При більшості фізіологічних |
|
|
|
|
|
|
|
|
|
|
Протеїнфосфатаза |
|
умов фосфорилаза неактивна, тому що інгібуєть- |
|
|
|
|
|
|
|
ся АТФ і глюкозо-6-фосфатом. Фосфорилаза b ак- |
|
|
|
-Н3РО4 |
|
|
|
|
|
|
|
|
|
тивна тільки тоді, коли енергетичний статус |
|
Рис. 9.5. Регуляція активності глікогенфосфорилази |
|
клітин низький. |
|
|
|
|
|
|
|
|
Глікогенфосфорилаза і глікогенсинтетаза регу- |
Мобілізація глікогену — це кінцева ланка кас- |
|
каду реакцій. Активація першого ферменту кас- |
|
люютьсяреципрокно: активаціяглікогенфосфорила- |
каду — аденілатциклази — спричинює посилен- |
|
зи (і фосфоролізу глікогену) відбувається в умовах |
ня розпаду глікогену і водночас пригнічення |
|
інактивації глікогенсинтетази (і синтезу глікогену). |
його синтезу. Активація аденілатциклази в ге- |
|
|
|
+АТФ |
|
|
|
патоцитах відбувається за умов взаємодії з мем- |
|
|
|
|
|
|
бранними рецепторами гормону α -клітин під- |
|
|
|
|
|
|
|
|
|
|
цАМФ-залежна протеїнкіназа |
|
шлункової залози, глюкагону. |
|
|
|
|
|
|
|
|