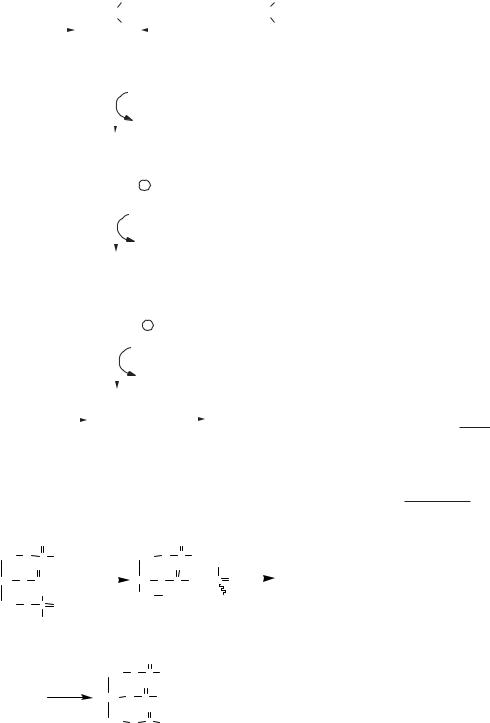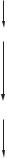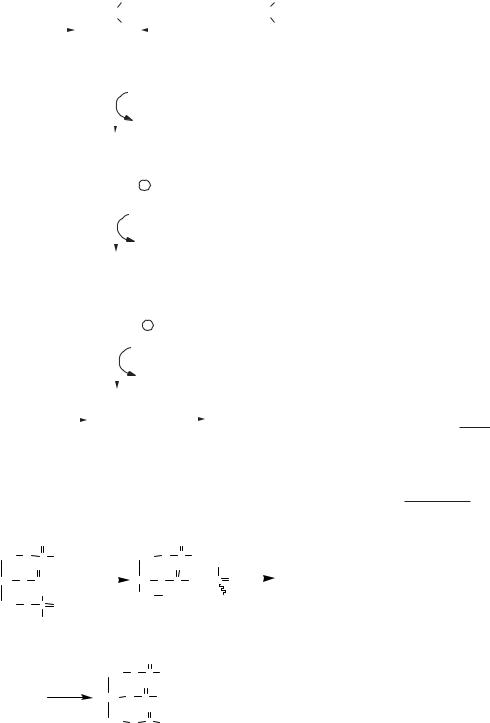1-й етап
Перетворення ацетил-КоА на мевалонову кислоту
Ацетил-КоА + Ацетил-КоА
Ацетил-КоА-ацетилтрансфераза
Ацетоацетил-КоА + НSКоА + Ацетил-КоА
+ НОН ГМГ-КоА-синтаза - НОН - HSKoA
β -Гідрокси-β -метилглутарил-КоА
+ 2 НАДФН+Н+ ГМГ-КоА-редуктаза - 2 НАДФ+ - НSКоА
Мевалонова кислота
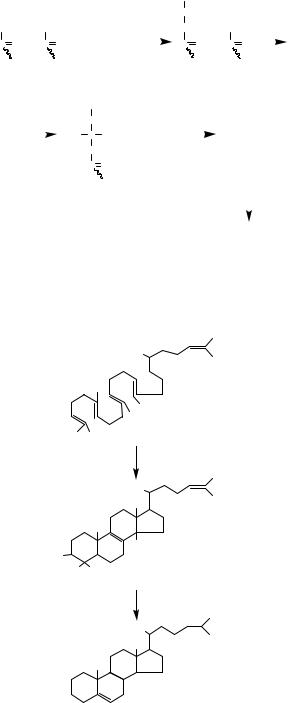
2-й етап
Утворення сквалену з мевалонової кислоти
3-й етап
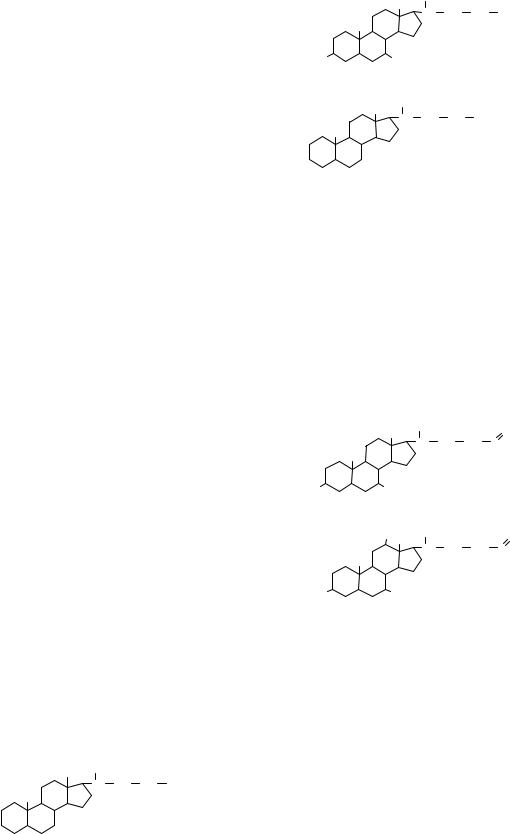
Циклізація сквалену у холестерол
Рис. 10.8. Схема біосинтезу холестеролу
Біосинтез холестеролу схематично подано на рис. 10.8.
Обмін холестеролу
Близько 80 % холестеролу синтезується в печінці, 10 % — у клітинах тонкого кишечнику, 5 % — у клітинах шкіри й 5 % — в інших клітинах.
При вмісті в добовій їжі людини 2–3 г холестеролу синтез ендогенного холестеролу майже повністю переривається, тому що холестерол інгібує ГМГ-КоА-редуктазу і пригнічує синтез мевалонової кислоти. У гепатоцитах і клітинах кишечнику синтезується холестерол не тільки для власних потреб, але й на «експорт». У цих клітинах утворюються ліпопротеїни, що надходять у кров (ліпопротеїнове ядро містить ефіри холестеролу, а вільний холестерол перебуває між шарами фосфоліпідів). У такому стані холестерол транспортується у кровоносному руслі.
Холестерол, що циркулює в крові у складі ліпопротеїнів, переміщається між окремими (в основному ЛПВЩ-ЛПНЩ) групами ліпопротеїдів, а також між ліпопротеїнами і клітинами. Так, особливо активний обмін холестеролу відбувається між ЛПНЩ і ЛПВЩ: при контакті цих частинок холестерол дифундує з однієї частинки в іншу, але в цілому переважає потік холестеролу в ЛПВЩ, активно відбувається етерифікація холестеролу під дією лецитин-холестерол-ацил- трансферази (ЛХАТ), що каталізує перенос ацильного залишку (переважно олеїнової або лінолевої кислот) із β -положення лецитину на холестерол. Локалізована ЛХАТ у поверхневому шарі ЛПВЩ, утворені тут ефіри холестеролу поринають усередину (в ядро) частинки. Внаслідок цього концентрація холестеролу в поверхневому
шарі ЛПВЩ зменшується й звільняється місце для надходження холестеролу з інших ліпопротеїнів.
Двосторонній обмін холестеролу шляхом дифузії відбувається також при контакті ліпопротеїнів із клітинами. І в цьому випадку існує переважний напрямок потоків: ЛПВЩ вилучають холестерол із клітинних мембран, а ЛПНЩ, навпаки, постачають клітинам холестерол. Навантажені холестеролом ЛПВЩ видаляються з кровотоку шляхом ендоцитозу клітинами кишечнику, а також печінки, а ЛПНЩ поглинаються клітинами багатьох органів. Отже, ЛПВЩ запобігає нагромадженню надлишку холестеролу
вклітинах, а ЛПНП забезпечує клітини холестеролом при збільшенні потреби в ньому (наприклад, під час росту і поділу клітин, коли холестерол витрачається на утворення нових мембран).
Видалення холестеролу з тканин, як і його поповнення в тканинах, також відбувається двома шляхами: його окисненням у жовчні кислоти
впечінці з наступною екскрецією жовчних кислот у тонкий кишечник і подальшим виведенням із калом (приблизно 0,5 г за добу), тобто сумарна кількість холестеролу, що надходить у кишечник з їжею й синтезованого в тканинах, дорівнює сумарній кількості холестеролу і жовчних кислот, що екскретуються:
Холестерол їжі + Холестерол ендогенний =
=Холестерол + Жовчні кислоти
Унормі концентрація холестеролу в крові дорівнює 115–340 мг% (або 3–9 ммоль/л). Якщо порушено баланс між надходженням холестеролу з їжею і його синтезом в організмі, з одного боку, і виведенням жовчних кислот і холестеролу, з іншого боку, то концентрація холестеролу в тканинах і крові змінюється. Найбільш серйозні наслідки пов’язані з гіперхолестеролемією: при цьому збільшується ймовірність захворювань на атеросклероз і жовчнокам’яну хворобу.
Жовчнокам’яна хвороба. При цьому захво-
рюванні в жовчному міхурі або протоках утворюються камені в результаті осадження і кристалізації компонентів жовчі. Звичайно в жовчних каменях основна маса — це холестерол і білірубін. Розрізняють два типи жовчних каменів: переважно холестеролові, які містять більше 70 % холестеролу, і переважно білірубінові. У 2/3 випадків хвороби зустрічаються холестеролові камені.
Холестерол у жовчі може існувати в трьох фазах. Перша фаза — це змішані міцели, що містять холестерол, жовчні кислоти й фосфатидилхолін. Друга фаза — позаміцелярний рідкокристалічний холестерол у водному оточенні жовчі. Третя фаза — твердокристалічний холестерол або його осад. Рідкокристалічна фаза нестабільна: холестерол із неї намагається перейти або в міцели, або
восад. Зменшення синтезу (або екскреції) жовчних кислот або збільшення синтезу холестеролу може призвести до відносного надлишку холе-