|
|
|
Оскільки ферментативна реакція оборотна, |
спочатку переноситься на кофермент з утворен- |
то, імовірно, у напрямку утворення γ -кетоглута- |
ням основи Шиффа, що піддається внутрішньо- |
рату фермент використовує НАД+, і НАДН+Н+, |
молекулярній перебудові, вивільняється кетокис- |
що утворюється, залучатиметься в ланцюг тка- |
лота і піридоксамінфосфат, що, у свою чергу, |
нинного дихання, а в напрямку утворення глу- |
взаємодіє з іншою кетокислотою з утворенням |
тамату фермент використовує відновлені кофер- |
проміжної сполуки (основи Шиффа), це приво- |
менти НАДФН+Н+, необхідні для відбудовних |
дить до синтезу нової амінокислоти й переходу |
біосинтетичних процесів. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
піридоксамінфосфату в піридоксальфосфат (рис. |
|
|
|
Слід зазначити, що в результаті дезамінуван- |
11.2). |
|
ня амінокислот лише частина аміаку, що утво- |
Докладне вивчення характеру зв’язку кофер- |
рюється, знешкоджується й виводиться з організ- |
менту й апоферменту в структурі амінотрансфе- |
му з сечею у вигляді сечовини, решта використо- |
раз показало, що кофермент зв’язується з апофер- |
вується для утворення замінних амінокислот із |
ментом шляхом зв’язку карбонільної групи кофер- |
продуктів небілкового походження. Таким чи- |
менту з ε -аміногрупою лізину апоферменту. |
ном, поряд із дезамінуванням амінокислот відбу- |
Взаємодія субстрату й коферменту відбу- |
вається амінування кетокислот, тобто процес пе- |
вається не шляхом конденсації з відщепленням |
реамінування, або трансамінування. Каталізу- |
молекули води, як це припускалося раніше, а |
ють цей процес амінотрансферази, у яких кофер- |
шляхом витискання аміногрупи лізину аміногру- |
ментом є піридоксальфосфат (фосфорний ефір |
пою субстрату. |
|
вітаміну В6). Характерною особливістю цього |
Як правило, акцептором аміногруп у реакці- |
коферменту є те, що він може існувати в аль- |
ях трансамінування є кетоглутарова кислота, а |
дегідній і амінній формах. Найбільш вивченими |
з огляду на високу активність глутаматдегідро- |
є дві |
трансамінази: аланінамінотрансфераза, що |
генази доведено існування в тканинах тварин |
каталізує оборотну реакцію переамінування між |
непрямого дезамінування амінокислот. Тобто |
аланіном і α -кетоглутаратом, і аспартатаміно- |
майже всі амінокислоти спочатку взаємодіють із |
трансфераза, що каталізує оборотну реакцію пе- |
α -кетоглутаратом з утворенням глутамінової |
реамінування між аспартатом і α -кетоглутара- |
кислоти й відповідної кетокислоти, а потім глу- |
том. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
тамінова кислота піддається окисному дезаміну- |
|
|
|
Теорію процесу трансамінування розробили |
ванню. Цей процес дістав назву трансдезаміну- |
А. Е. Браунштейн і М. М. Шемякін. У результаті |
вання. Враховуючи оборотність реакцій трансамі- |
трансамінування аміногрупа від амінокислоти |
нування і дезамінування, доведено існування в |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
організмі трансреамінування, завдяки якому |
R |
|
CH |
|
|
COOH + Білок-Лізин |
|
|
|
|
R |
|
|
CH |
|
|
|
COOH |
|
R |
C |
COOH |
здійснюється синтез замінних амінокислот. Ме- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ханізм його полягає у відновному амінуванні |
|
|
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
α -кетоглутарової кислоти з утворенням глутамі- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
H |
C |
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
|
|
|
|
|
|
нової під дією глутаматдегідрогенази, що вико- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ПАЛФ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ПАМФ |
COOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ПАЛФ |
|
|
|
|
|
|
|
ристовує як кофермент відновлений НАДФ+, і |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
потім у переносі аміногрупи від глутамату на |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C=O |
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ HOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
будь-яку кетокислоту в реакції трансамінування. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H + R |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 + H2N |
|
C |
|
|
H |
|
|
|
|
|
H2N |
|
C |
|
|
|
|
C |
|
COOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Вуглецеві залишки більшості амінокислот мо- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
ПАМФ |
|
|
|
|
|
|
|
|
|
ПАМФ |
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
жуть включатися в біосинтез глюкози (глікогенні |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
COOH |
COOH H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
амінокислоти). Три амінокислоти (фенілаланін, |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
COOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
тирозин, триптофан) можуть бути глікогенними |
|
|
|
|
|
|
|
C N |
|
|
C |
|
|
H |
|
|
|
|
HC N |
|
C |
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
- HOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ Білок-Лізин |
|
|
і кетогенними, лише лейцин і лізин є тільки кето- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
ПАМФ |
|
|
|
|
CH2 |
|
ПАМФ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
генними амінокислотами. Разом з тим, вуглецеві |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
COOH |
|
|
|
|
|
|
|
|
|
|
|
залишки амінокислот піддаються окисненню |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HOOC |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
COOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
|
|
|
NH2 |
+ Білок-Лізин |
шляхом залучення в цикл трикарбонових кислот |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
через піруват, ацетил-КоА, оксалоацетат, кето- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
H |
|
|
|
|
|
глутарову кислоту і сукциніл-КоА. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Існують мітохондріальні та цитоплазматичні |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
COOH |
|
|
|
|
ПАЛФ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
форми амінотрансфераз, зокрема АСТ, які від- |
|
|
|
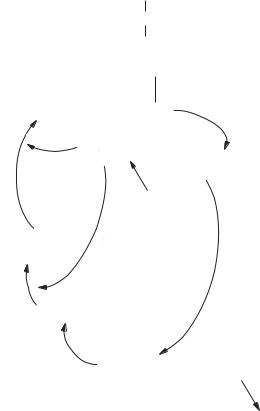
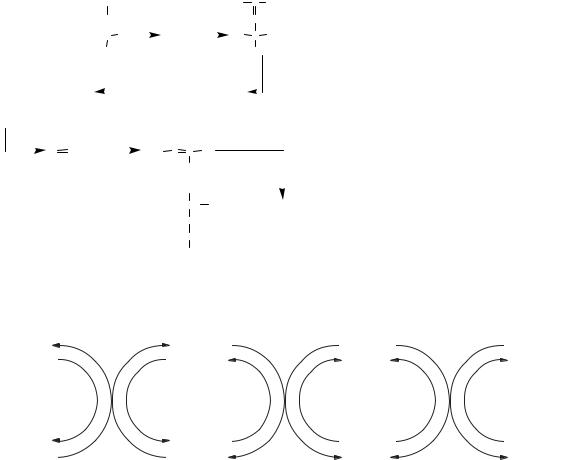
Рис. 11.2. Механізм трансамінування в тканинах |
різняються спрямованістю каталізованої реакції. |
|
|
|
|
|
|
|
|
|
|
|
Трансаміназа |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Глутаматдегідрогеназа |
Аміно- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ПАЛФ |
|
|
|
|
|
|
|
|
|
|
|
Глутамат |
+ НАД+ + НОН |
кислота |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
- НАД+ - NH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|