Материал: Біологічна та біоорганічна хімія_Мардашко О.О._ изд. 2008-342 с._ОНМедУ-2012

9. Типи інгібування ферментів: зворотне (кон- |
12. Ензимопатії — уроджені (спадкові) вади |
|
курентне, неконкурентне) та незворотне інгібу- |
метаболізму вуглеводів, амінокислот, порфіринів, |
|
вання. |
пуринів. |
|
10. Регуляція ферментативних процесів. Шля- |
13. Ензимодіагностика патологічних процесів |
|
і захворювань. |
||
хи і механізми регуляції: алостеричні ферменти; |
||
ковалентна модифікація ферментів. |
14. Ензимотерапія — застосування ферментів, |
|
їх активаторів та інгібіторів у медицині. |
||
|
||
11. Циклічні нуклеотиди (цАМФ, цГМФ) як |
15. Принципи та методи виявлення ферментів |
|
регулятори ферментативних реакцій і біологічних |
у біооб’єктах. Одиниці виміру активності й |
|
функцій клітини. |
кількості ферментів. |
Глава 7. ОСНОВНІ ЗАКОНОМІРНОСТІ ОБМІНУ РЕЧОВИН.
ЦИКЛ ТРИКАРБОНОВИХ КИСЛОТ
7.1. КАТАБОЛІЗМ, АНАБОЛІЗМ. |
нази вищих жирних кислот і амінокислот. На цій |
|
СПІЛЬНІ ШЛЯХИ ПЕРЕТВОРЕНЬ |
стадії, крім ацетил-КоА, утворюються відновлені |
|
БІЛКІВ, ВУГЛЕВОДІВ, ЛІПІДІВ |
коферменти НАД, ФАД, НАДФ, ФМН. Отже, і |
|
|
друга стадія катаболізму перебігає за участю |
|
|
ферментів, специфічних для вуглеводів, білків і |
|
Енергія в клітинах вивільнюється в процесі |
жирів. Тому ця стадія катаболізму також нази- |
|
катаболізму вуглеводів, жирів і білків. Розрізня- |
вається стадією специфічних реакцій. До таких |
|
ють три стадії катаболічних перетворень цих спо- |
процесів належать гліколіз, окиснення жирних |
|
лук. На першій стадії катаболізму білки гідролі- |
кислот, гліцеролу, дезамінування амінокислот. |
|
зуються на амінокислоти, полісахариди гідролі- |
Продукти, утворені на цій стадії, втрачають свою |
|
зуються переважно до глюкози, а також до |
специфічність (приналежність) до певного класу |
|
інших гексоз і пентоз, жири розпадаються на |
сполук (наприклад, піруват може утворювати- |
|
гліцерол, жирні кислоти й інші компоненти. На |
ся з глюкози, аланіну, гліцеролу; ацетил-КоА — |
|
цій стадії не відбувається вивільнення біологічно |
з пірувату і жирних кислот). |
|
корисної енергії. Катаболізм білків, жирів і вуг- |
Третя стадія катаболізму охоплює цикл |
|
леводів перебігає за участю специфічних для |
Кребса, тканинне дихання й окисне фосфорилу- |
|
кожної групи ферментів, в основному, представ- |
вання — це універсальний шлях окиснення |
|
ників класу гідролаз (гідролаз складних ефірів, |
білків, жирів і вуглеводів. Незалежно від того, з |
|
пептидних, глікозидних зв’язків), тобто відбува- |
яких речовин утворився ацетил-КоА, відновлені |
|
ються специфічні реакції катаболізму високомо- |
форми коферментів (НАДН, НАДФН, ФАДН2, |
|
лекулярних сполук до відповідних мономерів. |
ФМНН2), молекулярні механізми подальшого пе- |
|
Всі продукти, що утворилися на першій стадії |
ретворення цих сполук до СО2 і Н2О з виділенням |
|
катаболізму, на другій стадії перетворюються на |
енергії вже однакові. Тому третя стадія катабо- |
|
ще простіші сполуки, кількість яких порівняно |
лізму називається ще загальним шляхом катабо- |
|
невелика. Гексози, пентози й гліцерол розщеплю- |
лізму (стадією неспецифічних реакцій катаболіз- |
|
ються до піровиноградної кислоти (пірувату), що |
му). |
|
піддається окисному декарбоксилюванню й пере- |
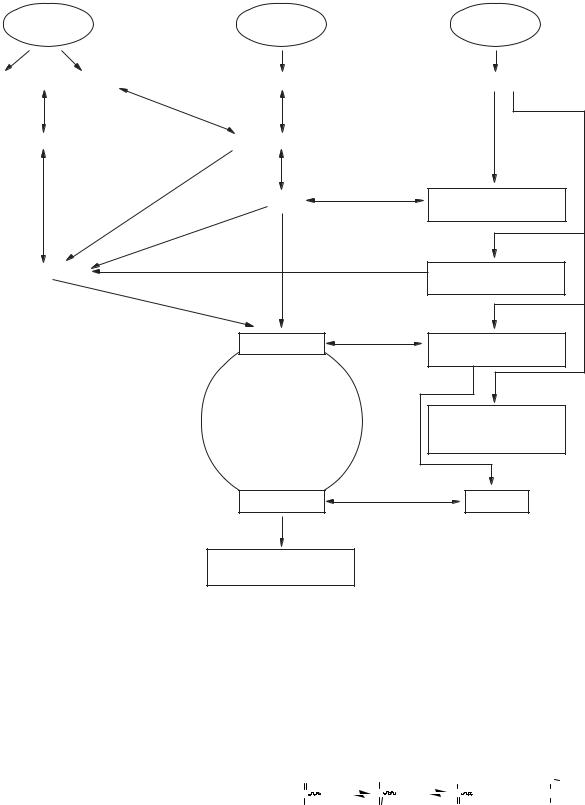
Катаболізм білків, вуглеводів і ліпідів ілюст- |
|
творюється на ацетил-КоА. Аналогічним пере- |
рує рис. 7.1. |
|
творенням піддаються амінокислоти. Жирні кис- |
|
|
лоти також розпадаються до ацетил-КоА. |
|
|
У процесі катаболізму білків, жирів і вугле- |
7.2. ЦИКЛ ТРИКАРБОНОВИХ |
|
водів відбувається відщеплення атомів Гідрогену, |
||
КИСЛОТ |
||
які через систему ферментів переносяться на ки- |
||
|
||
сень з утворенням води. Саме в ході цього пере- |
У результаті катаболізму вуглеводів, жирів і |
|
носу відбувається вивільнення енергії збуджених |
||
електронів. Отже, чим більше органічна речови- |
білків утворюється ацетил-КоА. Встановлено, що |
|
на містить атомів Гідрогену, які можуть відщеп- |
при катаболізмі цих сполук майже 100 % атомів |
|
лятися ферментативним шляхом і переноситися |
Карбону жирних кислот, близько 60 % атомів |
|
через систему каталізаторів на кисень, тим |
Карбону вуглеводів і близько 50 % атомів Кар- |
|
більша енергетична цінність цих речовин. |
бону амінокислот включається до ацетил-КоА. |
|
Відщеплення атомів Гідрогену від відповідних |
Утворений ацетил-КоА може окиснюватися в |
|
сполук починається на другій стадії в процесі |
циклі лимонної кислоти. Цей цикл був відкритий |
|
катаболізму. Його каталізують ферменти гліцер- |
англійським біохіміком Гансом Кребсом. За це |
|
альдегідфосфатдегідрогеназа, лактатдегідрогена- |
відкриття він був нагороджений Нобелівською |
|
за, глюкозо-6-фосфатдегідрогеназа, дегідроге- |
премією (1953), а цикл лимонної кислоти дістав |
99
Ліпіди |
Вуглеводи |
Білки |
Жирні кислоти + Гліцерол |
Глюкоза |
Амінокислоти |
Ацил КоА |
Гліцеральдегідфосфат |
|
|
Піруват |
Аланін, серин, треонін, |
|
|
цистеїн, валін |
Ацетил КоА |
|
Гліцин, лейцин, |
|
|
тирозин, фенілаланін |
|
Оксалоацетат |
Тирозин, фенілаланін, |
|
|
аспартат |
|
Цикл трикарбонових |
Аргінін, пролін, |
|
кислот |
оксипролін, гістидин, |
|
|
орнітин |
|
Кетоглутарат |
Глутамат |
Тканинне дихання, окисне фосфорилування
Рис. 7.1. Катаболізм білків, вуглеводів і ліпідів
назву циклу Кребса. Цикл лимонної кислоти називають також циклом трикарбонових кислот. Ця назва з’явилась у зв’язку з тим, що впродовж багатьох років після того, як Кребс постулював існування циклу, не було повної впевненості в тому, яка саме з трикарбонових кислот (лимонна або ізолимонна) є першим продуктом взаємодії ацетил-КоА з оксалоацетатом (щавлевооцтовою кислотою). Сьогодні точно відомо, що першою з трикарбонових кислот утворюється саме лимонна кислота (цитрат).
Цикл складається з 8 послідовних реакцій і перебігає в мітохондріях (рис. 7.2). Ацетил-КоА й оксалоацетат утворюються з пірувату в результаті його окисного декарбоксилювання під дією піруватдегідрогеназного комплексу і карбоксилювання під дією піруваткарбоксилази. Таким чином, з одного попередника — пірувату — утворюються два вихідних продукти циклу Кребса. Слід зазначити, що ацетил-КоА може утворюватися також у результаті окиснення ви-
щих жирних кислот, а оксалоацетат — внаслідок дезамінування аспартату (аспарагінової кислоти).
1-ша реакція — конденсація ацетил-КоА з оксалоацетатом з утворенням лимонної кислоти (цитрату) — цитратсинтазна реакція, яка відбувається в три стадії. На першій стадії ацетил-КоА перетворюється на енольну форму:
O |
OH |
|
|
|
|
O- |
O=C COOH |
|||
C S-KoA |
|
|
|
C |
S-KoA |
|
|
|
C S-KoA + H+ + CH2 |
|
|
|
|
|
|
|
|||||
CH3 |
CH2 |
|
|
|
|
CH2 |
COOH |
|||
Ацетил-КоА |
Енольна форма |
Оксалоацетат |
||||||||
|
|
|
|
|
ацетил-КоА |
|
||||
На другій стадії ацетил-КоА конденсується із оксалоацетату з утворенням активної форми лимонної кислоти — цитрил-КоА. Він утворюється в активному центрі ферменту цитратсинтази і швидко гідролізується на цитрат і НS-КоА (третя стадія першої реакції).
100

|
|
|
|
|
|
|
|
|
|
|
O |
|
Ацетил-КоА |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
= |
|
|
|
|
|
|
COOH |
|
|
|
|
|
|
|
|
|
|
|
COOH |
|||||||||||||||||||||||||||||||
CH –C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||
3 ~ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
SKoA |
+ |
|
|
|
- НОН |
|
|
CH2 |
|
|
+ НОН |
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|||||||||||||||
O=C–COOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
Оксалоацетат |
|
|
|
|
|
С |
|
СООН |
|
|
|
Н |
|
|
С |
|
СООН |
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
CH2–COOH |
|
1. Цитратсинтаза |
|
|
|
|
|
СН |
|
|
|
|
|
|
|
|
HC |
|
ОН |
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
CH2–COOH |
|
|
|
|
|
|
СООН |
|
|
|
|
|
|
|
|
|
|
|
СООН |
||||||||||||||||||||||||||||||
|
|
|
|
|
Цис-аконітова кислота |
|
Ізоцитрат |
|||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||
HO–C–COOH |
|
Цитрат |
|
|||||||||||||||||||||||||||||||||||||||||||||||
|
|
CH2–COOH |
|
2. Аконітаза |
Далі цис-аконітат приєднує молекулу води й |
|||||||||||||||||||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||
CH2–COOH |
|
перетворюється на ізоцитрат. Суть реакції поля- |
||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
Ізоцитрат |
гає в «рокіровці». Динамічна рівновага цієї ре- |
||||||||||||||||||||||||||||||||||||||||||||||
H–C–COOH |
|
|||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
акції встановлюється при співвідношенні: цитра- |
|||||||||||||||||||||||||||||||||
HO–C–COOH |
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ту 90 %, ізоцитрату — 8 % і цис-аконітату — |
|||||||||||||||||||||||||||||||||
H |
|
|
|
3. Ізоцитратдегідрогеназа |
||||||||||||||||||||||||||||||||||||||||||||||
|
|
НАД+ |
2 %. Біологічний сенс такого співвідношення ме- |
|||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
COOH |
|
|||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
таболітів полягає в тому, що цитрат має здат- |
|||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
ність виходити з мітохондрій у цитоплазму, ре- |
|||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
CH2 |
|
α -Кетоглутарат |
гулюючи у такий спосіб потік метаболітів по цик- |
||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
лу Кребса. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
C=O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
4. α -Кетоглутарат- |
3-тя реакція — перетворення ізоцитрату на α - |
|||||||||||||||||||||||||||||||||||
|
|
|
|
COOH |
|
НАД+ |
||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
кетоглутарат через оксалосукцинат (ізоцитрат- |
|||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
COOH |
|
|
|
|
дегідрогеназний |
||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
дегідрогеназна реакція). Протягом цієї реакції ізо- |
|||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
комплекс |
|||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
цитрат окиснюється шляхом відщеплення двох |
|||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
CH2 |
|
Сукциніл-КоА |
атомів Гідрогену й перетворюється на оксалосук- |
||||||||||||||||||||||||||||||||||||||||
O=C |
|
~SKoA |
|
|
|
|
цинат. Остання декарбоксилюється до α -кето- |
|||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
5. Сукциніл-КоА-синтетаза |
глутарату. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
Сукциніл- |
|
|
(тіокіназа) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
COOH |
|
фосфат~ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
COOH |
|
|
|
|
|
|
|
COOH |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
CH2 |
|
|
|
|
|
|
|
|
+ НАД(Ф)+ |
|
|
|
CH2 |
|
|
|
|
|
|
|
|
СН2 |
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
Сукцинат |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Н |
|
С |
|
СООН |
|
СН2 |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
- СО2 |
||||||||||||||||||||||||
|
|
|
|
CH2 |
|
|
|
- НАД(Ф)Н + Н+ |
|
|
||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
COOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
С |
|
О |
|
|
|
|
|
|
|
С |
|
О |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
ФАД |
6. Сукцинатдегідрогеназа |
|
|
|
|
|
|
|
|
|
|
|
|
|
СООН |
|
|
|
|
|
|
|
СООН |
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
COOH |
|
|
|
|
|
|
|
|
|
|
Оксалосукцинат α |
-Кетоглутарат |
||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||
|
|
|
CH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
Фумарат |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
= |
|
|
|
|
|
|
|
Цю реакцію, тобто перетворення ізоцитрату |
||||||||||||||||||||||||||||||||||||||||||
HC |
|
|
||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||
|
|
|
COOH |
|
|
7. Фумараза |
на оксалосукцинат і декарбоксилювання остан- |
|||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
COOH |
|
|
нього до α |
-кетоглутарату, каталізує ізоцитрат- |
||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
дегідрогеназа. Існує два типи ізоцитратдегідро- |
|||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||
HO–CH |
|
L-Малат |
генази: один використовує як акцептор протонів |
|||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
8. Малатдегідрогеназа |
і електронів НАД+, а другий — НАДФ+. У міто- |
||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
НАД+ |
хондріях існують ізоцитратдегідрогенази обох |
||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
COOH |
|
|||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
COOH |
|
|
|
|
|
типів: НАД+-залежна й НАДФ+-залежна; НАД+- |
||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
залежна зустрічається тільки в мітохондріях, а |
|||||||||||||||||||||||||||||||||||||
O=C |
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||
|
|
|
Оксалоацетат |
НАДФ+-залежна — як у мітохондріях, так і в ци- |
||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
топлазмі. У циклі Кребса, можливо, беруть |
|||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
участь обидва мітохондріальних ферменти, але |
||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
COOH |
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||
|
|
Рис. 7.2. Схема циклу трикарбонових кислот |
переважає НАД+-залежна ізоцитратдегідрогена- |
|||||||||||||||||||||||||||||||||||||||||||||||
|
|
за. Регуляторна роль ізоцитратдегідрогеназної |
||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||
Каталізує всі три стадії першої реакції (утво- |
реакції полягає в тому, що вона забезпечує спря- |
|||||||||||||||||||||||||||||||||||||||||||||||||
рення енольної форми ацетил-КоА, конденсацію |
мованість метаболізму по катаболічному або |
|||||||||||||||||||||||||||||||||||||||||||||||||
і гідроліз) фермент цитратсинтаза. |
анаболічному шляху залежно від форми кофер- |
|||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ментів, що утворюються. Участь НАДФ+-залеж- |
|||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
O |
ної ізоцитратдегідрогенази, імовірно, дозволяє |
|||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
C |
|
S-KoA |
|
|
C OH |
циклу працювати «на холостому ходу», даючи |
|||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
CH2 |
можливість використовувати НАДФН для біо- |
||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
HOOH C COOH + HOH |
|
|
НО C COOH + HS-KoA |
синтетичних процесів. Гальмування активності |
||||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
CH2 |
|||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ізоцитратдегідрогенази спричинює нагрома- |
||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
COOH |
|
|
COOH |
||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
дження цитрату й вихід його з мітохондрій у ци- |
|||||||||||||||||||||||||||||||||||||
|
|
|
|
Цитрил-КоА |
|
|
Цитрат |
|||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
топлазму, де він може перетворюватися на окса- |
||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||
|
2-га реакція — перетворення цитрату на ізо- |
лоацетат і ацетил-КоА, що йде на біосинтетичні |
||||||||||||||||||||||||||||||||||||||||||||||||
цитрат через цис-аконітат (аконітатгідратазна |
процеси, а також на утворення розчинного цит- |
|||||||||||||||||||||||||||||||||||||||||||||||||
реакція). У цій реакції цитрат піддається дегідра- |
рату Са2+, необхідного для системи згортання |
|||||||||||||||||||||||||||||||||||||||||||||||||
тації й перетворюється на цис-аконітову кисло- |
крові й забезпечення функцій нервової тканини. |
|||||||||||||||||||||||||||||||||||||||||||||||||
ту. Ця сполука пов’язана з ферментом аконіта- |
НАДФ+-залежна ізоцитратдегідрогеназа ка- |
|||||||||||||||||||||||||||||||||||||||||||||||||
зою і в нормі не відділяється від активного цент- |
талізує карбоксилювання α -кетоглутарату. Дже- |
|||||||||||||||||||||||||||||||||||||||||||||||||
ру цього ферменту. |
|
|
|
релом Карбону в цій реакції звичайно служить |
||||||||||||||||||||||||||||||||||||||||||||||
101

глутамат; трансамінування його приводить до |
6-та реакція — дегідрування сукцинату з ут- |
|||||||||||||||||||||||||||||||||||||||||||||
утворення α -кетоглутарату. Атоми Гідрогену, |
воренням фумарату. |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||
зв’язані з НАД+ (НАДН+Н+), далі переносяться |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
по ланцюгу дихальних ферментів на кисень з |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
утворенням Н2О, тобто процес іде по шляху |
|
|
|
|
|
|
|
COOH |
COOH |
|
|
|
|
|
|
|
|
|
|
COOH |
||||||||||||||||||||||||||
катаболізму. Атоми Гідрогену, зв’язані з НАДФ+ |
|
+ ФАД |
|
|
НС |
|
+ НОН |
СНОН |
|
+ НАД |
С О |
|||||||||||||||||||||||||||||||||||
(НАДФН+Н+), як правило, використовуються |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
- ФАДН2 |
|
|
|
СН |
|
СН2 |
|
- НАДН+ Н+ |
|
СН2 |
|||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||
по шляху біосинтезу різних сполук (вищих жир- |
|
|
|
|
|
|
|
СООН |
|
СООН |
|
|
|
|
|
|
|
|
|
|
СООН |
|||||||||||||||||||||||||
них кислот, холестеролу, стероїдних гормонів |
|
|
|
|
|
Фумарат |
L-Малат Оксалоацетат |
|||||||||||||||||||||||||||||||||||||||
тощо), тобто процес іде по шляху анаболізму. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
4-та реакція — окисне декарбоксилювання α - |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
кетоглутарату кислоти до сукциніл-КоА. У цій |
Окиснення сукцинату каталізує сукцинатде- |
|||||||||||||||||||||||||||||||||||||||||||||
реакції α -кетоглутарат піддається такому ж |
гідрогеназа, у молекулі якої з білком ковалентно |
|||||||||||||||||||||||||||||||||||||||||||||
складному окисному декарбоксилюванню, як і |
зв’язаний кофермент ФАД, |
що служить акцеп- |
||||||||||||||||||||||||||||||||||||||||||||
піруват, але утворюється не ацетил-КоА, а сук- |
тором Гідрогену в даній реакції. Сукцинатдегід- |
|||||||||||||||||||||||||||||||||||||||||||||
циніл-КоА. Сумарно дану реакцію можна запи- |
рогеназа — єдиний фермент циклу, зв’язаний із |
|||||||||||||||||||||||||||||||||||||||||||||
сати так: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
внутрішньою мембраною мітохондрій, решта ре- |
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
COOH |
акцій відбуваються в матриксі. |
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
7-ма реакція — гідратація фумарату з утво- |
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
СН2 |
||||||||||||||||||||||||||||||
|
+ ТПФ + ЛК + HS-KoA + ФАД + НАД+ |
ренням малату. Під час цієї оборотної реакції фу- |
||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||
|
СН2 |
|||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
- СО |
- НАДН + Н |
+ |
|
|
|
марова кислота приєднує молекулу води й пере- |
||||||||||||||||||||||||||||||||||||
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
O |
творюється на малат. Каталізує реакцію фума- |
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
SKoA |
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ратгідратаза (фумараза). Цей фермент має сте- |
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Сукциніл-КоА |
реоспецифічну дію: він гідратує тільки трансфор- |
|||||||||||||||||||||||||||||||
Сукциніл-КоА, що утворився, має макро- |
му подвійного зв’язку фумарової кислоти й не діє |
|||||||||||||||||||||||||||||||||||||||||||||
на цис-форму — малеїнову кислоту. |
||||||||||||||||||||||||||||||||||||||||||||||
ергічний карбоксил-тіоловий (тіоефірний) зв’я- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
зок, у якому резервується енергія окисного декар- |
|
|
HC |
|
COOH |
|
|
|
|
HC |
|
COOH |
||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||
боксилювания. Каталізує цю реакцію α -кетоглу- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||
|
|
HC—COOH |
|
HOOC |
|
|
CH |
|
|
|||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||
таратдегідрогеназний комплекс. За структурою |
Малеїнова кислота |
|
Фумарова кислота |
|||||||||||||||||||||||||||||||||||||||||||
і функцією цей комплекс дуже нагадує піруват- |
|
|||||||||||||||||||||||||||||||||||||||||||||
дегідрогеназний комплекс, він включає також |
У зворотній реакції (L-малат → |
|
|
|||||||||||||||||||||||||||||||||||||||||||
зв’язані з ферментами такі коферменти, як НАД+, |
фумарат) фу- |
|||||||||||||||||||||||||||||||||||||||||||||
ФАД, ТПФ, НSКоА й ліпоєву кислоту. |
мараза виявляє специфічність відносно оптично- |
|||||||||||||||||||||||||||||||||||||||||||||
5-та реакція — перетворення сукциніл-КоА |
го ізомеру L-малату, тобто каталізує дегідрата- |
|||||||||||||||||||||||||||||||||||||||||||||
на сукцинат через сукцинілфосфат (сукциніл- |
цію L-малату, але не діє на D-малат. |
|||||||||||||||||||||||||||||||||||||||||||||
КоА-синтетазна реакція). Протягом цієї реакції |
8-ма реакція — дегідрування малату з утво- |
|||||||||||||||||||||||||||||||||||||||||||||
спочатку сукциніл-КоА реагує з неорганічним |
ренням оксалоацетату — малатдегідрогеназна |
|||||||||||||||||||||||||||||||||||||||||||||
фосфатом і перетворюється на сукцинілфосфат. |
реакція. У ході цієї реакції L-малат втрачає два |
|||||||||||||||||||||||||||||||||||||||||||||
|
|
|
ОН |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
атоми Гідрогену (окиснюється) і перетворюється |
||||||||||||||||||||||||||||
|
|
|
|
|
COOH |
|
|
|
|
|
|
|
на оксалоацетат. Молекула оксалоацетату, що |
|||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
COOH |
|||||||||||||||||||||||||||||||
+ HO |
|
Р |
|
О |
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||
|
|
|
|
СН2 |
|
|
|
|
|
|
|
|
утворилася, може знову вступати в реакцію з |
|||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
ОН |
|
|
|
|
+ГДФ |
|
|
|
СН2 |
||||||||||||||||||||||||||||||||||
|
|
|
|
|
СН2 |
|
|
|
|
іншою молекулою ацетил-КоА, і процес розпочи- |
||||||||||||||||||||||||||||||||||||
|
- HSKoA |
|
|
|
|
|
-ГТФ |
|
|
|
|
|||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
СН |
|||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ОН |
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
С |
|
О |
нається спочатку. Каталізує реакцію малатде- |
|||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
СООН |
||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
О |
|
|
Р О |
|
||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
гідрогеназа, коферментом якої є НАД+. НАД+- |
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ОН |
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
Сукцинілфосфат Сукцинат |
залежна малатдегідрогеназа перебуває в мат- |
|||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
риксі мітохондрій. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
При цьому вивільняється НSКоА. Сукциніл- |
Відщеплення Гідрогену відбувається в чоти- |
|||||||||||||||||||||||||||||||||||||||||||||
рьох реакціях циклу Кребса — ізоцитратдегід- |
||||||||||||||||||||||||||||||||||||||||||||||
фосфат також має макроергічний, але не карбок- |
рогеназній, α |
-кетоглутаратдегідрогеназній, сук- |
||||||||||||||||||||||||||||||||||||||||||||
силтіоловий, а карбоксилфосфатний зв’язок. |
цинатдегідрогеназній і малатдегідрогеназній. |
|||||||||||||||||||||||||||||||||||||||||||||
Далі сукцинілфосфат реагує із ГДФ і перетво- |
||||||||||||||||||||||||||||||||||||||||||||||
Усього відщеплюються вісім атомів Гідрогену. |
||||||||||||||||||||||||||||||||||||||||||||||
рюється на сукцинат, а ГДФ, приєднавши фос- |
За один оборот циклу відбуваються дві реакції |
|||||||||||||||||||||||||||||||||||||||||||||
фат, перетворюється на ГТФ. Реакцію перетво- |
приєднання води. Одна молекула води при- |
|||||||||||||||||||||||||||||||||||||||||||||
рення сукциніл-КоА на сукцинат каталізує фер- |
єднується при гідролізі цитрил-КоА (у цитрат- |
|||||||||||||||||||||||||||||||||||||||||||||
мент сукциніл-КоА-синтетаза. Утворений у сук- |
синтазній реакції), а друга — при перетворенні |
|||||||||||||||||||||||||||||||||||||||||||||
циніл-КоА-синтетазній реакції ГТФ може потім |
фумарату на малат. У цих двох реакціях беруть |
|||||||||||||||||||||||||||||||||||||||||||||
передавати свою кінцеву фосфатну групу на |
участь чотири атоми Гідрогену двох молекул |
|||||||||||||||||||||||||||||||||||||||||||||
АДФ з утворенням АТФ; ця оборотна реакція |
води. Таким чином, за рахунок окиснення оц- |
|||||||||||||||||||||||||||||||||||||||||||||
каталізується нуклеозиддифосфаткіназою: |
тової кислоти вивільняються чотири атоми |
|||||||||||||||||||||||||||||||||||||||||||||
ГТФ + АДФ → |
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||
|
|
ГДФ + АТФ |
Гідрогену, тобто всі атоми, які входять до скла- |
|||||||||||||||||||||||||||||||||||||||||||
Отже, енергія окисного декарбоксилювання |
ду її молекули. Отже, у результаті реакцій одно- |
|||||||||||||||||||||||||||||||||||||||||||||
α -кетоглутарату |
остаточно може резервувати- |
го обороту циклу Кребса оцтова кислота окис- |
||||||||||||||||||||||||||||||||||||||||||||
ся в АТФ (субстратне фосфорилування). |
нюється з виділенням чотирьох атомів Гідроге- |
|||||||||||||||||||||||||||||||||||||||||||||
ну й двох молекул СО2. |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
102
Енергетичний баланс циклу |
3. Біосинтез ВЖК, холестеролу. Цитрат може |
|||
трикарбонових кислот |
|
виходити з мітохондрій у цитозоль, де розщеп- |
||
Цикл Кребса забезпечує організм енергією. |
люється з утворенням оксалоацетату та цито- |
|||
зольного ацетил-КоА, який надходить у систему |
||||
Від чотирьох проміжних продуктів циклу Креб- |
синтезу вищих жирних кислот, холестеролу. |
|||
са відділяються чотири пари атомів Гідрогену. Із |
4. Біосинтез гему. Сукциніл-КоА може вико- |
|||
них три пари атомів Гідрогену переносяться на |
||||
ристовуватися для біосинтезу порфіринів, що вхо- |
||||
НАД+, що є коферментом ізоцитратдегідрогена- |
дять до складу гему гемоглобіну, й в інші сполу- |
|||
зи, α -кетоглутаратдегідрогенази й малатдегідро- |
ки. Відтік проміжних продуктів циклу Кребса |
|||
генази. Далі ці атоми Гідрогену від НАДН+Н+ |
поповнюється завдяки дії іншого набору фер- |
|||
передаються на ланцюг дихальних ферментів і в |
||||
ментів. |
||||
остаточному підсумку відновлюють дві молеку- |
Спеціальні реакції, що забезпечують попов- |
|||
ли О2 з утворенням трьох молекул Н2О. |
||||
нення пулу проміжних продуктів циклу Кребса, |
||||
При окисненні однієї молекули НАДН+Н+ за |
||||
участю дихальних ферментів утворюються три |
дістали назву анаплеротичних (поповнюючих) |
|||
реакцій. Найважливіша реакція такого роду в |
||||
молекули АТФ, а всього — 9 молекул АТФ. Одна |
тваринних тканинах — це карбоксилювання |
|||
пара атомів Гідрогену потрапляє на дихальний |
пірувату за рахунок СО2 з утворенням оксало- |
|||
ланцюг через ФАД (кофермент сукцинатдегідро- |
ацетату: |
|||
генази), у результаті утворюються 2 молекули |
Піруват + СО2 + АТФ + Н2О → |
|||
АТФ. Одна молекула АТФ синтезується із ГТФ, |
||||
що утворюється в сукциніл-КоА-синтетазній ре- |
→ Оксалоацетат + АДФ + Н3РО4 + 2Н+. |
|||
акції (субстратне фосфорилування). |
Каталізує цю реакцію фермент піруваткар- |
|||
1. Ізоцитратдегідрогеназа |
||||
1 НАДН+Н+ → |
3 АТФ |
боксилаза. Ця реакція — головна анаплеротич- |
||
на реакція в печінці й нирках. У міокарді та м’я- |
||||
2. α -Кетоглутаратдегідрогеназа |
зах анаплеротичною є фосфоенолпіруваткарбок- |
|||
1 НАДН+Н+ |
→ |
3 АТФ |
сикіназна реакція: |
|
Фосфоенолпіруват + СО2 + ГДФ → |
||||
3. Сукцинілфосфат |
|
|
||
|
|
→ Оксалоацетат + ГТФ. |
||
1 ГТФ → |
1 АТФ |
|||
У цій реакції відбувається розщеплення мак- |
||||
4. Сукцинатдегідрогеназа |
||||
роергічної сполуки фосфоенолпірувату, що утво- |
||||
|
|
|
||
1 ФАДН2 → |
|
2 АТФ |
рився в процесі гліколізу. Енергія, що вивіль- |
|
5. Малатдегідрогеназа |
|
няється, використовується для карбоксилювання |
||
|
з утворенням оксалоацетату, а її залишок запа- |
|||
|
|
|
||
1 НАДН+Н+ → |
3 АТФ |
сається у формі ГТФ. |
||
Отже, при окисненні однієї молекули ацетил- |
Атоми Гідрогену відновленої форми НАДФ |
|||
(НАДФН+Н+), що утворюються в ізоцитратде- |
||||
КоА в циклі Кребса утворюються 12 молекул |
гідрогеназній реакції, можуть використовувати- |
|||
АТФ. |
|
|
ся для біосинтезу вищих жирних кислот, стероїд- |
|
|
|
|
них гормонів, холестеролу, нуклеотидів й інших |
|
Амфіболічні й анаплеротичні реакції |
речовин. |
|||
|
||||
Проміжні продукти циклу Кребса можуть бра- |
Регуляція циклу трикарбонових кислот |
|||
|
||||
ти участь у реакціях біосинтезу багатьох орга- |
Активність ключових ферментів циклу Креб- |
|||
нічних сполук. |
|
|
са й процесу в цілому контролюється енергетич- |
|
1. Біосинтез білка. Оскільки цикл може функ- |
ним статусом клітини. Негативним модулятором |
|||
ціонувати як катаболічний шлях, а також і як |
виступає високий рівень АТФ, тоді цитрат не ме- |
|||
джерело сполук для анаболічних шляхів, то його |
таболізується в ЦТК, а виходить із мітохондрій |
|||
часто називають амфіболічним шляхом (від |
у цитоплазму, де розпадається на оксалоацетат |
|||
грецьк. аmphi — обидва). α -Кетоглутарат і ок- |
і ацетил-КоА, що бере участь у біосинтезі вищих |
|||
салоацетат можуть видалятися з циклу й вико- |
жирних кислот і холестеролу. Ацетил-КоА, що не |
|||
ристовуватися як попередники амінокислот глу- |
окиснюється в мітохондріях у результаті гальму- |
|||
тамінової й аспарагінової, глутаміну й аспара- |
вання ЦТК, може переходити в цитоплазму за |
|||
гіну, решта — для біосинтезу білків, азотистих |
допомогою карнітинового човникового механіз- |
|||
основ, нуклеотидів, нуклеїнових кислот й інших |
му й брати участь у біосинтетичних процесах. |
|||
сполук. |
|
|
Однак гальмування реакцій ЦТК може відбува- |
|
2. Біосинтез глюкози. Оксалоацетат є вихід- |
тися в результаті порушення функції окисно- |
|||
ним продуктом глюконеогенезу. Оксалоацетат |
відновних ферментів при різних патологічних |
|||
і α -кетоглутарат утворюються в результаті |
процесах (наприклад цукровий діабет), тоді аце- |
|||
дезамінування аспарагінової й глутамінової |
тил-КоА, незважаючи на дефіцит макроергів у |
|||
кислот, а фумарова кислота — у циклі синтезу |
клітині, синтезує холестерол, тому при цукрово- |
|||
сечовини. |
|
|
му діабеті прогресує атеросклероз. |
|
103