Материал: Біологічна та біоорганічна хімія_Мардашко О.О._ изд. 2008-342 с._ОНМедУ-2012
КОНТРОЛЬНІ ПИТАННЯ |
3. Цикл трикарбонових кислот. Локалізація, |
|
|
1. Обмін речовин (метаболізм) — загальні за- |
послідовність ферментативних реакцій, значення |
кономірності перебігу катаболічних і анаболіч- |
в обміні речовин. |
них процесів. |
4. Енергетичний баланс циклу трикарбоно- |
2. Спільні стадії внутрішньоклітинного ката- |
вих кислот. Фізіологічне значення реакцій |
болізму біомолекул: білків, вуглеводів, ліпідів. |
ЦТК. |
Глава 8. МОЛЕКУЛЯРНІ ОСНОВИ БІОЕНЕРГЕТИКИ
8.1. БІОЕНЕРГЕТИЧНІ ПРОЦЕСИ: БІОЛОГІЧНЕ ОКИСНЕННЯ, ОКИСНЕ ФОСФОРИЛУВАННЯ, СИНТЕЗ АТФ
Відомо, що процеси утворення клітин, скорочення м’язів, пересування, передачі нервового імпульсу, осмосу, всмоктування поживних речовин, синтез органічних сполук тощо потребують витрати енергії. Клітини отримують необхідну енергію в процесі окиснення органічних сполук. Ще в серединіXVIII ст. Ломоносов і Лавуазьє висловлювали припущення, що між процесами горіння органічних сполук і процесами їхнього окиснення в організмі багато спільного. Надалі виявилося, що між горінням і окисненням органічних сполук в організмі існують істотні розбіжності:
1.Процеси горіння органічних сполук перебігають при температурі 100 °С і вище, а для окиснення їх у клітині оптимальна температура
—35–39 °С. Біологічне окиснення — це, по суті, горіння без вогню, або низькотемпературне горіння.
2.Процеси горіння перебігають у повітряному середовищі, у присутності достатньої кількості кисню, а окиснення — як правило, у водному середовищі. На відміну від горіння, біологічне окиснення може відбуватися не тільки в аеробних, але й в анаеробних умовах, тобто без участі кисню.
3.Горіння органічних сполук супроводжується виділенням великої кількості енергії у вигляді тепла і світла. При окисненні органічних сполук енергія перетворюється не тільки на тепло, але й на інші види біологічної енергії — м’язове скорочення, нервову провідність, акумулюється в АТФ і т. ін.
4.Біологічне окиснення органічних сполук може відбуватися кількома шляхами:
а) відщепленням від субстратів атомів Гідрогену, тобто шляхом дегідрування субстратів;
б) відщепленням від субстратів електронів; в) приєднанням до органічних сполук Окси-
гену, якщо при цьому відбувається перенос електронів із речовини, що окиснюється, на молекулу кисню (наприклад, мікросомальне окиснення).
Приєднання кисню до гемоглобіну не можна вважати окисненням, оскільки Ферум гемоглобіну не змінює при цьому валентності.
Більшість реакцій біологічного окиснення перебігає шляхом дегідрування, тобто відщеплення атомів Гідрогену. Якщо акцептором Гідрогену є кисень, то процес називається аеробним окисненням. Якщо ж акцептором Гідрогену є якась інша речовина, то процес окиснення називається анаеробним окисненням. Наприклад, при окисненні ацетил-КоА у ЦТК атоми Гідрогену відщеплюються від субстратів ЦТК і переносяться по ланцюгу дихальних ферментів на кисень з утворенням Н2О. Прикладом анаеробного окиснення може бути окиснення гліцераль- дегід-3-фосфату в 1,3-бісфосфогліцерат. При цьому атоми Гідрогену від гліцеральдегід-3-фосфату приєднуються до НАД+ (кофермент гліцеральдегідфосфатдегідрогеназа), перетворюючи його на НАДН+Н+, потім 2Н+ у анаеробних умовах переносяться на піруват, який перетворюється на лактат.
O |
|
|
|
|
O |
HO O |
C H |
+ НАД+ + H PO |
C O |
P OH |
|||
|
|
|
||||
HC OH OH |
3 |
4 |
HC OH OH |
|||
|
- НАДH + H+ |
|
|
|||
CH2 O P O |
|
|
|
|
CH2 |
O P=O |
OH |
|
|
|
|
|
OH |
Гліцеральдегід-3-фосфат 1,3-Бісфосфогліцерат
|
CH3 |
+ НАДH + H+ |
|
CH3 |
||||||
|
|
|
|
|
|
|||||
C |
|
O |
|
|
|
|
|
|
CHOH |
|
|
|
|
|
|
|
|
||||
|
|
|
- НАД+ |
|
|
|||||
|
|
|
|
|
|
|||||
COOH |
|
|
|
COOH |
||||||
Піруват |
Лактат |
|||||||||
Окиснення гліцеральдегід-3-фосфату й відновлення НАД+ до НАДН+Н+, окиснення НАДН+ +Н+ і відновлення пірувату до лактату становлять гліколітичну оксидоредукцію.
Важливим етапом аеробного окиснення є тканинне дихання — багатоступінчастий ферментативний процес переносу протонів і електронів по ланцюгу дихальних ферментів до кисню.
Біохімічні механізми тканинного дихання
Як відомо, для аеробного окиснення необхідний кисень. Однак атмосферний молекулярний кисень при звичайних умовах має інертні властивості і є поганим окисником органічних сполук. Виникли труднощі в поясненні участі інерт-
104
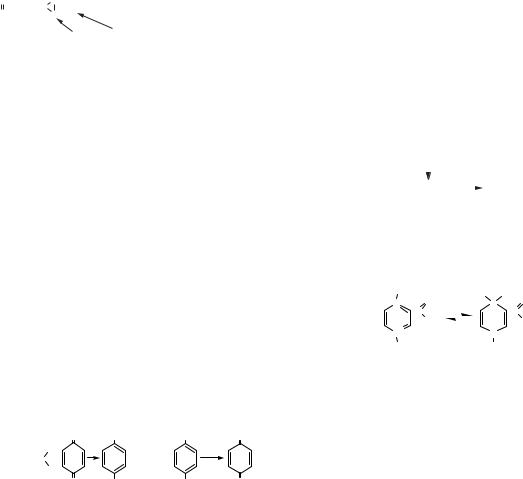
ного кисню в біологічному окисненні. У 1897 р. О. М. Бах сформулював теорію, що пояснює механізм активації кисню (перекисна теорія О. М. Баха). Він вважав, що для активації кисню необхідно розірвати одну з валентностей у його молекулі. Це здійснюється ненасиченими, легко окиснюваними органічними сполуками, які він назвав оксигеназами. У результаті сполучення оксигеназ із киснем утворюються органічні перекиси, вони з’єднуються з ферментом пероксидазою, яка утворює комплекс з атомарним Оксигеном.
O |
+ R → |
R O |
+ 2P → 2P–O + R → P–O + Субстрат→ Субстрат–О |
О |
|
O |
|
ОксиОрганічні Перокгенази перекиси сидаза
Недоліки теорії полягали в тому, що ці досліди проводилися на рослинах. Піддавалися окисненню феноли, яких багато в рослинах, але у тканинах тварин це не головний субстрат окиснення.
У1907–1912 рр. була розроблена й експериментально підтверджена теорія В. І. Палладіна, що пояснювала механізм тканинного дихання. Ця теорія дістала назву теорія дегідрування субстратів. В. І. Палладін припустив, що окиснення субстратів здебільшого відбувається шляхом дегідрування, тобто відщепленням Гідрогену, а кисень є тільки акцептором Гідрогену.
Уклітинах рослин В. І. Палладін виявив особливі пігменти хромогени, які можуть перебувати у двох формах: а) відновлена (наприклад гідрохінон) — безбарвна; б) окиснена (наприклад хінон) — кольорова.
Процес окиснення, за теорією Палладіна, розпочинається з дегідрування субстрату, який передає атоми Гідрогену на хромогени (наприклад на хінон), хінон відновлюється і перетворюється на інший хромоген — гідрохінон, а субстрат окиснюється.
O |
OH |
OH |
|
O |
H |
+ Sub |
|
+ 1/2O2 |
|
Sub + |
|
|
+ H2O |
|
H |
|
|
|
|
O |
OH |
OH |
|
O |
Хінон Гідрохінон Гідрохінон Хінон
Гідрохінон — нестійка сполука, за участю оксидази його Гідроген з’єднується з киснем з утворенням Н2О. Гідрохінон при цьому перетворюється на хінон і т. ін. Палладін також довів, що процес окиснення шляхом відщеплення атомів Гідрогену може відбуватися і без кисню, тобто в анаеробних умовах, якщо є інший (не кисень) акцептор Гідрогену. Як акцептор Гідрогену вчений використовував метиленову синь.
Сучасна теорія механізму тканинного дихання
Сучасна теорія механізму тканинного дихання сформувалася на основі досліджень Баха, Палладіна, Віланда, Варбурга, Скулачова, Се-
веріна, Ленінджера та ін. Процес складається з кількох етапів.
І етап — дія нікотинамідних ферментів
Перший етап тканинного дихання — дія нікотинамідних ферментів. Процес біологічного окиснення починається з дегідрування субстратів (наприклад, ізоцитрат, малат, β -гідроксіацил- КоА, глутамат та ін.).
Процес дегідрування каталізується ферментами дегідрогеназами. Якщо вони забирають атоми Гідрогену від субстратів і передають їх якомусь проміжному акцептору (наприклад, на ФФ
— флавінові ферменти), тоді вони називаються анаеробними дегідрогеназами. Коферментом цих дегідрогеназ є НАД+ або НАДФ+, що мають у своїй структурі амід нікотинової кислоти. Тому всі ферменти, які містять як кофермент НАД+ або НАДФ+, називаються нікотинамідними ферментами (це понад 150 ферментів).
Отже, схематично перший етап тканинного дихання за участю дегідрогеназ можна представити так:
|
|
2Н+ 2e |
|
|
|
|
Cуб.Н |
2 |
+ НАД(Ф)+ |
|
Cуб. + НАД(Ф)Н+ Н+ |
||
|
||||||
|
|
|
|
|
|
|
Урезультаті цієї реакції окиснюється субстрат
івідновлюється НАД(Ф)+. Протони та електрони, що надходять від субстратів, приєднуються до аміду нікотинової кислоти НАД(Ф)+.
H |
|
|
|
|
|
H |
H |
|
|
C O |
|
|
|
O |
|||||
|
|
|
C |
|
|
||||
|
|
C NH2 |
+ 2H |
|
|
C NH2 + H+ |
|||
|
|
|
|
||||||
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
||
N+ |
|
- 2H |
|
|
|||||
|
|
|
|
|
N |
|
|
|
|
R |
|
|
|
|
|
R |
|
|
|
НАД(Ф)+ |
|
|
НАД(Ф)Н + Н+ |
||||||
Було встановлено, що один протон і один електрон стають у пара-положення відносно Нітрогену піридинового кільця. Другий електрон нейтралізує протилежний за знаком заряд Нітрогену в нікотинамідному кільці, а один протон залишається в розчині. Вважають, що він підкислює середовище.
ІІ етап — дія флавінових ферментів
Флавінові ферменти можуть приймати Гідроген від нікотинамідних ферментів, тобто від відновлених форм НАД+ або безпосередньо від субстратів (наприклад, сукцинату, ацил-КоА, ксантину та ін.). Здебільшого флавінові ферменти одержують Гідроген від нікотинамідних ферментів, тобто відновлених НАД+. Сукцинатдегідрогеназа, ацил-КоА-дегідрогеназа, оксидаза L-амінокислот тощо приймають атоми Гідрогену безпосередньо від відповідних субстратів, тому належать до дегідрогеназ першого порядку.
Флавінові ферменти можуть передавати свої електрони на цитохроми (тоді вони називаються анаеробними дегідрогеназами) або, минаючи цитохроми, безпосередньо на кисень (аеробні дегідрогенази).
105
Флавінові ферменти належать до групи складних ферментів, коферментом у яких є ФАД або ФМН. До складу цих ферментів входить рибофлавін (В2), через що вони дістали назву флавінових ферментів (флавопротеїнів), яких відомо близько 30.
Схематично другий етап тканинного дихання можна зобразити так:
(НАДН + Н+) |
+ ФФ |
|
|
(НАД +) + ФФН2 |
||||||||||||||||
|
|
|||||||||||||||||||
Відновлена |
Окиснена |
|
Окиснена |
|
Відновлена |
|||||||||||||||
форма |
форма |
|
форма |
|
форма |
|||||||||||||||
|
|
R |
|
|
|
|
|
|
|
|
|
|
|
|
R |
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H C |
|
N N C |
|
O + 2H |
H C |
|
|
N NHC |
|
O |
||||||||||
|
|
|
|
|||||||||||||||||
|
|
|
||||||||||||||||||
3 |
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
H3C |
|
|
|
|
|
|
|
|
|
H3C |
|
|
|
|
|
|
|
|||
|
N |
C |
NH - 2H |
|
|
NH C |
NH |
|||||||||||||
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
Окиснена форма ФФ |
|
Відновлена форма ФФ |
||||||||||||||||||
|
|
(жовта) |
|
|
|
|
|
|
|
|
|
|
|
(безбарвна) |
|
|
|
|||
У результаті цієї реакції утворюється відновлена форма ФФ-ФФН2. Безпосереднім акцептором Гідрогену від відновлених форм НАД у флавінових ферментів є метильований ізоалоксазин, тобто складова частина вітаміну В2.
III етап — дія убіхінону (коензиму Q)
Схематично цей етап можна зобразити так:
2Н++ 2e |
|
ФФН2 + КоQ |
КоQН2 + ФФ |
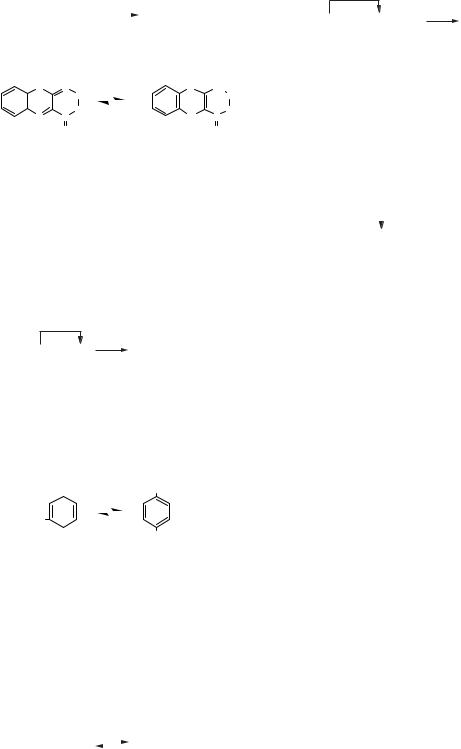
У результаті взаємодії відновленої форми флавінових ферментів з окисненим убіхіноном (коензим Q → КоQ) утворюється відновлена форма убіхінону й окиснена форма флавінових ферментів. Атоми Гідрогену приєднуються до убіхінону по місцю розриву подвійних зв’язків до Оксигену:
|
|
O |
|
|
|
|
|
|
|
|
OH |
||||
R |
|
R1 |
+ 2H |
|
R |
|
|
|
R1 |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
R |
|
R2 |
|
|
|
R |
|
|
|
R2 |
|||||
|
- 2H |
|
|
|
|
||||||||||
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
||
|
|
O |
|
|
|
|
|
|
|
|
|||||
Окиснена форма |
|
|
|
Відновлена форма |
|||||||||||
убіхінону |
|
|
|
|
|
|
|
убіхінону |
|||||||
IV етап — дія системи цитохромів
Цитохроми також належать до групи складних ферментів, небілковою частиною яких є ферумпорфіринові комплекси.
Ферум в цитохромах має властивість змінювати ступінь окиснення, що пов’язано з приєднанням електронів до Феруму або віддачею їх:
Fe3+ |
|
+e |
|
Fe2+ |
|
|
|
||
|
– e |
|
||
|
|
|
|
Fe3+ містить окиснена форма цитохрому, а Fe2+ — відновлена.
Усього відомо близько 20 цитохромів. Їх переважно позначають літерами латинського алфа-
віту b, c1, c, а, a3. Оскільки відбувається транспорт 2 атомів Гідрогену (два протони і два електрони), то у передачі 2 електронів беруть участь по 2 цитохроми.
Отже, убіхінон, окиснюючись, передає свої електрони на 2 цитохроми в, а протони тимчасово залишаються в розчині.
2Н++ 2e |
|
КоQН2 + 2 цит. в Fe3+ |
КоQ + 2 цит. в Fe2+ |
Залізо цитохрому в, приєднавши електрон, перетворюється з окисненої форми на відновлену. Цитохром в передає електрони послідовно на цитохроми с1, с, а і а3.
2 цит. в Fe2+ + 2 цит. с1 Fe3+ → |
2 цит. в Fe3+ + 2 цит. с1 Fe2+ |
||||||
2 |
цит. с1 Fe2+ + 2 цит. с Fe3+ → |
2 цит. с1 Fe3+ + 2 цит. с Fe2+ |
|||||
2 |
цит. с Fe2+ + 2 цит. а Fe3+ → |
2 цит. с Fe3+ |
+ 2 |
цит. а Fe2+ |
|||
2 |
цит. а Fe2+ + 2 цит. а3 Fe3+ → |
2цит. аFe3+ |
+ 2 |
цит. а3 Fe2+ |
|||
|
|
|
|
|
|
|
|
|
|
- 2e |
|
|
|
|
|
|
|
|
|
|
|
||
2 |
цит. а3 Fe++ + 1/2O2 → 2 цит. а3 Fe+++ + O2- |
|
|||||
Цитохромоксидаза називається ще дихальним ферментом Варбурга (або цитохромом а3). При блокуванні цього ферменту (наприклад, цианідами, що зв’язують Fe3+) електрони з цитохромів не будуть переноситися на кисень.
Утворення води відбувається в матриксі мітохондрій з високоактивного кисню:
O2– + 2Н+ → H2O
Всю систему тканинного дихання можна представити у вигляді загальної схеми ферментних комплексів:
І — НАДН-КоQН2-редуктаза (інгібіторами є ротенон, барбітурати);
ІІ— сукцинат-КоQН2-редуктаза (інгібітором
єкарбоксин);
ІІІ — КоQН2-цитохром с-редуктаза (інгібітором є антиміцин А);
ІV — цитохром а-цитохромоксидаза (інгібіторами є оксид карбону, ціаніди).
Поряд із наведеним найбільш поширеним шляхом окиснення субстратів є також довші й коротші шляхи. Приклад довшого шляху — окиснення пірувату і α -кетоглутарату. При окисному декарбоксилюванні цих кислот атоми Гідрогену передаються спочатку на ліпоєву кислоту, а потім — на нікотинамідні ферменти, надалі окиснення нікотинамідних ферментів здійснюється по основному шляху.
Коротшим шляхом окиснюється кислота, атоми Гідрогену якої передаються не на нікотинамідні ферменти, а відразу на флавінові, а потім на убіхінон і цитохроми. Цей шлях окиснення має важливе значення при адаптації організму до несприятливих умов, зокрема до холоду. При короткому шляху окиснення сукцинат окиснюється швидше, тому й швидше вивільняється енергія, необхідна організму. Крім цього, при такому
106

шляху окиснення не утворюється надлишок АТФ, який міг би гальмувати окиснення й ослабляти теплотворення в умовах холоду.
Приклад ще більш короткого шляху окиснення субстратів — окиснення ксантину, гіпоксантину, амінокислот за участю оксидази α -аміно- кислот й інших субстратів. Атоми Гідрогену від цих субстратів передаються на флавінові ферменти (ФФ), а з них — на молекулярний кисень, минаючи цитохроми:
ФФH2 + O2 → ФФ + Н2О2
Оскільки кисень у цьому випадку не активується електронами, то кінцевим продуктом окиснення буде не Н2О, а Н2О2.
Послідовність розташування й дії тих або інших ферментів у процесі тканинного дихання визначається:
1)швидкістю окиснення й відновлення окремих компонентів ланцюга дихальних ферментів;
2)величиною редокс-потенціалу кожного компонента ланцюга дихальних ферментів.
Перенос Гідрогену й електронів завжди йде від каталізатора з меншою величиною редокспотенціалу до каталізатора з більшою величиною редокс-потенціалу, тобто від більш негативного до більш позитивного. Наприклад, редокспотенціал багатьох субстратів становить –0,6 В;
НАДН/НАД+ — –0,32 В, ФФ — 0,06–0,1 В; цито-
хрому а3 — +0,5 В. Процеси тканинного дихання, як видно з наведених даних, перебігають східчасто (поступово), що має досить важливе біологічне значення. Атоми Гідрогену, що відщеплюються від субстратів, мають надлишкову енергію, яку можуть віддати. Цей процес може відбуватись одномоментно, швидко — це спостерігається при горінні органічної сполуки. У результаті поступового окиснення органічних сполук, тобто поступового переносу протонів і електронів по ланцюгу дихальних ферментів, енергія виділяється і використовується поступово.
8.2. ХЕМІОСМОТИЧНА ТЕОРІЯ ОКИСНОГО ФОСФОРИЛУВАННЯ. ІНГІБІТОРИ І РОЗ’ЄДНУВАЧІ ОКИСНОГО ФОСФОРИЛУВАННЯ
Процеси тканинного дихання й окисного фосфорилувания перебігають у мітохондріях (в одній клітині печінки їх налічується більше 1000). Мітохондрія обмежена двома мембранами — зовнішньою й внутрішньою. Зовнішня мембрана гладка, складається приблизно на 50 % із білків і на 50 % — із ліпідів. Через неї проходять усі речовини, що мають молекулярну масу до 10 000 Да. Зовнішня мембрана виконує захисну функцію щодо внутрішньої.
Внутрішня мембрана мітохондрій складається приблизно на 75 % із білків і на 25 % — із ліпідів; 30–40 % усіх білків внутрішньої мембрани — це білки ферментів дихального ланцюга. Вона утворює численні випини (кристи). На по-
верхні крист, зверненій до матриксу, наявні утворення, названі елементарними тільцями (або грибоподібними виростами). У мембрани крист вмонтовані комплекси ферментів, що каталізують перенос протонів і електронів й окисне фосфорилування. Вона непроникна для великих молекул і всіх іонів, пропускає СО2 і NH3. Внутрішній простір мітохондрій заповнений так званим матриксом — драглеподібною напіврідкою масою, що складається на 50 % із білка. У матриксі знаходяться ферменти циклу трикарбонових кислот (ЦТК) — крім сукцинатдегідрогенази (СДГ), окиснення ВЖК й ін.
Окисне фосфорилування
Окисне фосфорилування — це процес синтезу АТФ із АДФ і неорганічного фосфату при переміщенні протонів і електронів по ланцюгу дихальних ферментів до кисню. Відомо, що при окисненні 1 мол. НАДН+Н+ у ланцюзі дихальних ферментів виділяється 220,1 кДж/моль енергії. Із цієї кількості частина енергії акумулюється в 3 мол. АТФ (це 3 · 30,5=91,5 кДж, тобто 41 %). На підставі експериментальних даних виділено 3 пункти в ланцюзі дихальних ферментів, де може синтезуватися АТФ при переміщенні протонів і електронів. Ці пункти називаються пунктами спряження окиснення й фосфорилування. Перша молекула АТФ синтезується при переносі електронів і протонів від відновлених нікотинамідних ферментів на флавінові ферменти.
І |
|
ІІ |
ІІІ |
АДФ + РН АТФ |
АДФ + РН АТФ |
АДФ + РН АТФ |
|
Суб.–Н2 → НФ → |
ФФ → |
УХ → 2 цит. в → |
2 цит. с1 → 2 цит. с → |
→ |
2 цит. а → 2 цит. а3 → |
1/2О2 |
|
Друга молекула АТФ синтезується при переносі електронів від відновленого цитохрому b на цитохром с1. Третя молекула АТФ синтезується при переносі електронів від відновленого цитохрому с на цитохромоксидазу. Оцінити кількісно ступінь спряження окиснення й фосфорилування можна за допомогою коефіцієнта Р:О, який показує, скільки молекул фосфорної кислоти використовується для синтезу АТФ на кожний зв’я- заний з Гідрогеном атом Оксигену. Для більшості субстратів співідношення Р:О=3, тобто на кожний атом іонізованого Оксигену витрачається 3 молекули фосфорної кислоти для синтезу 3 мол. АТФ; для сукцинату Р:О=2. Отже, сумарне рівняння для переносу електронів від НАДН+Н+ до кисню й сполучене з ним окисне фосфорилування має вигляд: Р:О≈ 2,7.
Який же механізм окисного фосфорилування, тобто синтезу АТФ із АДФ і неорганічного фосфату за рахунок енергії електронів, що рухаються по ланцюгу дихальних ферментів? Існує кілька теорій, що пояснюють механізм окисного фосфорилування.
107
|
|
Хеміосмотична теорія П. Мітчела |
переносяться два іони Гідрогену з матриксу на |
|||||||||||||||||||||||||||
|
|
Процеси дихання і фосфорилування перебіга- |
зовнішню поверхню мембрани мітохондрій. |
|||||||||||||||||||||||||||
ють у внутрішній мембрані мітохондрій. Спря- |
|
Переміщення електронів по ланцюгу дихаль- |
||||||||||||||||||||||||||||
них ферментів і протонів із внутрішньої поверхні |
||||||||||||||||||||||||||||||
женість дихання і окисного фосфорилування зу- |
мембрани мітохондрій на зовнішню приводить до |
|||||||||||||||||||||||||||||
мовлена системою трансмембранного переміщен- |
нагромадження протонів на зовнішній поверхні |
|||||||||||||||||||||||||||||
ня електронів і протонів (іонів Гідрогену). Саме |
мембрани й зменшення їхньої концентрації у мат- |
|||||||||||||||||||||||||||||
нерозривний взаємозв’язок переміщення елект- |
риксі. Мітохондріальна мембрана непроникна |
|||||||||||||||||||||||||||||
ронів по ланцюгу дихальних ферментів і протонів |
для іонів Н+ і ОН-. Це обумовлює виникнення по- |
|||||||||||||||||||||||||||||
через мембрану мітохондрій на кисень являє со- |
зитивного заряду на зовнішній поверхні мембра- |
|||||||||||||||||||||||||||||
бою центральну ланку дихання і сполученого з |
ни й негативного — на її внутрішній поверхні. |
|||||||||||||||||||||||||||||
ним фосфорилування. У цьому процесі провідну |
Так виникає електрохімічний потенціал, що |
|||||||||||||||||||||||||||||
роль відіграє енергія збуджених електронів, зав- |
складається з двох компонентів: різниці в концен- |
|||||||||||||||||||||||||||||
дяки якій відбувається переміщення (перекачу- |
трації іонів Гідрогену (тобто хімічного потенціа- |
|||||||||||||||||||||||||||||
вання) іонів Гідрогену з матриксу на зовнішню |
лу) й різниці електричного заряду (тобто елект- |
|||||||||||||||||||||||||||||
поверхню внутрішньої мембрани мітохондрій. |
ричного потенціалу). |
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
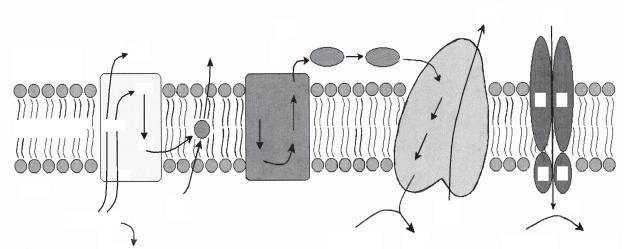
Як показано на рис. 8.1, на внутрішній по- |
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
верхні мембрани мітохондрій атоми Гідрогену від- |
|
Енергія електрохімічного потенціалу і викори- |
||||||||||||||||||||||||||||
стовується для біосинтезу АТФ. При цьому про- |
||||||||||||||||||||||||||||||
щеплюються від НАДН+Н+ і переносяться за до- |
||||||||||||||||||||||||||||||
помогою ФМН і SH-груп на зовнішню поверх- |
тони проходять через протонний канал (Fo — |
|||||||||||||||||||||||||||||
ню мембрани мітохондрій, де відбувається поділ |
фактор о) мембрани мітохондрій до білкового ком- |
|||||||||||||||||||||||||||||
атома Гідрогену: протон виділяється в зовнішній |
плексу F1 |
(фактор 1), що приводить до зменшен- |
||||||||||||||||||||||||||||
розчин, а електрони за допомогою FeS-білка за- |
ня величини електрохімічного потенціалу й |
|||||||||||||||||||||||||||||
ліза переносяться на КоQ, тобто убіхінон, до |
трансформації його енергії для утворення АТФ із |
|||||||||||||||||||||||||||||
внутрішньої поверхні мембрани. Каталізує цей |
АДФ і ФН (Н3РО4). |
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
процес фермент НАДН-дегідрогеназа, що містить |
|
F1 |
— грибоподібний випин на кристах міто- |
|||||||||||||||||||||||||||
як простетичну групу ФМН, а також має у своїй |
хондрій. Білковий комплекс Fо і F1 |
називається |
||||||||||||||||||||||||||||
структурі SH-групу й FeS-білок. |
|
|
|
|
|
|
|
|
протонною системою АТФ-синтетази, або про- |
|||||||||||||||||||||
|
|
При приєднанні електронів до КоQ він отри- |
тонною АТФазою, або Н+АТФазою. |
|
||||||||||||||||||||||||||
мує негативний заряд і захоплює протон із мат- |
|
Н+АТФаза складається з двох головних ком- |
||||||||||||||||||||||||||||
риксу мітохондрій, перетворюючись на відновле- |
понентів: |
Fо і F |
1 |
(від англ. |
factor). |
|
F нагадує |
|||||||||||||||||||||||
ну форму КоQН2. Остання дифундує крізь мемб- |
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|||||||||||||||||
формою круглу дверну ручку, звернену у бік мат- |
||||||||||||||||||||||||||||||
рану до зовнішньої поверхні, де розташований |
риксу мітохондрій, або шапку гриба (тому ці ут- |
|||||||||||||||||||||||||||||
цитохром b; КоQН2 окиснюється біля зовнішньої |
ворення називають ще грибоподібними вироста- |
|||||||||||||||||||||||||||||
сторони мембрани, віддаючи електрони цитохро- |
ми). «Шапка» за допомогою ніжки прикріп- |
|||||||||||||||||||||||||||||
му b, а протони — на зовнішню поверхню внут- |
люється до компонента Fo, що вбудований у |
|||||||||||||||||||||||||||||
рішньої мембрани мітохондрій. |
|
|
|
|
|
|
|
|
внутрішню мембрану й пронизує її наскрізь (ця |
|||||||||||||||||||||
|
|
Причому при переносі електронів від цитохро- |
частина молекули АТФ-синтетази зв’язує оліго- |
|||||||||||||||||||||||||||
му c1 на c з матриксу мітохондрій протони знову |
міцин — потужний інгібітор цього ферменту). Fо- |
|||||||||||||||||||||||||||||
переміщуються на зовнішню поверхню мембрани |
F1-АТФаза в ізольованому вигляді каталізує |
|||||||||||||||||||||||||||||
мітохондрій за допомогою КоQ. Отже, при окис- |
розщеплення АТФ на АДФ і Н3РО4. Однак у |
|||||||||||||||||||||||||||||
ненні НАДН+Н+ пара електронів перетинає |
мітохондріях головна її біологічна функція поля- |
|||||||||||||||||||||||||||||
внутрішню мембрану мітохондрій тричі, щоразу |
гає не в розщепленні, а в синтезі АТФ із АДФ і |
|||||||||||||||||||||||||||||
|
|
КОМПЛЕКС I |
|
|
|
КОМПЛЕКС III |
|
|
|
2H+ |
КОМПЛЕКС IV |
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2H+ |
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
цит. с |
цит. с |
|
|
|
|
|
|
|
|
|
|
|
||||
|
Міжмембранний |
2H+ |
|
2H+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
простір |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
цит. a |
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
FeS |
|
|
|
|
|
цит. с1 |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
F0 |
|
|
F0 |
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
цит. |
вk |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Міжмітохондрі |
- |
|
FMN |
Q |
|
|
|
|
|
|
|
|
|
|
|
цит. a3 |
|
|
|
|
|
|
|
|
|
|||
|
альна мембрана |
|
|
|
|
|
|
|
|
|
Cytb |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
FeS |
|
|
|
|
|
|
|
|
FeS |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
цит. вт |
|
|
|
|
|
2e |
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
Maтрикс |
2e |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
F1 |
|
F1 |
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
2H+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
2H+ |
|
|
|
|
|
2H |
+ |
||||||
|
|
НАДH + H+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1/2O2 + 2H+ |
H2O |
AДФ + Pi |
|
ATФ + H2O |
||||||||||||
НАД+ Рис. 8.1. Діаграма мітохондріального ланцюга дихання (перенос електронів і протонні насоси)
108