Материал: Біологічна та біоорганічна хімія_Мардашко О.О._ изд. 2008-342 с._ОНМедУ-2012

Глава 6. ФЕРМЕНТИ ТА КОФЕРМЕНТИ, КОФЕРМЕНТНІ
ФУНКЦІЇ ВІТАМІНІВ. РЕГУЛЯЦІЯ МЕТАБОЛІЗМУ
6.1. ФЕРМЕНТИ. СТРУКТУРА, ФІЗИКО-ХІМІЧНІ ВЛАСТИВОСТІ БІЛКІВ-ФЕРМЕНТІВ, КЛАСИФІКАЦІЯ ЗА ТИПОМ РЕАКЦІЇ
Здавна спостерігали, що перетворення виноградного соку на вино супроводжується виділенням пухирців газу, яке за зовнішніми ознаками нагадує кипіння, тому весь цей процес, тобто бродіння, назвали ферментацією (від лaт. fermentation — кипіння, бродіння), а речовини, що прискорюють бродіння, — ферментами. Через те, що бродіння прискорювали дріжджі, багато ферментів було знайдено спочатку у дріжджах і ферменти дістали другу назву — ензими (від грецьк. en zyme — у дpіжджax).
Перші наукові уявлення про ферменти були висловлені у 1814 р. K. C. Kіpхгoфoм, який довів, що саме екстракти з паростків зерна, багаті на білки, здатні розщеплювати крохмаль до мальтози. Знaчeння цих дослідів ученого полягало в тoму, що впepшe була пoкaзaна рoль самe білків у пеpeтвоpeнні вyглeвoдів. О. Я. Дaнилeвcький розробив мeтoди виділeння фepмeнтів (їx екcтpaкцію, aдcopбцію, елюцію) і за їх допомогою у 1862 р. виділив із підшлункової залози ферменти aмілaзy і тpипcин, дослідивши їх властивості. Лyї Пacтep у дослідах із зеленою пліснявою довів, щo ферменти цієї плісняви зброджують тільки D-виннy киcлoтy і нe зброджують її L-фopмy. Цими дослідами булa доведена cпeцифічніcть дії фepмeнтів. У подальшому значний внесок у pозвиток фepмeнтoлoгії зробили О. М. Бax, І. П. Пaвлoв, B. І. Пaллaдін та ін. Зараз відомо близько 3000 ферментів, триває їх подальший пошук і дослідження, оскільки хімічні процеси, які відбуваються в біологічних системах, є ферментативними.
Існують такі дoкaзи, що всі фepмeнти є білками:
1.Пoдібнo до білків, фepмeнти мають виcoкy мoлeкyляpнy мacy — від дecятків тиcяч дo кількоx мільйoнів дaльтoн (Да). Haпpиклад, мoлeкyляpнa мaca піpyвaтдeгідpoгeнaзи дорівнює 4 000 000 Да, лактатдегідрогенази — 140 000 Да, кaталaзи —
24 800 Да.
2.Як і білки, фepмeнти утворюють кoлoїдні розчини. Мoлeкyли фepмeнтів нe здатні до діaлізy, тoмy за допомогою діaлізу їx розчини можна звільнити від низькомолекулярних домішок.
3.Під впливом різних фізичних і хімічних факторів (виcoкa тeмпepaтypa, міцні киcлoти, луги, coлі важких мeтaлів та ін.) відбувається дeнaтypaція фepмeнтів. Фермент при цьому втрачає здатність каталізувати хімічну реакцію.
4.Ферменти, як і білки, можна висолювати нeйтpaльними coлями (cyльфaтoм aмoнію, xлopидoм нaтpію). Саме завдяки висолюванню виділено багато ферментів у формі кристалів.
5.Пpи гідpoлізі фeрмeнти, як і білки, pозпaдaютьcя нa aмінoкиcлоти.
6.Дoкaзoм білкoвoї пpиpoди фepмeнтів є їx лaбopaтopний cинтeз із aмінoкиcлoт.
Ферменти — це специфічні білки, що виконують в організмі роль біологічних каталізаторів. Як усі білки, ферменти мають первинну, вторинну, третинну, а багато які з них — четвертинну структуру. Ферменти з четвертинною структурою складаються з протомерів (субодиниць).
Номенклатура ферментів
Наявність великої кількості ферментів (сьогодні їх відомо близько 3000) викликала необхідність розробити єдину класифікацію й номенклатуру ферментів. У 1961 р. у Москві на V Міжнародному біохімічному конгресі була затверджена єдина міжнародна (систематична) класифікація й номенклатура ферментів. В основу її покладено принцип поділу ферментів за типом хімічних реакцій, які вони каталізують. Тип реакції, що каталізують ферменти, у сполученні з назвою субстрату (субстратів) — основа для систематичного найменування ферментів.
Усі відомі реакції, що перебігають в організмі, можуть бути зведені до шести основних типів:
1.Окисно-відновні реакції.
2.Реакції переносу окремих груп атомів від одних субстратів на інші.
3.Реакції розщеплення внутрішньомолекулярних зв’язків органічних речовин за участю молекули води.
4.Оборотні реакції відщеплення різних груп атомів від субстратів негідролітичним шляхом з утворенням подвійного зв’язку або приєднання груп атомів до місця подвійного зв’язку.
5.Реакції ізомеризації.
6.Реакції синтезу органічних речовин з інших вихідних молекул із використанням розпаду АТФ або іншого нуклеозидтрифосфату.
Відповідно до шести типів хімічних реакцій всі ферменти поділені на шість класів:
1.Оксидоредуктази.
2.Трансферази.
3.Гідролази.
4.Ліази.
5.Ізомерази.
6.Лігази (синтетази).
Класи ферментів, у свою чергу, поділяються на підкласи, підкласи — на підпідкласи. Поділ ферментів на підкласи в межах одного класу зроблено з урахуванням основних видів субстратів, які беруть участь у даному типі хімічних перетворень. Наприклад, окремі підкласи оксидоредуктаз формують ферменти, що окиснюють
субстрати, які містять спиртові групи (–СН2–ОН) до альдегідних і кетонних груп (перший підклас),
іферменти, що окиснюють альдегіди і кетони до кислот (другий підклас оксидоредуктаз). Поділ
84
трансфераз на підкласи зроблено з урахуванням |
ферментів, у якій назви ферментів скорочені. На- |
|||
тієї групи, що підлягає переносу, гідролаз — з |
приклад, цей же фермент має тривіальну назву |
|||
урахуванням типу зв’язку, що гідролізується, і |
лактатдегідрогеназа. |
|
||
т. ін. |
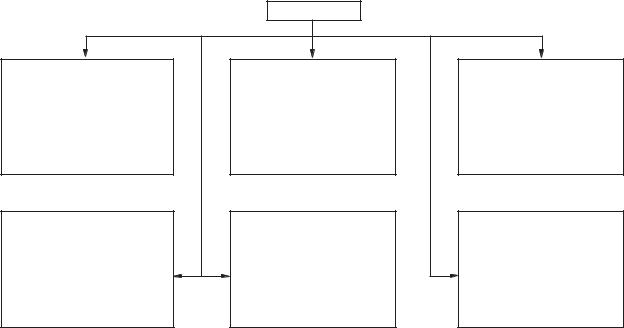
Класифікація ферментів наведена на рис. 6.1. |
|||
Поділ підкласів ферментів на підпідкласи |
Номенклатура — цифрове відображення місця |
|||
відбувається з урахуванням природи хімічних |
кожного ферменту в класифікації. |
|||
сполук донорів або акцепторів, які беруть участь |
Код ферменту складається з чотирьох цифр: |
|||
у реакції. Наприклад, у гідролаз підпідклас уточ- |
1-й знак |
— клас ферменту (від 1 до 6); |
||
нює тип зв’язку, що гідролізується, а у ліаз — |
2-й знак |
— функціональна група; |
||
тип групи, що відщеплюється. Нарешті, всі фер- |
3-й знак |
— кофермент; |
||
менти, об’єднані в один підпідклас, отримують |
4-й знак |
— субстрат. |
||
порядковий номер. |
1. Оксидоредуктази. Оксидоредуктази каталі- |
|||
Кожний фермент має код, або шифр, що |
||||
зують окисно-відновні реакції. Відповідно до сис- |
||||
містить чотири цифри, розділені крапками. Ці |
тематичної номенклатури назви їх складаються |
|||
шифри утворюються за таким принципом. Пер- |
за формою «донор:акцептор-оксидоредуктаза». |
|||
ша цифра вказує на номер одного з шести класів |
Відповідно до робочої номенклатури розрізняють |
|||
ферментів, друга означає підклас, третя — |
такі основні оксидоредуктази: |
|||
підпідклас і четверта — порядковий номер фер- |
1) Анаеробні дегідрогенази — каталізують |
|||
менту у підпідкласі. На початку шифру ставить- |
||||
перенос атомів Гідрогену або електронів на будь- |
||||
ся дві літери — КФ (класифікація ферментів). На- |
який проміжний субстрат, але не на кисень і не |
|||
приклад, повний шифр ферменту лактатдегідро- |
на перекис водню (наприклад, лактатдегідроге- |
|||
генази — КФ 1.1.1.27. Цей фермент належить до |
наза — лактат:НАД+-оксидоредуктаза). |
|||
класу оксидоредуктаз, до першого підкласу — |
2) Аеробні дегідрогенази (або оксидази) — |
|||
оксидоредуктаз, які окиснюють оксигрупи до ке- |
||||
каталізують перенос атомів Гідрогену або елек- |
||||
тонних груп, до першого підпідкласу, у якому |
тронів безпосередньо на кисень (наприклад, ци- |
|||
акцептором водню є НАД+, порядковий номер |
тохромоксидаза каталізує перенос електронів від |
|||
цього ферменту в підпідкласі — 27. |
цитохрому а3 на кисень). |
|
||
Крім шифру ферменти мають певну назву за |
|
|||
3) Каталаза і пероксидаза. Каталаза каталі- |
||||
систематичною і робочою (тривіальною) номен- |
||||
зує перенос двох атомів Гідрогену з однієї молеку- |
||||
клатурою. За систематичною номенклатурою |
ли пероксиду гідрогену на іншу: |
|||
назва ферментів складається з двох частин. Пер- |
Н2О2 + Н2О2 → |
2Н2О + О2 |
||
ша частина вказує на назву субстрату, на який |
||||
діє фермент, друга — на природу хімічної реакції |
Пероксидаза каталізує перенос двох атомів |
|||
й має закінчення -аза. Наприклад, лактат: |
||||
Гідрогену з різних субстратів, включаючи від– |
||||
НАД+-оксидоредуктаза. Цей фермент каталізує |
новлені піридинові й флавінові ферменти, на пер- |
|||
перенос протонів і електронів від лактату на |
оксид гідрогену: |
|
||
НАД. У повсякденній практиці використовують |
Н2О2 + 2Н+ → |
2Н2О |
||
так звану робочу (тривіальну) номенклатуру |
||||
ФЕРМЕНТИ
1-й клас — Оксидоредуктази
13 підкласів Окисно-відновні реакції
—НАДзалежні
—ФАДзалежні
—цитохроми
4-й клас — Ліази
5 підкласів Негідролітичне розщеплення ковалентних зв’язків
—Декарбоксилази
—Дегідратази
2-й клас — Трансферази
8 підкласів Перенос груп атомів:
—метильні
—ацильні
—амінні
—фосфатні
5-й клас — Ізомерази
5 підкласів Реакції ізомеризації Цис-транс-ізомерази Внутрішньомолекулярні оксидоредуктази Внутрішньомолекулярні трансферази
3-й клас — Гідролази
9 підкласів Гідролітичне розщеплення зв’язків складних ефірів:
—фосфатази
—глікогідролази
—пептидгідролази
6-й клас — Лігази
4 підкласи Синтез із використанням енергії макроергів
С–О-зв’язки С–S-зв’язки С–N-зв’язки С–С-зв’язки
Рис. 6.1. Класифікація ферментів
85
2. Трансферази. До класу трансфераз належать ферменти, що каталізують перенос різних груп атомів від одних субстратів на інші.
Найменування їх складається за формою: «донор + акцептор — група, що транспортується
— трансфераза». Розрізняють трансферази, що каталізують перенос:
а) одновуглецевих залишків (наприклад, метилтрансферази каталізують перенос метильних груп (–СНЗ), формілтрансферази — перенос формільних груп);
б) залишків фосфорної кислоти — фосфотрансферази (наприклад, гексокіназа: АТФ + гексоза →
→гексозо-6-фосфат + АДФ);
в) аміногруп — амінотрансферази. З них найбільш досліджені дві: аланінамінотрансфераза (АЛТ) і аспартатамінотрансфераза (АСТ).
АЛТ каталізує реакцію оборотного переносу аміногрупи між α -аланіном і α -кетоглутаровою кислотою з утворенням пірувату і α -глутаміно- вої кислоти:
L-Аланін + α -Кетоглутарат →
→Піруват + L-Глутамат.
АСТ каталізує реакцію оборотного переносу аміногрупи між аспарагіновою кислотою й α -ке- тоглутаровою кислотою з утворенням оксалоацетату і L-глутамінової кислот:
Аспартат + α -Кетоглутарат →
→Оксалоацетат + L-Глутамат;
г) трансферази, що каталізують перенос залишків різних кислот (ацилів), — ацилтрансферази (наприклад, перенос ацилів із коензиму А на гліцеролфосфорну кислоту в процесі біосинтезу тригліцеридів). Розрізняють також глікозилтрансферази, що каталізують перенос залишків вуглеводів, й інші трансферази.
3. Гідролази. До класу гідролаз належать ферменти, що каталізують розщеплення внутрішньомолекулярних зв’язків органічних речовин за участю молекули води:
R–X + Н2О → R–ОН + НХ.
Найменування їх складається за формулою: «субстратгідролаза» (наприклад, ацетил-КоА- гідролаза — фермент, що розщеплює за участю молекули води ацетил-КоА на коензим А й оцтову кислоту). До гідролаз належать ферменти, що гідролізують складні ефірні, глікозидні, пептидні зв’язки та ін. Ферменти, що каталізують гідроліз складних ефірів карбонових кислот, мають робочу назву естерази (від лат. ester — ефір). Наприклад, фермент ліпаза каталізує гідроліз зв’язків гліцеридів, розщеплюючи їх на гліцерол і карбонові кислоти; ацетилхолінестераза каталізує гідроліз ацетилхоліну на холін і оцтову кислоту. Ферменти, що каталізують гідроліз фосфомоноефірів, за робочою номенклатурою називаються фосфатазами (наприклад, глюкозо-6- фосфатаза каталізує гідроліз глюкозо-6-фосфату на глюкозу і фосфорну кислоту). Ферменти, що каталізують гідроліз глікозидних зв’язків, розщеплюють вуглеводи (амілаза, мальтаза, лакта-
за, сахароза та ін.). Ферменти, що каталізують гідроліз пептидних зв’язків, називаються пептидгідролази (пепсин, трипсин, хімотрипсин).
4.Ліази. До класу ліаз належать ферменти, що каталізують відщеплення від субстратів негідролітичним шляхом різних груп з утворенням подвійного зв’язку або приєднання різних груп до місця подвійного зв’язку. Систематична назва цих ферментів утворюється аналогічно гідролазам, тобто «субстрат-відщеплена група-ліаза» (наприклад, малатгідроліаза каталізує оборотне відщеплення молекули води від яблучної кислоти з утворенням фумарової кислоти). Залежно від характеру зв’язків, які руйнують ліази, вони поділяються на Карбон-Карбон-ліази (С-С-ліа- зи), Карбон-Оксиген-ліази (С-О-ліази), Карбон- Нітроген-ліази (C-N-ліази) та ін. До Карбон- Карбон-ліаз належать декарбоксилази (піруватдекарбоксилаза). Карбон-Оксиген-ліази за робочою номенклатурою називаються дегідратазами (гідратазами). Це, наприклад, карбоангідраза,
що розщеплює вугільну кислоту на СО2 і Н2О. Прикладом ферменту, що діє на Карбон-Нітро- ген-зв’язок, може бути фермент аргінінсукцинатліаза, що каталізує розщеплення аргінінбурштинової кислоти на аргінін і фумарову кислоту.
5.Ізомерази. До класу ізомераз належать ферменти, що каталізують різні типи реакцій ізомеризації з утворенням різних ізомерів, тобто речовин однакового хімічного складу і молекулярної маси, але різних за будовою молекули і властивостями. Ізомерази, що діють на субстрати з одним асиметричним атомом Карбону, називаються рацемазами. Якщо ізомерази діють на субстрати з кількома асиметричними атомами Карбону, то вони називаються епімеразами. Наприклад, УДФ-глюкозо-епімераза перетворює УДФ-глю- козу на УДФ-галактозу. До ізомераз належать також цис-транс-ізомерази. Якщо ізомеризація включає внутрішньомолекулярний перенос груп, фермент дістає назву мутаза. Наприклад, фосфоглюкомутаза каталізує взаємоперетворення глюкозо-1-фосфату на глюкозо-6-фосфат.
6.Лігази (синтетази). До класу лігаз належать ферменти, що каталізують синтез органічних речовин із двох вихідних молекул з використанням енергії АТФ або інших нуклеозидтрифосфатів. Систематична назва лігаз складається за формою «X-Y-лігаза», де через X-Y позначаються вихідні речовини (наприклад, глутаматаміаклігаза). За участю цього ферменту з глутамінової кислоти й аміаку в присутності АТФ синтезується глутамін — одна з транспортних форм аміаку.
Залежно від характеру зв’язків, що утворюються, лігази поділяються на такі, що утворюють С-С-зв’язки, С-О-зв’язки, С-N-зв’язки та ін. До лігаз, що утворюють С-С-зв’язки, належить, наприклад, ацетил-КоА-карбоксилаза, що катал-
ізує біосинтез малоніл-КоА з ацетил-КоА і СО2; піруваткарбоксилаза, що каталізує біосинтез щавлевооцтової кислоти з піровиноградної кис-
лоти і СО2. До лігаз, що утворюють С-О-зв’язки, належить, наприклад, фермент аміноацилсинтетаза, що каталізує утворення аміноацил-тРНК
86
у процесі біосинтезу білків. До лігаз, що утворюють С-N-зв’язки, належать пептидсинтетази, що каталізують утворення пептидних зв’язків.
Специфічність дії ферментів
Специфічність дії ферментів — це спрямованість дії ферменту на певний субстрат або групу близьких за структурою й властивостями субстратів. Специфічність зумовлена конформаційною й електростатичною комплементарністю між молекулами субстрату та ферменту й унікальною структурою активного центру ферменту, чим забезпечується висока спорідненість і вибірковість перебігу однієї реакції серед багатьох інших. Розрізняють такі види специфічності:
1. Абсолютна специфічність — фермент ката-
лізує перетворення тільки одного субстрату (наприклад, аргіназа розщеплює аргінін на орнітин і сечовину; уреаза каталізує розпад тільки сечовини, а на тіосечовину не впливає).
|
NH2 |
|
NH2 |
||||
C |
|
O |
C |
|
S |
||
|
|
||||||
|
|
||||||
|
|
|
|
|
|
|
|
NH2 |
NH2 |
||||||
Сечовина |
Тіосечовина |
||||||
2.Групова специфічність — фермент каталі-
зує перетворення групи субстратів, що мають один тип будови і спільний тип зв’язку в будові
субстратів, а також будову ділянки молекули субстратів, яка цей зв’язок оточує. Так, α -аміла-
за розщеплює крохмаль і глікоген. Обидва субстрати мають один тип зв’язку — α -1-4-глікозид- ний зв’язок, утворений залишками глюкози.
3.Відносна специфічність дії ферменту — це здатність діяти на субстрати, що мають один певний тип хімічного зв’язку. Травні ферменти — пепсин, трипсин — специфічні щодо пептидних зв’язків, утворених певними амінокислотами в різних білках.
Ліпаза гідролізує складноефірні зв’язки в триацилгліцеролах, побудованих із залишків гліцеролу й різних вищих кислот. Цитохром Р-450 бере участь у гідроксилюванні різних сполук (близько 7000 найменувань). Це найменш специфічна ферментна система, що бере участь у перетворенні природних речовин, ліків, отрут.
4.Стереохімічна специфічність — фермент ка-
талізує перетворення тільки одного з можливих стереоізомерів субстрату ( D- або L-форму, цисабо транс-ізомерів).
Відомі оксидази D- і L-амінокислот. Оксидаза D-амінокислот високоактивна при фізіологічних значеннях рН середовища, порівняно з оксидазою L-амінокислот (оптимум рН=10). Фумараза каталізує перетворення тільки фумарату (транс-ізомер) і не діє на малеїнат (цис-ізомер):
COOH |
COOH |
||||
|
|
|
|
|
|
CH |
CH |
||||
|
|
|
|
|
|
HCH |
CH |
||||
|
|
COOH |
|
|
COOH |
Фумарат |
Малеїнат |
||||
Таким чином, завдяки специфічності дії ферментів забезпечується перебіг із високою швидкістю певних реакцій з величезного різноманіття можливих перетворень, чим регулюється інтенсивність обміну речовин.
6.2. КОФАКТОРИ ТА КОФЕРМЕНТИ. КОФЕРМЕНТНІ ФУНКЦІЇ ВІТАМІНІВ
За хімічним складом ферменти поділяються на дві групи: прості й складні ферменти. Прості фер- менти-протеїни представлені поліпептидними ланцюгами й при гідролізі розпадаються на амінокислоти. До таких ферментів належать: пепсин, хімотрипсин, α -амілаза, ліпаза.
Більшість природних ферментів — це складні ферменти, які складаються з білкової частини (апофермент) і небілкової (кофактора). Складний фермент, що складається з апоферменту й кофактора, називається холоферментом:
Холофермент = Апофермент + Кофактор (кофермент, простетична група)
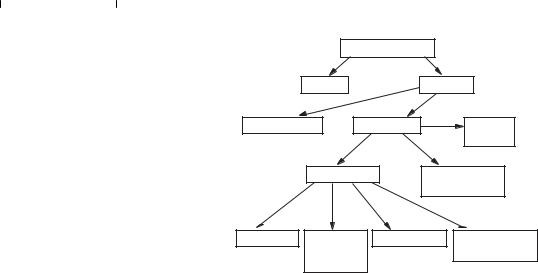
ФЕРМЕНТИ
Прості Складні
Апофермент |
Кофактор |
Іони |
|
|
металів |
Кофермент |
Простетична |
|
|
|
група |
Вітаміни Фосфорні Нуклеотиди Металовмісні ефіри комплекси вітамінів
Зв’язок між білковою й небілковою частиною в складних ферментах може бути різної міцності. У тих випадках, коли небілкова частина ферменту міцно зв’язана з апоферментом ковалентним зв’язком, вона називається простетичною групою (наприклад, у молекулі аце- тил-КоА-карбоксилази біотин ковалентно зв’язаний з апоферментом за допомогою амідного зв’язку).
Якщо небілкова частина ферменту слабо зв’я- зана з ферментним білком (наприклад, водневими або іншими зв’язками) і з’єднується з ним тільки під час каталітичної реакції, то вона називається коферментом. Типові представники коферментів: НАД+ і НАДФ+.
Однак різницю між простетичною групою й коферментом не можна абсолютизувати, оскільки в одних випадках, наприклад, в оксидазі D- амінокислот ФМН може бути легко відділений від білкової частини шляхом діалізу; той же ФМН міцно зв’язаний ковалентно з ферментами
87
тканинного дихання, виконуючи функції простетичної групи. Яка роль апоферменту й коферменту (простетичної групи) у каталізі? Один кофермент може з’єднуватися з різними апоферментами з утворенням різних ферментів, які каталізують різні біохімічні реакції. Наприклад, ПАЛФ є коферментом амінотрансфераз і декарбоксилаз амінокислот, НАД+ і НАДФ+ входять до складу більш як 150 різних ферментів. Саме апофермент визначає специфічність дії складного ферменту. Однак без коферменту складний фермент функціонувати не може, тому що кофермент, як правило, безпосередньо взаємодіє з субстратом. Отже, до коферментів належать органічні речовини порівняно складної будови, що беруть безпосередню участь у ферментативних реакціях.
Важливу роль у ферментативних реакціях виконують так звані кофактори. Це, як правило, речовини менш складної будови, зокрема, іони металів й інші неорганічні сполуки. Кофактори найчастіше не контактують із субстратом і не беруть участь у реакції, а переводять фермент в активну форму, сприяючи каталітичній реакції. Наприклад, іони Mg2+ активують фермент аденозинтрифосфатазу, іони Zn2+ — деякі пептидази. Однак цей поділ умовний, тому що іони можуть входити до складу ферментів і брати участь у каталітичній реакції як частина молекули ферменту.
Іони металів як кофактори ферментів
Металоферменти — дуже поширена група ферментів (чверть від усіх ферментів) (табл. 6.1). Іони металів як кофактори входять до складу ферментів, що належать до різних класів. Металоферменти, що каталізують реакції окисненнявідновлення, досить численні. Іон металу може перебувати в активному центрі або входити до складу органічної молекули (наприклад гему),
|
|
Таблиця 6.1 |
|
Деякі металозалежні ферменти |
|||
|
|
|
|
Фермент |
Іон металу |
Механізм участі |
|
у каталізі |
|||
|
|
||
|
|
|
|
Гексокіназа |
Mg2+ |
Зв’язування |
|
|
|
субстрату |
|
Піруваткіназа |
Mg2+, K+ |
Зв’язування |
|
|
|
субстрату |
|
Аргіназа |
4 Mn2+ |
Зв’язування |
|
|
|
субстрату |
|
|
|
й каталіз |
|
Піруват- |
4 Mn2+ |
Каталіз |
|
карбоксилаза |
|
|
|
Транскетолаза |
Ca2+ |
Стабілізація |
|
|
|
четвертинної |
|
|
|
структури |
|
Супероксид- |
2 Zn2+, 2 Cu2+ |
Каталіз |
|
дисмутаза |
|
|
|
γ -Амілаза |
Ca2+ та аніон Cl |
Стабілізація |
|
|
|
третинної |
|
|
|
структури |
|
|
|
|
|
або може бути зв’язаний залишками амінокислот апоферменту. Оскільки під дією оксидоредуктаз відбувається перенос електронів і змінюється ступінь окиснення субстратів, то в ролі кофакторів виступають іони металів зі змінним ступенем окиснення: Ферум, Купрум, Молібден, Кобальт. Металоферменти, що каталізують реакції гідролізу субстратів, містять метали з постійним ступенем окиснення: Цинк, Кальцій, Магній.
Роль металів у каталітичній дії ферменту
Метал, будучи електрофільною групою активного центру, здатний взаємодіяти з негативно зарядженими групами субстрату. Такий металосубстратний комплекс легше атакується ферментом. Наприклад, іони Mg2+ або Mn2+ утворюють комплекс із АТФ або АДФ у реакціях, що каталізуються кіназами й АТФазою. У разі відсутності металів ферменти малоактивні або не активні.
Метал зі змінною валентністю сам може брати участь у транспорті електронів (іони Fe3+→ Fe2+ у цитохромах в, с1, с, а, а3).
Метал сприяє формуванню каталітично активної конформації третинної й четвертинної структури апоферменту. Стабілізація можлива шляхом утворення сольових містків між іоном металу й карбоксильними групами амінокислот. Наприклад, позбавлена Цинку алкогольдегідрогеназа дисоціює на субодиниці й втрачає активність. Іони металів служать своєрідним містком між апоферментом і коферментом. Нормальна функція великого сімейства металоферментів залежить від нормального надходження в організм металів, що здебільшого належать до групи мікроелементів, звідси й висока біологічна роль цих металів: недостатнє надходження їх з їжею може спричинити серйозні порушення обміну речовин в організмі.
Коферменти, їх хімічна будова й функції
Коферментами можуть бути різноманітні за хімічною структурою органічні речовини. Вони поділяються на такі групи:
1.Коферменти — вітаміни.
2.Коферменти — фосфорні ефіри вітамінів.
3.Коферменти — нуклеотиди.
4.Коферменти — металовмісні комплекси.
1) До коферментів-вітамінів належать, на-
приклад, такі вітаміни, як ліпоєва кислота, фолієва кислота, біотин та ін. Ліпоєва кислота є одним із коферментів піруватдегідрогеназного комплексу, альфа-кетоглутаратдегідрогеназного комплексу, що каталізують окисне декарбоксилювання відповідно пірувату й альфа-кетоглу- тарату до ацетил-КоА і сукциніл-КоА. Біотин входить до складу ферментів, що каталізують реакції карбоксилювання. Наприклад, при біосинтезі вищих жирних кислот біотин необхідний для перетворення ацетил-КоА на малоніл-КоА (аце- тил-КоА-карбоксилаза). Біотин є коферментом
88