Материал: Біологічна та біоорганічна хімія_Мардашко О.О._ изд. 2008-342 с._ОНМедУ-2012

замін зв’язується з аспарагіном за рахунок гідроксильної групи Гідрогену й водню аміногрупи амінокислоти.
Друга структурна відмінність гліколіпідів від глікопротеїнів — кожна молекула гліколіпіду має лише один вуглеводний ланцюг, тоді як у глікопротеїнів таких ланцюгів може бути кілька. Ці ланцюги бувають різної довжини, однак є одне важливе обмеження: кожна молекула глікопротеїну завжди містить ланцюги тільки одного типу, тобто з однаковою моносахаридною послідовністю.
Вуглеводи зв’язуються із зовнішніми ділянками молекул мембранних білків і ліпідів, утворю-
ючи глікопротеїни і гліколіпіди. Вуглеводний шар, що утворюється на зовнішній поверхні мембрани, дістав назву глікокалікс. Він заряджений негативно, виконує кілька важливих функцій: зв’язує позаклітинний кальцій, стабілізує мембранні структури, служить матриксом для прикріплення інших клітин.
Гліколіпіди мембран є, головним чином, похідними сфінгозину (глікоцераміди, гангліозиди).
Глікопротеїни мембран утворюються за рахунок ковалентних зв’язків із білками мембран: гідроксильних груп серину та треоніну (О-гліко- зидні зв’язки) і амідної групи аспарагіну (N- глікозидні зв’язки).
Олігосахаридні залишки гліколіпідів і глікопротеїнів виконують функції лігандів для зовнішніх білків, тобто забезпечують процес розпізнавання і міжклітинної взаємодії, а також особливо важливі в реакціях клітинного імунітету.
Аномальні зміни структури поверхневих гангліозидів у мембранах пухлинних клітин призводять до втрати характерного для росту нормальних клітинних пластів феномена «контактного інгібування», що спричинює неконтрольований ріст.
Моделі мембран
Ліпіди здатні взаємодіяти з білками своїми полярними групами — у цьому випадку їхні молекули зв’язуються між собою силами електростатичного притягання зарядів. Було встановлено, що коли ліпіди розташовуються у воді суцільним бімолекулярним шаром, то білки могли б розташуватися на верхній і нижній поверхні цього шару. Утворюється щось подібне до бутерброда: зверху й знизу — два шари білка, а всередині ліпіди, на зразок масла. У такій примітивній формі «бутербродна» модель мембран запропонована американськими дослідниками Даніелі й Доусоном (1931) (рис. 5.2).
Згодом, з надходженням нових даних, її поступово вдосконалювали і змінювали. З’явилися факти, які суперечили «бутербродній» моделі та уявленням про її універсальність. Насамперед, якщо всі мембрани побудовані за єдиним принципом, то вони повинні містити однакову кількість ліпідів і білків. Виявилося, що мієлінова мембрана містить в 2,5 рази більше ліпідів, ніж білка, тоді як у мембрані еритроцитів співвідношення
1 |
3 |
|
2
а |
1 |
б |
Рис. 5.2. Моделі біомембрани:
а— за Даніелі — Доусоном;
б— за Стейном — Даніелі Позначення: 1 — білкові шари; 2 — ліпідний бішар;
3 — мембранні пори.
зворотне, а в мембранах деяких бактерій вміст білка в 5–6 разів перевищує кількість ліпідів.
«Бутербродна» модель виявилася також неспроможною пояснити той факт, що природні мембрани не розщеплюються на білки й ліпіди при додаванні в середовище неорганічних солей. У присутності солей слабшає електростатична взаємодія між білками й ліпідами, на якій грунтується ця модель. Штучно виготовлені моделі, в яких ліпіди й білки зв’язані електростатичними силами, у розчинах солей розпадаються, а природні мембрани чомусь виявляються стійкими.
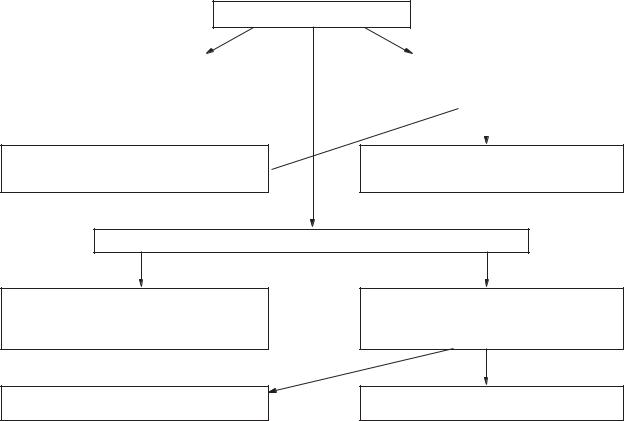
З’явилася нова модель мембрани — мозаїчна, відповідно до якої мембрана складається з білків, простір між якими заповнено ліпідними молекулами, тобто мембрана — це ліпідне море, в якому плавають білкові айсберги. Подальші детальні електронно-мікроскопічні дослідження підтвердили мозаїчну модель мембрани (рис. 5.3).
Відповідно до цієї моделі, присутні в мембрані білки розділяють на два типи:
1. Периферійні білки — це білки, прикріплені до зовнішньої поверхні мембрани електростатич-
1
2
Рис. 5.3. Рідинно-мозаїчна модель біомембрани за Сингером — Нікольсоном
Позначення: 1 — периферичні білки; 2 — інтегральні білки.
79
ними силами: а) сумарний позитивний заряд |
них важливе значення мають гази — кисень, вуг- |
білка й негативно заряджені голівки мембранних |
лекислий газ. Деякі невеликі полярні молекули |
ліпідів; б) більшість периферійних білків мають |
(Н2О, NH3, гліцерол, сечовина, етанол, наркоти- |
негативний сумарний заряд, тому пов’язані з го- |
ки) також здатні проникати крізь ліпідний бішар |
лівками не безпосередньо, а через катіони Са2+ і |
через міжмолекулярні пори. |
Мg2+. |
Розчинність багатьох речовин у жирах зале- |
2. Інтегральні білки — це білкові глобули, що |
жить від рН середовища. Багато молекул можуть |
плавають у «ліпідному морі» подібно до айс- |
існувати в протонованій формі (речовина + Н+) |
бергів, так що одна частина глобули занурена |
або в непротонованій формі. Непротонована мо- |
в мембрану, а друга — у водне середовище. Час- |
лекула проходить крізь мембрану легше, ніж про- |
тина білкових глобул («айсбергів») не вільно |
тонована. Однією з основних функцій мембран |
плаває у ліпідному морі, а зв’язана з цитоплаз- |
є регуляція надходження й виходу різних речо- |
матичними структурами клітини — мікротрубоч- |
вин у клітину та з клітини. Одні речовини вільно |
ками й мікрофіламентами. Деякі з інтегральних |
проходять через мембрану, а для інших вона не- |
білків другого типу пронизують мембрану |
проникна. Розрізняють такі шляхи транспорту |
наскрізь. Одна полярна ділянка пронизуючих |
речовин через мембрану: а) пасивний транспорт |
білків найчастіше несе вуглеводні ланцюги, ви- |
(проста та полегшена дифузія); б) активний |
ходить у зовнішній простір, а друга — у цито- |
транспорт. |
плазму. Між ними існує неполярна ділянка, що |
Гідрофільні речовини і великі полярні молеку- |
пронизує ліпідний бішар. Уявлення про мембра- |
ли, які не розчиняються в ліпідах, відштовхують- |
ну у вигляді мозаїчної моделі досить спрощене й |
ся ліпідною серцевиною мембрани. Щоб пройти |
схематичне. По-перше, у «ліпідному морі» у ба- |
крізь плазматичну мембрану, вони повинні взає- |
гатьох випадках більше «айсбергів», ніж «води». |
модіяти зі спеціальними білками-носіями або |
По-друге, не всі ліпіди, що входять до складу |
білком трансмембранного каналу (рис. 5.4). |
мембран, розташовані за принципом бішару. |
|
Мембранний транспорт
Незаряджені ліпофільні (жиророзчинні) речовини можуть безпосередньо проникати крізь ліпідну серцевину плазматичних мембран. Серед
Пасивний транспорт
Якщо мембрана клітини проникна для розчинної речовини, то ця речовина вільно переміщається з більш концентрованого розчину в менш концентрований, такий шлях транспорту
МЕМБРАННИЙ ТРАНСПОРТ
Пасивний транспорт — |
|
Полегшена дифузія — переміщення речовин |
|
переміщення речовин згідно з законом дифузії |
|
за градієнтом концентрації |
|
за градієнтом концентрації |
|
за участю мембранних переносників |
|
|
|
|
|
|
|
|
|
Нерухомі переносники формують канали Рухомі переносники (мала та велика каруселі) і забезпечують перенесення речовин,
і забезпечують перенесення речовин,
змінюючи свою конформацію
Активний транспорт — перенесення речовин проти градієнта концентрації
Первинний активний транспорт відбувається за рахунок енергії макроергів
Збіг напрямку переміщення двох речовин — симпорт (Na+ і глюкоза)
Вторинний активний транспорт відбувається за рахунок первинного активного транспорту однієї речовини, який створює умови
для транспорту іншої речовини
Протилежно спрямоване переміщення — антипорт (Na+-К+-насос)
Рис. 5.4. Мембранний транспорт
80
речовин через мембрани називають пасивним транспортом.
Якщо речовина добре розчинна в жирах, то вона переміщається через будь-яку ділянку мембрани за звичайними законами дифузії, тобто відбувається процес простої дифузії. Транспорт через мембрану води й невеликих, незаряджених молекул (не розчинних у жирах) здійснюється через тимчасові порожнечі (діри) у мембрані. Вони утворюються внаслідок того, що вуглеводневі ланцюги ліпідів постійно звиваються, у мембрані утворюються тимчасові порожнини, по яких і проходять молекули. Більші молекули, що дифундують, у тому числі й такі, що несуть електричні заряди, проходять крізь мембрану по спеціальних каналах (порах), стінки яких вистелені білками. Проста (звичайна) дифузія розчиненої речовини, яка не має заряду, прямо пропорційна градієнту його концентрації; його коефіцієнту дифузії; площі мембрани; зворотно пропорційна товщині мембрани.
Сторонні речовини можуть проходити крізь мембрани шляхом пасивного транспорту всередину клітини, якщо вони ліпофільні.
Полегшена дифузія (уніпорт) відрізняється від звичайної тільки тим, що відбувається з рухливим переносником, який полегшує проходження речовини за градієнтом концентрації. Так транспортуються великі полярні молекули. Вони транспортуються білками-переносниками, а заряджені іони — білками трансмембранних ка-
налів. Транспорт шляхом полегшеної дифузії використовується для перенесення органічних кислот, моносахаридів, жиророзчинних вітамінів, стероїдних гормонів. У випадку полегшеної дифузії транспорт речовин через мембрану також відбувається за градієнтом концентрації, тобто відбувається процес дифузії, вирівнювання концентрації речовин по різні боки мембрани. Однак при полегшеній дифузії транспорту речовин за градієнтом концентрації «допомагають» спеціальні мембранні переносники. З їхньою допомогою дифузія речовин відбувається значно швидше, тобто швидкість дифузії зростає. Транспорт речовин за допомогою переносників відрізняється від простої дифузії не тільки більшою швидкістю, але й тим, що ця швидкість залежить не тільки від градієнта концентрації, але й від потужності переносника. Крім цього, транспорт речовин за участю переносника можна сповільнити за допомогою інгібітора. При цьому інгібітор займає місце на переноснику, але сам через мембрану не проходить. Ще одна особливість полегшеної дифузії — переносники молекул й іонів мають специфічність (вибірковість), тобто переносять не всі молекули й іони, а тільки певні, наприклад, якийсь один моносахарид (глюкозу, галактозу), якусь одну амінокислоту і т. ін. За принципом дії мембранні переносники поділяються на два типи: рухливі переносники і нерухливі.
Рухливі переносники діють за типом порома. Приєднавши до себе молекули, вони переміщуються разом із ними крізь мембрани й повертаються назад або порожніми, або захоплюють молекули інших сполук.
Рухливі переносники можуть бути двох видів: а) працюючі за принципом «малої каруселі»; б) працюючі за принципом «великої каруселі».
Якщо переносник погано розчинний у воді, то він реагує з молекулами, які переносить, й іонами на поверхні мембрани, тобто працює за принципом «малої каруселі». Інші переносники добре розчинні у воді, тому виходять на «полювання» з мембрани, захоплюють потрібну молекулу або іон, переміщуються разом через мембрану, виводять її на протилежну сторону й там відпускають приєднану речовину, тобто працюють за принципом «великої каруселі».
Рухливі переносники можуть робити під час переносу обертові рухи (обертовий переносник) або поступальні (рухливий переносник).
Нерухливі переносники не здійснюють човникових рухів, а вбудовуються в мембрану, утворюючи фіксований канал. Ці переносники, як правило, є білками. Такі транспортні білки забезпечують перенос, змінюючи свою конформацію, тобто стінки каналів можуть розширюватися й скорочуватися, внаслідок чого в мембрані відкриваються канали. Відомо, що транспортні білки переносять такі гідрофільні речовини, як моносахариди, амінокислоти, іони Nа+, К+ і Са2+.
Переносники можуть бути змішаного типу: 1) обертовий переносник разом із фіксованим — при цьому обертовий переносник транспортує молекули до каналу, а далі вони переносяться по каналу; 2) рухливий переносник разом із фіксованим — працює як і попередній, тільки не обертається.
1. Більшість іонних каналів відіграє роль селективого (вибіркового) фільтра, який вибірково перепускає іони тільки одного типу. Так, натрієві канали перепускають в основному іони натрію, а калієві канали — іони калію, але не перепускають інші види іонів.
Чим іонний канал відрізняється від пори? Мембранні пори — це щілини між молекулами ліпідів, які забезпечують просту дифузію в мембрані. Іонні канали — це отвори з воротами, які можуть знаходитись у відчиненому або зачиненому стані й регулювати швидкість надходження іонів крізь мембрану. Іони можуть надходити крізь канал, тільки якщо він відчинений.
Які три основних конформаційних стани іонного каналу? Стан спокою — канал зачинений, але готовий до відкриття у відповідь на хімічний або електричний імпульс. Стан активації — канал відчинений і забезпечує надходження іонів. Стан інактивації — канал зачинений і нездатний до активації. Стан інактивації розвивається одразу після успішної активації (відкриття) каналу у відповідь на хімічний або електричний імпульс.
Лігандзалежні іонні канали хімічно регулюються і тісно пов’язані з мембранним рецептором. Зв’язування хімічного посередника з даним рецептором спричинює конформаційні зміни в каналі, які викликають його відчинення. Лігандзалежні канали часто бувають неселективними іонними каналами, які у відкритому стані перепус-
81
кають більше одного типу однаково заряджених іонів. Наприклад, зв’язування ацетилхоліну з рецептором на мембрані скелетного м’яза активує лігандзалежний іонний канал, який при фізіологічних умовах мембранного потенціалу переносить іони натрію всередину клітини й іони калію
—з клітини.
Потенціалзалежні іонні канали відчиняються
при зміні мембранного потенціалу. Зміни електричного поля, яке оточує іонний канал, спричинюють зміщення позитивно заряджених амінокислотних залишків α -субодиниці, що утворюють стінки каналу, і переводить канал у відкритий стан. Ряд селективних іонних каналів, які забезпечують клітинну збудливість (наприклад, Na+-, K+-, Ca2+-канали), належать до потенціалзалежних.
2. На відміну від іонних каналів, транспортні білки вибірково зв’язуються молекулами субстрату і за рахунок конформаційних змін переносять їх крізь мембрану. Цим транспортні білки (білкипереносники, пермеази) схожі на ферменти. Різниця полягає в тому, що вони «каталізують» направлений транспорт, а не ферментативну реакцію. Білки-транспортери виявляють специфічність (іноді групову) до субстратів, які підлягають переносу.
Активний транспорт
Активний транспорт є ферментативним процесом. Він здійснюється спеціальними транспортними системами, здатними використовувати хімічну енергію АТФ або енергію електрохімічного потенціалу для транспортування речовин. Залежно від виду використаної енергії активний транспорт може бути первинним і вторинним. Первинний активний транспорт відбувається за рахунок енергії, яка утворюється безпосередньо при гідролізі АТФ або деяких інших макроергічних фосфатів; вторинний активний транспорт — за рахунок енергії, яка утворюється за допомогою первинного активного транспорту внаслідок неоднакових концентрацій іонів по обидві сторони мембрани. При вторинному активному транспорті одна речовина (А) створює умови для проходження іншої речовини (В). Причому напрямок переміщення крізь мембрану двох речовин або співпадає, або не співпадає.
Якщо речовина транспортується в одному напрямку (наприклад, Na+ і глюкоза), то такий спільний транспорт має назву симпорт (котранспорт). Якщо речовини перетинають мембрану в протилежних напрямках, то такий транспорт має назву антипорт (зустрічний транспорт). При цьому транспорт речовин через мембрану відбувається проти градієнта концентрації (від розчину з меншою концентрацією даної речовини —
урозчин із більшою концентрацією), тобто мембрана діє подібно до насосу. Це енергозалежний процес, для його здійснення використовується, головним чином, енергія АТФ. Наприклад, звичайно концентрація білка й інших макромолекул
уклітині вища, ніж у навколишньому середовищі. На відміну від води, ці макромолекули не
проходять вільно через мембрану, тому вода за законами осмосу входить у клітину, збільшуючи цим внутрішній тиск, — клітина починає набухати. Щоб протистояти надходженню води, клітини запускають біологічний насос, що викачує назовні іони натрію. У результаті цього внутрішня ділянка клітини здобуває негативний заряд щодо оточуючого її середовища. Одночасно насос накачує іони калію з оточуючого середовища у внутрішнє середовище клітини. У результаті концентрація іонів натрію стає вищою поза клітиною, а калію — всередині клітини. Так працює калій-натрієвий насос — це натрій-калій залежна АТФаза. Цей фермент звичайно розташований у мембранах і активується при підвищенні концентрації Nа+ усередині клітини або К+
— у зовнішньому середовищі. На переміщення трьох іонів Nа+ і двох іонів К+ витрачається енергія однієї молекули АТФ. На транспорт двох іонів Са2+ через мембрану також використовується одна молекула АТФ.
У клітинах спостерігається процес, коли градієнт концентрації однієї сполуки використовується для транспорту іншої, що дістало назву
вторинно-активного транспорту. Наприклад,
під час функціонування Na+/K+-АТФази і переміщення іонів Nа+ і К+ відбувається надходження до клітин глюкози, амінокислот і виведення з клітин кінцевих продуктів обміну.
Основні процеси, за допомогою яких речовини проходять через клітинні мембрани
Первинний активний транспорт
Шляхом первинного активного транспорту переносяться іони Натрію, Кальцію і Магнію через клітинну мембрану, а протони — через мітохондріальну мембрану. Транспортними системами служать спеціальні АТФази, які гідролізують АТФ до АДФ і неорганічного фосфату й використовують енергію фосфатних зв’язків на перенесення іонів крізь мембрану. Для кожного з іонів існує своя специфічна АТФаза.
Na+ , K+-АТФаза присутня у всіх клітинах організмів рослинного і тваринного походження, у бактеріях. В організмі людини найвища активність її в нервовій тканині, нирках і секреторних органах, тобто там, де найбільше виражені процеси активного транспорту речовин. Na+, K+-АТФаза локалізована переважно у клітинній мембрані.
Na+, K+-АТФаза (насос)
Складається з двох α -субодиниць, які утворюють основний транспортний білок, і двох
β-субодиниць. Більші α -субодиниці містять ділянку зв’язування кардіотонічних стероїдних інгібіторів і ділянку зв’язування АТФ. Менші
β-субодиниці містять вуглеводні групи, у плазматичній мембрані вони розташовані ближче до її зовнішньої сторони (як і більшість глікопро-
теїнів мембран) і просторово розділені двома α -субодиницями (рис. 5.5).
Натрієвий насос працює в такий спосіб. На внутрішній стороні плазматичної мембрани роз-
82
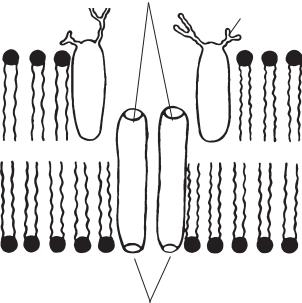
Ділянки зв’язування стероїдного інгібітора
Залишки цукру
β
αα
Поверхня мембрани, звернена до цитозолю
Ділянки зв’язування АТР
Рис. 5.5. Схематичне зображення субодиничної структури і розташування в мембрані Na+, K+-насоса
ташовані центри Nа+, К+-АТФази, що вибірково приєднують три іони Натрію. Зв’язування натрію ініціює фосфорилування Nа+, К+-АТФа- зи (фосфат від АТФ як донора приєднується складноефірним зв’язком до вільної карбоксильної групи залишку аспарагінової кислоти). У результаті фосфорилування утворюється фосфорильована форма ферменту — Nа+-Е~P. Після цього відбуваються конформаційні зміни Nа+, К+- АТФази, у ході яких центри зв’язування ферменту разом з іонами Натрію виявляються на зовнішній стороні плазматичної мембрани, де відбувається вивільнення іонів Натрію. На конформаційні зміни і вивільнення іонів Натрію витрачається енергія макроергічного зв’язку Nа+-Е~Р. Е-Р зв’язує два іони Калію із зовнішнього середовища й утворює комплекс К+-Е-Р. Приєднання К+ до Е-Р стимулює К+-Е-Р, що приводить до дефосфорилування і конформаційних змін К+-Е. Конформаційні зміни поєднані з переміщенням двох іонів Калію із зовнішньої поверхні мембрани на внутрішню, де відбувається вивільнення іонів Калію. Цим закінчується цикл роботи натрієвого насоса: зв’язування Nа+ — фосфорилування — зміна конформації — вивільнення Nа+
— зв’язування К+ — дефосфорилування — зміна конформації — вивільнення К+. Під дією Na+, K+- АТФази іони Натрію постійно виходять із клітини, а іони Калію надходять із позаклітинного середовища всередину клітини, тобто спостерігається антипорт цих іонів. Серед регуляторів Na+, K+-АТФази існують інгібітори й активатори. Її природним регулятором є іони Кальцію. Позаклітинні іони Кальцію активують зв’язування зовнішнього калію специфічною ділянкою ферменту і включають роботу Na+, K+-АТФази з транспорту іонів. Надлишок внутрішньоклітинного кальцію блокує Na+, K+-АТФазу, і
тільки усунення високих концентрацій внутрішньоклітинного кальцію іншими системами дозволяє включити Na+, K+-насос. Класичними інгібіторами ферменту є серцеві глікозиди, широко використовувані в медичній практиці як стимулятори серцевих скорочень. Глікозиди інгібують Na+, K+-АТФазу, зв’язуючись із ділянками ферменту, оберненими на зовнішню сторону клітинної мембрани, тобто конкурують за місце зв’язування з іонами калію. Якщо глікозидами діяти на фермент із внутрішньої сторони, то вони ніякого впливу на функцію Na+, K+-насоса не чинять. Тому дії серцевих глікозидів можна перешкодити іонами Калію, що використовується в медичній практиці, коли вводять в організм розчини солей калію при отруєнні серцевими глікозидами. Інгібіторами ферменту є також тетраетиламоній, іони Купруму, Феруму, деякі гормони (естрогени, глюкагон, адреналін). Активують Na+, K+-АТФазу природні амінокислоти, дипептиди (карнозин, ансерин). Збільшують кількість цього ферменту в нирках кортикостероїди (особливо альдостерон).
Са2+-АТФаза (кальцієвий насос)
Са2+-АТФаза (або кальцієвий насос) знаходиться у клітинній і позаклітинній мембранах ендоплазматичного ретикулума та мітохондрій. Висока активність Са2+-АТФази відмічається в м’язовій (особливо в саркоплазматичному ретикулумі), у нервовій тканині, нирках, тобто там, де процеси активного транспорту визначають функцію органів і тканин. Са2+-АТФаза відкачує іони Кальцію за рахунок енергії АТФ в обмін на іони Натрію або Магнію, тобто відбувається антипорт цих іонів. Са2+-АТФаза мембран мітохондрій обмінює іони Кальцію на іони Гідрогену, причому іони Кальцію надходять усередину мітохондрій, а протони — назовні.
Вторинний активний транспорт (антипорт)
Натрій-гідрогенний насос використовує електрохімічний градієнт іонів Натрію, створений Na+, K+-насосом, для перенесення протонів із клітини за механізмом вторинного активного транспорту. При цьому процесі зв’язування позаклітинного натрію і внутрішньоклітинних протонів із протилежними сторонами білка-перенос- ника приводить до конформаційних змін його структури і положення в мембрані. Перенесення іонів Натрію в клітину й іонів Гідрогену з клітини, що відбувається при цьому, служить буферним механізмом, який запобігає закисненню у клітині. У мембрані еритроцитів іони НСО3– обмінюються на іони Хлору.
КОНТРОЛЬНІ ПИТАННЯ
1.Біологічні мембрани: мембранні структури тваринної клітини та їх функції; молекулярні компоненти біомембран.
2.Ліпіди біомембран: особливості їх структурної організації, ліпідний склад субклітинних мембран, молекулярні моделі мембранних ліпідів.
3.Рідинно-мозаїчна модель будови біомембран; біофізичні властивості мембран.
83