Материал: Біологічна та біоорганічна хімія_Мардашко О.О._ изд. 2008-342 с._ОНМедУ-2012
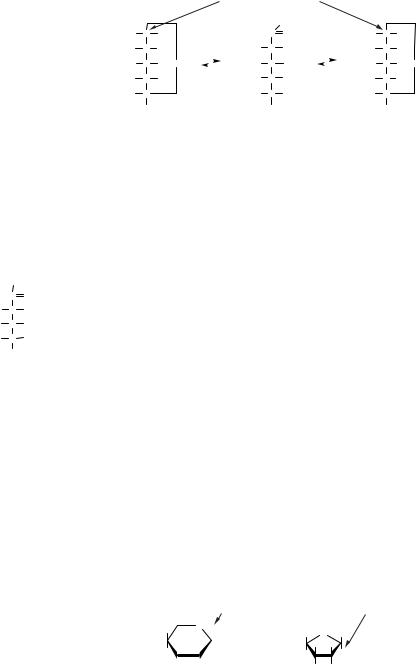
(від грецьк. сheir — рука), тобто являють собою |
атомів. Вперше припущення про циклічну будо- |
||||||||||
дзеркальне зображення. У проекційній формулі |
ву глюкози висунув дослідник А. О. Коллі (1870), |
||||||||||
D-гліцеральдегідів гідроксильна група знахо- |
а згодом — німецький учений Б. Толленс (1883). |
||||||||||
диться праворуч біля «кінцевого» хірального цен- |
У п’яти- і шестивуглецевих ланцюгах може спо- |
||||||||||
тру, а в L-гліцеральдегіді — ліворуч. D- і L-гліце- |
стерігатися зближення в просторі двох функціо- |
||||||||||
ральдегід є енантіомерами (стереоізомери, що |
нальних груп — альдегідної (кетонної) і гідрок- |
||||||||||
співвідносяться між собою як предмет і несумісне |
сильної біля С-4 чи С-5 атома Карбону. За ра- |
||||||||||
з ним дзеркальне зображення). Наявність хіраль- |
хунок цієї внутрішньомолекулярної взаємодії ут- |
||||||||||
них центрів у молекулі моносахаридів свідчить |
ворюється внутрішній циклічний напівацеталь. |
||||||||||
про те, що вони мають оптичну активність, тоб- |
Якщо утворюється п’ятичленна циклічна по- |
||||||||||
то здатні обертати плоскополяризоване світло за |
хідна, замкнена на атом Оксигену, то цикл на- |
||||||||||
годинниковою стрілкою або проти неї (вправо- |
зивається фуранозним, а якщо шестичленна — то |
||||||||||
вліво). Знак обертання площини поляризації |
піранозним. ОН-групу, що утворилася, назива- |
||||||||||
світла моносахаридами не пов’язаний з їх при- |
ють напівацетальною, чи глікозидною. Наприк- |
||||||||||
належністю до D- чи L-рядів. Він визначається |
лад, глюкоза існує в п’яти формах, із них — чо- |
||||||||||
експериментально і залежить від вкладу всіх |
тири циклічних. |
|
|
|
|
|
|
||||
хіральних центрів у молекулі. Оптичну ак- |
|
|
|
|
|
Аномерний центр |
|
|
|||
тивність вуглеводів позначають знаком (+) для |
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
правообертаючих сполук і знаком (–) — для |
|
|
|
|
|
1C |
H |
|
|
||
лівообертаючих. Серед альдогексоз і кетогексоз |
H C |
OH |
O |
|
HO C H |
||||||
D-стереохімічного ряду є як лівообертаючі, так і |
H C OH |
H 2C |
OH |
|
H C OH |
||||||
правообертаючі сполуки. Для зображення стерео- |
HO C |
H O |
|
|
|
HO 3C |
H |
|
|
|
HO C H O |
|
|
|
|
|
|||||||
|
|
|
|
|
|
||||||
ізомерів у моносахаридах користуються проек- |
H C |
OH |
H 4C |
OH |
|
H C OH |
|||||
ційними формулами Фішера. |
H C |
|
|
|
|
H 5C |
OH |
|
H C |
||
|
|
|
|
|
O |
|
|
|
|
|
|
O |
|
|
|
CH2OH |
|
|
|
6CH2OH |
CH2OH |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
α -D-Глюкоза |
|
|
|
D-Глюкоза |
β -D-Глюкоза |
|||
|
|
|
|
C |
|
H |
|
|
C |
|
|
H |
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(циклічна) |
|
(відкрита форма) |
(циклічна) |
||||||
H |
|
|
|
C |
|
OH |
HO |
|
C |
|
|
H |
|
||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(формула |
|
|
|
(формула |
(формула |
|||||
HO |
|
|
C |
|
|
H |
HO |
|
C |
|
|
|
H |
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Коллі – Толленса) |
Фішера) |
Коллі – Толленса) |
|||||||
H |
|
|
C |
|
|
OH |
H |
|
C |
|
|
|
OH |
||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
H |
|
|
C |
|
|
OH |
H |
|
C |
|
|
|
OH |
У циклічній формулі виникає додатковий |
|||||||||||||
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
CH2OH |
|
|
CH2OH |
||||||||||||||||||||
|
|
|
|
|
|
центр хіральності, |
який називають аномерним, а |
||||||||||||||||||||
|
|
|
|
|
|
І |
|
|
|
|
|
|
|
|
|
ІІ |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
два стереоізомери, що утворилися, — α - і β -ано- |
||||||||||||
D(+)-Глюкоза |
L(–)-Глюкоза |
||||||||||||||||||||||||||
мерами. В α -аномері конфігурація аномерного |
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
центру збігається з конфігурацією «кінцевого» |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
хірального центру в молекулі моносахариду, а у |
||||||||||
|
|
|
|
|
|
|
|
|
H |
|
|
CH2OH |
|||||||||||||||
|
|
|
|
|
C |
|
|
|
|
|
β -аномері вона є протилежною. У цілому α - і |
||||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
C |
O |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
HO |
|
C |
|
|
H |
|
β -аномери через наявність ще кількох центрів |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
HO |
|
|
|
|
|
|
|
H |
HO C |
H |
|||||||||||||||||
|
|
C |
|
|
|
|
хіральності в молекулі є діастереомерами, а не |
||||||||||||||||||||
|
|
|
|
|
H C |
OH |
|||||||||||||||||||||
H |
|
|
|
|
|
|
|
OH |
|||||||||||||||||||
|
|
C |
|
|
|
|
енантіомерами. |
|
|
|
|||||||||||||||||
|
|
|
|
|
|
H C |
OH |
|
|
|
|||||||||||||||||
H |
|
|
|
|
|
|
|
OH |
|
|
|
||||||||||||||||
|
|
C |
|
|
|
|
Аномери — це окремий випадок епімерів. Для |
||||||||||||||||||||
|
|
|
|
|
|
|
CH2OH |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
CH2OH |
|
зображення кисневмісних циклів зручно користу- |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
ІІІ |
|
|
|
|
|
|
|
ІV |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
ватися формулами не Коллі — Толленса, а Хеу- |
||||||||||||||
D(+)-Маноза |
D(–)-Фруктоза |
орса. Вони мають вигляд плоских багатокут- |
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ників, розташованих перпендикулярно до площи- |
||||||||
Сполуки I, III, IV належать до D-генетично- |
ни рисунка. Атом Оксигену розміщується в піра- |
||||||||||||||||||||||||||
го ряду, IІ — до L-ряду. |
|
|
|
|
|
|
|
|
нозах у далекому правому куті циклу, а в фура- |
||||||||||||||||||
Оптичні ізомери I і II — енантіомери; I і III — |
нозах — за площиною рисунка. У циклічній фор- |
||||||||||||||||||||||||||
епімери. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
мулі виникає додатковий центр хіральності — |
|||||||||||
Епімерами називають діастереомери, які |
атом Карбону, що раніше входив до складу кар- |
||||||||||||||||||||||||||
відрізняються за конфігурацією тільки одного |
бонільної групи. Цей атом називається аномер- |
||||||||||||||||||||||||||
асиметричного атома Карбону (для I і III — це |
ним, а два відповідних стереоізомери — α - і β -ано- |
||||||||||||||||||||||||||
С-2). |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
мерами. У α -аномера конфігурація аномерного |
|||||||||||
Переважна більшість природних моносаха- |
центру однакова з конфігурацією «кінцевого» |
||||||||||||||||||||||||||
ридів належить до D-ряду. Живі організми не |
хірального центру, що визначає приналежність до |
||||||||||||||||||||||||||
«впізнають» і не вміють переробляти L-глюкозу; |
D- чи L-ряду, а в β |
-аномера — протилежна. |
|||||||||||||||||||||||||
L-глюкоза не піддається спиртовому бродінню |
Глікозильний гідроксил |
Глікозильний гідроксил |
|||||||||||||||||||||||||
дріжджовими клітинами. |
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
α -аномера |
|
|
β -аномера |
||||||||||||||||
Кількість виділених ізомерів виявилася вдвічі |
|
|
|||||||||||||||||||||||||
5 |
|
O OH |
|
|
|
||||||||||||||||||||||
більшою, ніж слід очікувати за формулою Фіше- |
|
|
|
|
|||||||||||||||||||||||
4 |
|
|
|
O |
|||||||||||||||||||||||
ра: N=2n. Відомі 32 ізомери альдогексоз (замість |
|
|
|
1 |
|
|
|||||||||||||||||||||
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
OH |
||||||||||||||||||||
16). Для всіх альдогексоз, виділених із живих |
|
|
|
|
|
|
|
||||||||||||||||||||
|
3 |
|
2 |
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
||||||||||||||||||||||
організмів чи синтезованих, встановлені відносні |
Піранозний цикл |
Фуранозний цикл |
|||||||||||||||||||||||||
конфігурації |
замісників |
біля асиметричних |
|||||||||||||||||||||||||
(β -піранозний цикл) |
(α -фуранозний цикл) |
||||||||||||||||||||||||||
54
Перехід від проекційних формул до формул |
У суміші таутомерів превалюють піранозні |
|
Хеуорса здійснюється таким чином. Усі замісни- |
форми. Оксоформа, а також таутомери з фура- |
|
ки, що знаходяться ліворуч від вуглецевого лан- |
нозними циклами містяться у малих кількостях. |
|
цюга, розміщуються над площиною оксидного |
Аналогічні таутомерні перетворення відбувають- |
|
циклу, а праворуч — під площиною. В альдогек- |
ся у кетогексоз за переважання фуранозних |
|
соз D-ряду СН2ОН-група завжди розміщується |
форм. |
|
над площиною. У твердому стані моносахариди |
Конформації |
|
мають циклічну будову. Залежно від розчинни- |
||
Хоча у формулах Хеуорса моносахариди зоб- |
||
ка під час перекристалізації глюкопіраноза може |
||
бути виділена в α -формі ([α ]=+112°) — питомий |
ражуються у вигляді плоского багатокутника, у |
|
кут обертання — або в β -формі ([α ]=+19°). Через |
дійсності вони не мають плоскої будови. Наприк- |
|
деякий час свіжоприготовлений розчин глюкози |
лад, шестичленний піранозний цикл подібно до |
|
поступово змінює питомий кут обертання до |
циклогексану набуває найбільш вигідної кон- |
|
+52,5°. Зміна з часом кута обертання площини |
формації крісла. |
|
поляризації світла розчинами цукрів називаєть- |
Методом рентгеноструктурного аналізу вста- |
|
ся мутаротацією. Хімічна основа мутаротації — |
новлено, що з двох кріслоподібних конформацій |
|
здатність цукрів до цикло-оксо-таутомерії, або |
піранозного циклу в β -D-глюкопіранозі відбу- |
|
кільцево-ланцюгової таутомерії. |
вається та, в якій усі великі за розміром замісни- |
|
|
ки перебувають в екваторіальному стані: |
|
CH2OH |
|
|
|
|
|
H |
|
O |
|
|
CH2OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
C |
|
|
|
|
OH |
CH2OH |
|
OH |
CH2OH |
|
||||||||||||||||||||||
|
|
|
O |
|
|
|
|
|
H |
|
|
OH |
|
|
|
|
O |
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
O |
|
|||||
H H |
|
|
H |
|
|
|
|
H H |
|
|
|
H |
|
|
|
H |
|
|
|
|||||||||||||||||||||
|
|
|
HO |
|
|
H |
|
|
|
|
|
|
|
|
H |
|
|
|
H |
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
OH |
H |
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
H |
H |
H |
OH |
|||||||||||||||||||
|
|
|
H |
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
HO |
OH |
|
HO |
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
H |
HO |
|
|
|
|
HO |
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
H |
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
OH H |
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
OH |
|
|
|
H |
|
|
OH |
|
H |
|
|
|
|||||||||||||
|
H |
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
CH2OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
α -D-Глюкопіраноза |
β -D-Глюкопіраноза |
|||||||||||||||||||
α -D(+)-Глюко- |
|
D-Глюкоза |
|
β -D(+)-Глюко- |
||||||||||||||||||||||||||||||||||||
|
|
(30 %) |
|
(70 %) |
|
|||||||||||||||||||||||||||||||||||
піраноза (36 %) |
|
(формула |
|
піраноза (64 %) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
(формула Хеуорса) Фішера) (формула Хеуорса)
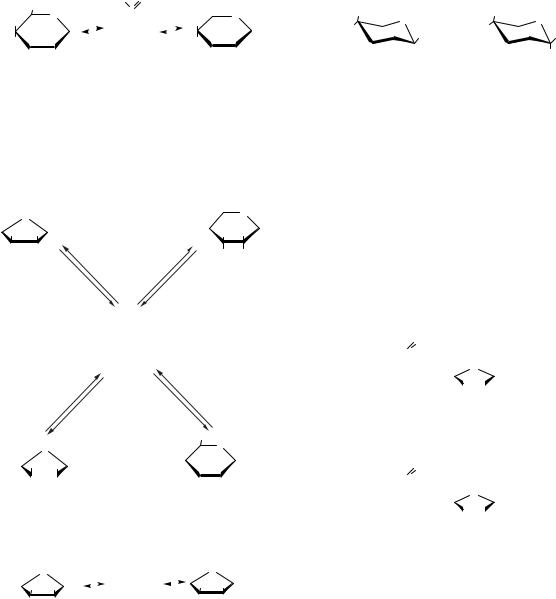
Таким чином, у водному розчині D-глюкоза існує у вигляді п’яти таутомерів: α - і β -аномерів піранозних і фуранозних циклічних форм й оксиформи (рис. 3.2).
|
CH2OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2OH |
|
|
|||||||||||||
HO |
|
|
H O |
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
O |
H |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
||||||||||||||
|
|
|
OH |
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HO OH H |
OH |
|||||||||||||||
|
H |
|
|
|
|
|
OH |
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
H |
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
OH |
|
|
|||||||
α -D(+)-Глюко- |
|
|
|
|
α -D(+)-Глюко- |
||||||||||||||||||||||||||
|
|
|
|
піраноза (36 %) |
|||||||||||||||||||||||||||
|
фураноза |
|
|
|
|
|
|
|
|
|
|
|
|
(формула |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
Хеуорса) |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
HO |
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2OH |
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
D-Глюкоза |
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
(формула |
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
Фішера) |
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
CH2OH |
|
|
|
|
|
|
|
|
|
|
CH2OH |
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
||||||||
|
|
HO |
|
|
H O |
|
|
|
|
|
|
|
|
H |
|
|
|
H |
|
|
|||||||||||
|
|
|
|
OH |
H |
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
H |
|
|
|
|
OH H |
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
HO |
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
OH |
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
H |
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
H |
OH |
|
|
|
|
H OH |
|
|
|
|
|
|||||||||||||
β -D(+)-Глюкофура- |
β -D(+)-Глюкопіраноза (64 %) |
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
ноза |
|
|
(формула Хеуорса) |
|||||||||||||||||||||
У β -аномері всі великі за розміром замісники перебувають у більш енергетично вигідному екваторіальному стані, тому він переважає в суміші.
β -D-глюкопіраноза — унікальний моносахарид із повним екваторіальним розміщенням замісників. Цим зумовлена його висока термодинамічна стійкість, що є основною причиною його широкого розповсюдження в природі.
Пентози
Біологічно важливими пентозами є:
—альдопентози: D-рибоза, 2-дезокси-D-рибо- за, L-арабіноза, D-ксилоза;
—кетопентози: D-рибулоза, D-ксилулоза.
|
1C |
|
O |
|
|
|
|
|
|||
|
|
H |
5 |
CH2OH |
|||||||
|
|
||||||||||
H |
2 |
|
|
OH |
|
||||||
|
|
|
|||||||||
|
|
|
|||||||||
H |
3 |
|
|
OH |
|
4 |
|
O |
|
~OH |
|
|
|
|
|
|
|
||||||
H |
4 |
|
|
OH |
|
|
|
|
1 |
||
|
|
|
|
3 |
2 |
|
|||||
|
|
|
|||||||||
5 |
|
|
|
|
|
|
OH |
OH |
|||
|
CH2OH |
|
|||||||||
D-Рибоза |
D-Рибофураноза |
|||||||||||
(ф-ла Фішера) |
|
(ф-ла Хеуорса) |
||||||||||
|
1C |
|
|
O |
|
|
|
|
|
|||
|
|
H |
5 |
CH2OH |
||||||||
|
|
|||||||||||
H 2 |
|
|
|
H |
|
|||||||
H |
3 |
|
|
|
OH |
|
4 |
|
O |
|
~OH |
|
|
|
|
|
|
|
|
||||||
H |
4 |
|
|
|
OH |
|
|
|
|
1 |
||
|
|
|
|
|
3 |
2 |
|
|||||
|
|
|
||||||||||
5 |
|
|
|
|
|
|
|
OH |
|
|
||
|
CH2OH |
|
|
|
||||||||
|
|
|
HOH C |
|
|
|
|
|
|
|
|
|
|
CH2OH |
|
|
||||||||||
CH OH |
|
|
|
C |
|
OH |
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|||||||||||||||||||||
|
|
2 O |
OH |
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
O |
|
CH2OH |
||||||
|
|
|
|
|
HO |
|
C |
|
H O |
|
||||||||||||||||
|
H |
OH |
|
|
|
|
|
|
|
|
H |
OH |
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
H |
|
C |
|
OH |
|
|
|
|
|
|
|
|
|
OH |
||
H |
|
|
|
CH2OH |
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|||||||
|
|
OH |
H |
|
|
|
|
|
H |
|
C |
|
|
|
|
|
|
|
OH |
H |
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
β -D-Фруктофура- |
|
|
|
|
|
CH2OH |
α -D-Фруктофура- |
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
ноза |
|
|
|
|
D-Фруктоза |
|
|
|
|
|
ноза |
|||||||||||||||
Рис. 3.2. Таутомери D-глюкози
2-Дезокси-D-рибоза 2-Дезокси-D-рибо- (ф-ла Фішера) фураноза (ф-ла Хеуорса)
D-рибоза — альдопентоза, у β -фуранозній формі входить до складу рибонуклеїнових кислот, ряду коферментів (НАД+, НАДФ+, ФАД, ФМН), глікозидів і антибіотиків.
2-Дезокси-D-рибоза (дезоксирибоза) — альдопентоза, відрізняється від D-рибози відсутністю
55
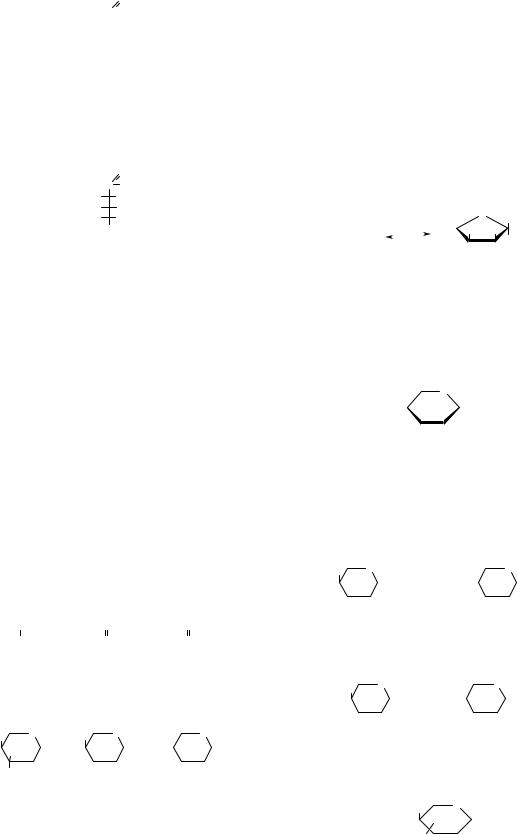
ОН-групи у С-2. Входить до складу дезоксирибонуклеїнових кислот.
|
|
|
1C |
|
|
O |
||
|
|
|
|
|
|
H |
||
|
|
|
|
|
|
|||
HO |
2 |
|
|
|
H |
|||
|
|
|
|
|||||
H |
3 |
|
|
|
OH |
|||
|
|
|
|
|||||
H |
4 |
|
|
|
OH |
|||
|
|
|
|
|
||||
5 |
|
|
|
|
|
|||
|
|
|
CH2OH |
|||||
D-Арабіноза
L-Арабіноза, D-арабіноза виявлені в природі в складі деяких полісахаридів, наприклад, гуміарабіку, полісахаридах туберкульозної палички. У вільному вигляді міститься в хвойних деревах.
O 1C H
H 2 OH
HO 3 H
H 54 OH
CH2OH
D-Ксилоза
D-Ксилоза зустрічається в рослинних ксиланах, застосовується в кондитерському виробництві, а також для синтезу ксиліту, що використовується як лікарський засіб.
D-Рибулоза, D-ксилулоза — кетопентози, що у вигляді фосфорних ефірів утворюються в організмі людини (пентозофосфатний цикл).
|
|
CH2OH |
|
|
|
CH2OH |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
O |
|
|
C |
|
|
|
O |
||
|
|
|
|
|
|
||||||||
H |
|
|
|
OH |
HO |
|
|
|
|
H |
|||
|
|
|
|
|
|
|
|||||||
H |
|
|
|
OH |
H |
|
|
|
|
|
OH |
||
|
|
|
|
|
|
|
|||||||
|
|
CH2OH |
|
|
|
CH2OH |
|||||||
D-Галактоза (молочний цукор) входить до складу дисахариду лактози, що міститься в молоці, а також до складу гетерополісахаридів (про-
теогліканів).
D-Маноза рідко зустрічається у вільному стані (шкірка цитрусових), вельми поширена в полісахаридах (мананах), рослинних і бактеріальних глікопротеїнах. У тваринному організмі входить до складу олігосахаридної частини мембран гліколіпідів і глікопротеїнів. Продукт відновлення манози — шестиатомний спирт манітол (маніт) — використовується в медицині як осмотичний діуретик і замінник цукру при цукровому діабеті.
D-Фруктоза (плодовий цукор), подібно D-глюкозі, міститься в плодах рослин, у меді.
|
|
CH2OH |
|
|
|
|
|
|
|
O |
|
|
|||||||
|
|
|
|
|
|
|
|
|
HOH2C |
|
|
|
CH2OH |
||||||
|
|
C |
|
|
O |
|
|
|
|||||||||||
|
|
|
|
|
|
H |
HO |
|
|||||||||||
HO |
|
|
|
H |
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
H |
|
|
|
|
|
|
OH |
||||||
H |
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
OH |
H |
|
|
|||||||
H |
|
|
|
|
OH |
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
CH2OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
α ,D(–)-Фруктофураноза
D-Фукоза виявлена у таких глікопротеїнах крові, як групоспецифічні речовини, антибіотики, у складі слизів (наприклад, травного каналу, сперматозоїдів).
|
|
|
CH3 |
O |
|
|
||
HO |
|
|
|
|
OH |
|||
|
H |
|
|
|
||||
|
|
|
OH |
H |
|
|
||
H |
H |
|||||||
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
H |
OH |
|
|
|||
D-Рибулоза |
D-Ксилулоза |
β -L-Фукоза (6-дезокси-β -L-галактоза) |
|||||||||||
|
Гексози |
Амінопохідні моносахаридів (аміноцукри) |
|||||||||||
Серед гексоз до альдогексоз належать D-глю- |
Найбільш поширені похідні 2-аміно-2-дезок- |
||||||||||||
коза та її емпімери: D-галактоза, D-маноза, до |
сицукрів: N-ацетилглюкозамін, N-ацетилгалак- |
||||||||||||
кетогексоз — D-фруктоза. Два цукри, які від- |
тозамін, N-ацетилмурамова кислота. |
|
|||||||||||
різняються конфігурацією у одного атома Кар- |
|
|
CH2OH |
|
|
CH2OH |
|
||||||
бону, є емпімерами, тому D-глюкоза і D-маноза |
|
|
|
|
|
||||||||
|
|
|
|
O |
HO |
|
O |
|
|||||
— емпімери відносно С-2, а D-глюкоза і D-галак- |
|
|
|
OH |
|
~OH |
|
OH |
~OH |
||||
|
|
|
|
|
|
|
|||||||
тоза — емпімери відносно С-4. |
HO |
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
NH2 |
|
|
|
|
NH2 |
|
|
|
|
|
O |
|
|
|
|
|
O |
|
|
|
|
O |
|
|
|
|
|||||||
|
|
|
|
C |
|
H |
1 |
|
|
|
|
C |
|
|
H |
|
|
C |
|
|
H |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HO |
|
|
|
H |
2 |
|
|
H |
|
|
|
OH |
H |
|
|
|
OH |
|||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HO |
|
|
|
H |
3 |
HO |
|
|
|
|
H |
HO |
|
|
|
|
|
H |
||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
H |
|
|
|
OH |
4 |
|
|
H |
|
|
|
|
OH |
HO |
|
|
|
|
|
H |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
H |
|
|
|
OH |
5 |
|
|
H |
|
|
|
|
OH |
H |
|
|
|
|
OH |
||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
CH2OH |
|
|
|
|
|
|
CH2OH |
|
|
|
CH2OH |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
CH2OH |
|
|
|
CH2OH |
|
|
CH2OH |
|||||||||||||||||
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
O |
OH |
|
|
|
O |
||||||
|
|
OH OH ~OH |
|
|
|
OH |
|
~OH |
|
|
OH |
|
|
|
~OH |
|||||||||||
|
|
|
|
|
|
|||||||||||||||||||||
OH |
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
OH |
D-Маноза D-Глюкоза D-Галактоза
D-Глюкоза (декстроза, виноградний цукор)
— найпоширеніший моносахарид; у вільному вигляді зустрічається в рослинах, переважно у плодах, крові й лімфі людини і тварин. Особливо великий вміст D-глюкози в олігосахаридах і полісахаридах.
D-Глюкозамін D-Галактозамін (2-аміно-2-глюко- (2-аміно-2-галакто- піраноза, хітозамін) піраноза, хондрозамін)
|
CH2OH |
|
|
CH2OH |
||||||||||
|
|
|
O |
HO |
|
|
O |
|||||||
|
|
OH |
|
|
~OH |
|
OH |
|
|
~OH |
||||
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
||||||||||
HO |
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH |
|
|
|
|
|
NH |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
O |
|
|
|
|
C |
|
O |
||
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
CH3 |
|
|
|
|
CH3 |
||||||
N-Ацетилглюкозамін N-Ацетилгалактозамін
|
|
|
CH2OH |
||||||
|
|
|
|
|
O |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HO |
|
|
|
|
|
OH |
|||
|
|
O |
|
NH |
|||||
|
|
|
|
|
|||||
HOOC |
|
CH |
|
|
|
|
|
||
|
C |
|
O |
||||||
|
|
|
|
|
|
||||
|
|
|
CH3 |
|
|
|
|
|
|
|
|
CH3 |
|||||||
|
|
|
|
|
|||||
N-Ацетилмурамова кислота
56
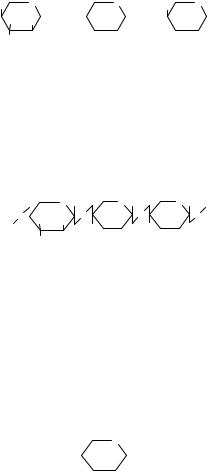
N-Aцетилглюкозамін у вигляді гомополімеру |
маніт — у водоростях. Велике значення має |
||||||||||||||||||||||||||
хітину формує скелет комах і ракоподібних; у |
ксиліт — один із найсолодших поліолів, який за- |
||||||||||||||||||||||||||
бактерій, поряд із N-ацетилмурамовою кислотою, |
стосовується у харчовій промисловості і як замін- |
||||||||||||||||||||||||||
є компонентом клітинної стінки. |
ник цукру при діабеті. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
У тваринному світі N-ацетилглюкозамін вхо- |
Відновлення фруктози в організмі до сорбіту |
||||||||||||||||||||||||||
дить до складу глікозаміногліканів сполучної |
спричинює нагромадження його в кришталику |
||||||||||||||||||||||||||
тканини (гіалуронової кислоти, хонодроїтин- |
ока при цукровому діабеті, |
що викликає ката- |
|||||||||||||||||||||||||
сульфатів, гепарину), глікопротеїнів (групи |
ракту. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
крові). |
|
|
|
CH2OH |
|
|
CH2OH |
|
|
|
CH2OH |
|
|
|
CH2OH |
||||||||||||
Залишок N-ацетилглюкозаміну звичайно |
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
H |
|
|
|
|
|
OH |
HO |
|
|
|
|
H |
H |
|
|
|
|
|
OH |
H |
|
|
|
|
|
OH |
|
знаходиться на відновлюючому кінці N-глікозид- |
HO |
|
|
|
|
H |
HO |
|
|
|
|
H |
HO |
|
|
|
|
H |
HO |
|
|
|
|
H |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
них вуглеводних ланцюгів тварин глікопро- |
H |
|
|
|
|
OH |
H |
|
|
|
|
OH |
HO |
|
|
|
H |
H |
|
|
|
OH |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
OH |
H |
|
|
|
OH |
H |
|
|
|
OH |
|
|
|
CH2OH |
|||||||||
теїнів, який утворює зв’язок вуглеводбілок. |
|
|
|
|
CH2OH |
|
|
|
CH2OH |
|
|
|
|
CH2OH |
|
|
|
|
|
|
|
||||||
N-Ацетилгалактозамін виконує аналогічну |
D-Глюцит |
D-Маніт |
D-Галактит |
|
|
|
Ксиліт |
||||||||||||||||||||
роль, але в О-глікозидних ланцюгах, у складі |
|
|
|
||||||||||||||||||||||||
(сорбіт) |
|
|
|
|
|
|
(дульцит) |
|
|
|
|
|
|
|
|||||||||||||
глікопротеїнів і гліколіпідів. N-Ацетилгалакто- |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
замін є детермінантним цукром груп крові, що |
Глюкуронові (уронові) кислоти |
|
визначає їхню специфічність. |
||
|
Нейрамінова і сіалові кислоти
Нейрамінова кислота і її похідні (сіалові кислоти) є компонентами біомембран (гангліозидів), глікопротеїнів і протеогліканів біологічних рідин, слизів, сполучної тканини.
У вільному стані нейрамінова кислота міститься у спинномозковій рідині. З хімічної точки зору вона є кетонозою (нонулоза).
|
|
COO- |
|
Піруват |
|
|
|
|
|
|
|
|
|
|
COO- |
|
Піруват |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
C |
|
|
O |
|
|
|
|
|
|
|
|
|
C |
|
|
|
O |
||||||
|
|
|
|
|
|
|
|
(залишок) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(залишок) |
|
|
CH2 |
|
|
O |
|
|
|
CH2 |
||||||||||||||||
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
H |
|
|
OH |
|
|
|
|
|
|
|
|
H |
|
|
|
OH |
|
||||||||
H2N |
|
|
|
|
H |
|
|
H3C |
|
|
C |
|
HN |
|
|
|
|
H |
|
N-Ацетил- |
|||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
HO |
|
|
|
H |
|
|
|
|
|
|
|
|
HO |
|
|
|
|
H |
|||||||
|
|
|
|
Манозамін |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
H |
|
|
|
OH |
|
|
|
|
|
|
|
H |
|
|
|
|
OH |
манозамін |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
H |
|
|
OH |
|
|
|
|
|
|
|
|
|
H |
|
|
|
OH |
|
|
||||||
|
|
CH2OH |
|
|
|
|
|
|
|
|
|
|
CH2OH |
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
D-Глюкоза |
D-Галактоза |
|
D-Маноза |
||||||||||||||||||||||||||||
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
O |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
|
H |
|
|
|
|
C |
|
|
H |
|
|
|
C |
|
|
H |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
H |
|
|
|
|
|
|
OH |
|
H |
|
|
|
|
OH |
HO |
|
|
|
|
H |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
HO |
|
|
|
|
|
H |
HO |
|
|
|
H |
HO |
|
|
|
|
H |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
H |
|
|
|
|
|
OH |
HO |
|
|
|
H |
|
H |
|
|
|
|
OH |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
H |
|
|
|
|
|
OH |
|
H |
|
|
|
OH |
|
H |
|
|
|
|
OH |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
COOH |
|
|
|
|
|
COOH |
|
|
|
COOH |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
COOH |
|
COOH |
|
|
COOH |
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
O |
HO |
|
|
|
|
|
|
O |
|
|
|
|
|
|
O |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
~OH |
|
|
|
|
~OH |
|
|
OH HO ~OH |
|||||||||||
|
|
OH |
|
|
|
|
OH |
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
HO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HO |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
||
D-Глюкуронова D-Галактуронова D-Мануронова кислота кислота кислота
Нейрамінова |
N-Ацетилнейрамінова |
Уронові кислоти є компонентами рослинних і |
||||||||||||||||||
кислота |
(сіалова) кислота |
|||||||||||||||||||
бактеріальних полісахаридів. Пектинові речови- |
||||||||||||||||||||
(відкрита форма) |
(відкрита форма) |
|||||||||||||||||||
ни, що містяться в плодах і овочах, являють со- |
||||||||||||||||||||
|
|
|||||||||||||||||||
Назвою «сіалові кислоти» позначається гру- |
бою продукти поліконденсації D-галактуронової |
|||||||||||||||||||
па різних N- і О-ацильованих похідних нейрамі- |
кислоти — полігалактуронової (пектинової) кис- |
|||||||||||||||||||
нової кислоти. Знаходячись на відновлюючому |
лоти. |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
кінці олігосахаридних ланцюгів (гліколіпідів і |
|
COOH |
|
|
|
|
COOH |
|
|
COOH |
|
|||||||||
глікопротеїнів), сіалові кислоти додають поліме- |
|
|
O |
|
O |
|
O |
|
O |
|
O |
|
||||||||
|
|
|
|
|
||||||||||||||||
ру негативного заряду. Наявність сіалових кис- |
O |
OH |
|
OH |
|
|
|
OH |
|
O |
||||||||||
лот на кінцях олігосахаридних ланцюгів тварин |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
OH |
|
|
|
|
OH |
|
|
OH |
|
|||||||||
глікопротеїнів забезпечує можливість циркуляції |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
Полігалактуронова (пектинова) кислота |
||||||||||||||||||||
останніх у кровотоку, запобігаючи захопленню |
||||||||||||||||||||
їх клітинами печінки. |
|
Деякі пектинові речовини справляють проти- |
||||||||||||||||||
Сіалові кислоти багато в чому визначають |
||||||||||||||||||||
виразкову дію і є основою низки препаратів (на- |
||||||||||||||||||||
властивості клітинної поверхні. Зміна вмісту сіа- |
||||||||||||||||||||
лових кислот на клітинній поверхні супроводжує |
приклад плантаглюцид із подорожника). |
|||||||||||||||||||
такі процеси, як диференціація клітин і злоякісне |
Утворення глікозидів глюкуронової кислоти |
|||||||||||||||||||
— глюкуронидів — є окремим випадком проце- |
||||||||||||||||||||
переродження. Наявністю надлишкової кількості |
||||||||||||||||||||
сіалових кислот на поверхні пояснюють багато |
су кон’югації, тобто взаємодії лікарських препа- |
|||||||||||||||||||
властивостей пухлинних клітин. |
ратів або їх метаболітів із біогенними речовина- |
|||||||||||||||||||
ми. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
Альдити (поліоли) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
D-Глюкуронова і α -ідуронова кислоти є струк- |
||||||||||||||||||||
При відновленні карбонільної групи моноса- |
турними одиницями гепарину. |
|
|
|
|
|||||||||||||||
харидів утворюються багатоатомні спирти (полі- |
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
оли), які називаються альдитами. |
|
|
|
|
|
|
|
|
COOH |
~OH |
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
Ці альдегіди добре розчинні у воді, мають со- |
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
||||||
|
|
|
|
|
OH |
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
лодкий смак і часто використовуються як замін- |
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|||
ники цукру. Сорбіт виявлений у горобині, |
|
|
α -Ідуронова кислота |
|
||||||||||||||||
57
Уронові кислоти виконують в організмі важливу функцію: утворюють з лікарськими речовинами, їх метаболітами в печінці водорозчинні глікозиди, які виводяться з сечею.
Альдонові кислоти
Альдонові і уронові кислоти мають тенденцію до внутрішньомолекулярної етерифікації з утворенням 5- і 6-членнихлактонів (циклічних ефірів).
|
|
|
CH2OH |
|
|
|
CH2OH |
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
H |
|
C |
|
OH |
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
O |
O + |
|
|
O |
|
|
|
|
O |
- 2H |
|
|||||
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
HO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
OH |
|
|
|
|
OH |
OH |
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
D-Глюко- |
|
|
|
|
L-Аскорбінова |
|||||||||||||||||||
δ -лактон |
кислота (вітамін С) |
|||||||||||||||||||||||
|
|
|
|
|
|
CH2OH |
|
|
|
|
|
COOH |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
H |
|
C |
|
|
OH |
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
O |
|
|
C |
||||||||||||||||
|
- 2H |
|
|
|
O |
+ H2O |
|
|
||||||||||||||||
|
|
|
|
O |
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
C |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
OH |
|
|
|
|
|
|
|
O |
O |
|
|
HO |
|
|
|
H |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
CH2OH |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
L-Дегідроаскор- 2,3-Дикето-L-гуло- |
|||||||||||||||||||||||
|
бінова кислота |
|
|
нова кислота |
||||||||||||||||||||
Прикладом альдонових кислот є глюконова кислота, яка у вигляді фосфорного ефіру утворюється в організмі при окисненні глюкози (пентозофосфатний шлях). У медицині використовується кальцієва сіль глюконової кислоти (глю-
конат кальцію).
Вітамін С є γ -лактоном α -дикетогулонової кислоти (альдонової кислоти).
Глікозиди
Глікозиди — сполуки, які є продуктами конденсації моносахаридів (або моносахаридних залишків у складі складного цукру) зі спиртами чи фенолами.
Глікозиди складаються з двох частин: аглікону (невуглеводний фрагмент) і глікону (вуглеводна частина). Вуглеводна частина найчастіше представлена D-глюкозою, рідше — D- і α -га- лактозою, D-манозою.
Особливо широко глікозиди представлені в рослинах: це пігменти квітів, ароматичні речовини, багато природних барвників. Вітамін Р (рутин) є О-глікозидом. Вуглеводна частина рутину — це дисахарид, що складається із залишків D-глюкози та L-рамнози; невуглеводна (аглікон) — похідне флавону кверцетин:
|
H |
|
O H |
HO |
|
|
|
|
|
|
||||||
OH |
|
|
HO |
|
O |
|
OH |
|
|
|||||||
CH |
3 |
|
|
Кверцетин |
||||||||||||
H |
H |
H |
O |
CH2 |
|
|
|
|
||||||||
|
|
|
|
|
|
O |
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|||||||
|
OH |
|
OH H |
|
O |
O |
OH |
|
|
|||||||
|
|
|
|
|
|
|||||||||||
|
|
OH H |
|
|
|
|
|
|
||||||||
L-РамнозаOH |
|
|
|
H |
|
|
|
|
|
|||||||
H OH |
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
Глюкоза |
|
|
|
|
|
|
|||
Вітамін Р (рутин)
Амігдалін — сполука, що міститься в кісточках плодів (персик, абрикос, вишня, мигдаль).
Вуглеводна частина побудована з двох залишків β -D-глюкози. Аглікон складається із залишків бензенового альдегіду та синільної кислоти:
|
CH2OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
O |
|
O |
|
|
CH2 |
O |
|
|
|
C6H5 |
|||||
|
OH |
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
HO |
|
|
|
|
|
|
|
|
|
|
O |
|
CH |
||||
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
||
|
|
OH OH |
|
|
|
|
|
|
C |
|
N |
||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
Амігдалін
Серцеві глікозиди, що використовуються для стимуляції діяльності міокарда при серцевій недостатності, виділяють із різних видів наперстянки, конвалії, горицвіту.
Глікозиди зустрічаються й у тваринному світі. Найбільш відомими і розповсюдженими глікозидами є гліколіпіди — гангліозиди, що входять до складу нуклеїнових кислот і більшості коферментів.
Реакційна здатність моносахаридів
Моносахариди вступають у більшість реакцій, які характерні для спиртів і оксосполук.
Біологічна дія моносахаридів зумовлена їх хімічною будовою. Структура цукрів визначає механізм реакцій, які лежать в основі біохімічних перетворень. Так, утворення циклічних структур спричинило появу найбільш реакційноздатного напівацетального гідроксилу.
Завдяки високій реакційній здатності напівацетального гідроксилу відбувається утворення важливих метаболітів. Моносахариди при взаємодії зі спиртами в безводному середовищі за наявності кислотного каталізатора утворюють повні ацеталі. Зв’язок між С=1 і ОR називають глікозидним. Незалежно від аномерної форми вихідного моносахариду в результаті утворюється суміш α - і β -ізомерів. Метод синтезу глікозидів запропонував Е. Фішер (1893).
CH2OH |
|
|
|
|
CH2OH |
|
||||
|
O |
|
HCI (газ) |
|
O |
|
||||
|
|
|
|
|
|
|
|
|||
OH OH |
+ CH3OH |
|
|
|
OH OH |
OCH3 + H2O |
||||
|
|
|
||||||||
|
|
|
||||||||
OH |
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
OH |
|
||
α -D-Глюко- |
|
|
|
Метил-D-глюкопіра- |
||||||
піраноза |
|
|
|
|
нозид (α - і β -ізомери) |
|||||
Розчини глікозидів не мутаротують, оскільки таутомерні переходи неможливі.
Глікозиди, як і всі ацеталі, гідролізуються в кислому середовищі, але стійкі до дії розведених лугів.
Алкірування моносахаридів — утворення простих ефірів:
|
CH2OH |
|
|
|
|
|
CH2OH |
||||||
|
|
O |
|
BaO |
|
|
|
O |
|||||
|
|
|
|
+ 5CH3I |
|
|
|
|
OCH3+ 5Hl |
||||
|
OH |
|
|
|
|
|
|
|
|
||||
OH |
OH |
H3C |
|
O |
O |
|
CH3 |
||||||
|
|
|
|
|
|
|
|
|
|||||
|
|
OH |
|
|
|
|
|
|
|
|
OCH3 |
||
Простий ефір
58