Материал: Біологічна та біоорганічна хімія_Мардашко О.О._ изд. 2008-342 с._ОНМедУ-2012
нокислота) та аміногрупи другої амінокислоти (друга амінокислота) з утворенням пептидного зв’язку:
O H
C N
Наприклад, при взаємодії гліцину та α -ала- ніну утворюється дипептид гліцил-аланін, який має пептидний зв’язок:
O O
H2N CH C OH + H2N CH C OH 
H |
CH3 |
Гліцин (перша α -Аланін (друга амінокислота) амінокислота)
O H O
 H2N CH C N CH C OH H CH3
H2N CH C N CH C OH H CH3
Гліцил-аланін (дипептид)
Пептид складається з двох або більше амінокислотних залишків, з’єднаних пептидними зв’язками.
Пептиди, що мають більше 10 амінокислотних залишків, називають поліпептидами.
Структуру пептиду прийнято позначати так, щоб N-кінцевий залишок (який містить вільну аміногрупу) розміщувався ліворуч, а С-кінцевий залишок (з вільною карбоксильною групою) — праворуч.
Лінійна послідовність амінокислотних залишків у поліпептидному ланцюзі називається
первинною структурою пептиду. При найме-
нуванні пептиду його розглядають як похідне С-кінцевого амінокислотного залишку. Якщо первинна структура пептиду відома, то трилітерні позначення амінокислотних залишків з’єднують рисками:
Glu—Ala—Lys—Gly—Tyr—Ala
Більшість природних поліпептидних ланцюгів містить від 50 до 2000 амінокислотних залишків. Молекулярна вага більшості поліпептидних ланцюгів — від 500 до 220 000. Вагу білків позначають у дальтонах (Да). Білки з молекулярною вагою 50 000 мають вагу 50 000 дальтон, або
50кДа (кілодальтон).
Умовною різницею між поліпептидами та
білками вважається молекулярна вага й здатність до діалізу. Поліпептиди мають молекулярну вагу до 5000 Да і здатні до діалізу, а білки — більше 5000 Да і не здатні до діалізу.
Рівні структури молекул білка
Розрізняють чотири рівні структури (структурної організації) білкової молекули.
І. Первинна структура молекули білка — це послідовне розміщення амінокислотних залишків у поліпептидному ланцюзі. Зв’язок, стабілізуючий первинну структуру, — це пептидний зв’я- зок.
Жорсткість пептидного зв’язку
У структурних формулах пептидів зв’язок між атомами Карбону карбоксильної групи й атомами Нітрогену показується як одинарний, але він має характер часткового подвійного зв’язку. Вільне обертання навколо нього неможливе, і всі чотири атоми лежать в одній площині.
O H |
|
|
|
|
|
|
|
O- |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
N |
|
|
|
|
|
|
|
C |
|
N |
|
||||
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H+ |
||
Обертання ж навколо інших зв’язків, навпаки, досить вільне (рентгеноструктурні дослідження пептидів свідчать про жорсткість і плоску конфігурацію пептидних груп).
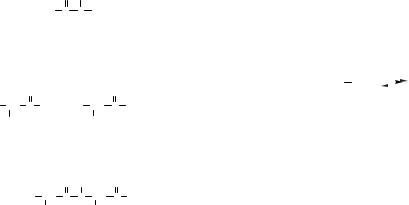
ІІ. Вторинна структура білка — просторове розміщення, тобто конформація сусідніх амінокислотних залишків поліпептидного ланцюга у просторі.
До вторинної структури належать α -спіраль
іβ -структура («складчастий лист»), β -згин (β -bend), нерегулярна структура (неупорядкований клубок), надвторинна структура.
α-Спіраль — найпростіша форма поліпептидного ланцюга, що містить жорсткі поліпептидні зв’язки (при тому, що навколо решти зв’язків свобода обертання зберігається).
У цій структурі поліпептидний остов утворює
витки навколо довгої осі молекули. Закручування поліпептидного ланцюга в α -
спіралі відбувається за годинниковою стрілкою, що зумовлено α -амінокислотними залишками. На кожний виток спіралі припадає 3,6 амінокислотного залишку, крок спіралі (відстань на протязі осі) = 0,54 нм, на один амінокислотний залишок — 0,15 нм. Кут підйому спіралі = 26°; через кожні 5 витків спіралі (18 амінокислотних за-
лишки) структурна конформація поліпептидного ланцюга повторюється. Стабільність α -спіралі забезпечується переважно великою кількістю водневих зв’язків.
1.α -Спіраль стабілізується водневими зв’язками між атомами Гідрогену, зв’язками з атомами Нітрогену пептидної групи та карбонільним Оксигеном, що відстає від даного на протязі ланцюга на чотири позиції.
2.В утворенні водневого зв’язку беруть
участь усі пептидні групи. Це забезпечує максимальну стабільність α -спіралі.
3.В утворення водневих зв’язків залучені всі
атоми Нітрогену й Оксигену пептидних груп, що значною мірою знижує гідрофільність α -спі- ралі та збільшує її гідрофобність.
4.α -Спіраль утворюється самостійно та є найстійкішою конформацією поліпептидного ланцюга, що відповідає мінімуму вільної енергії.
5.У білках, побудованих з L-амінокислот, права спіраль набагато стабільніша за ліву.
Деякі амінокислоти запобігають скручуванню ланцюга в α -спіраль, в місці їх розміщення безперервність α -спіралі порушується. До таких амінокислот належать пролін (у ньому атом Нітрогену служить частиною жорсткого кільця,
іобертання навколо пептидного зв’язку стає не-
44
можливим). Крім того, амінокислоти із зарядженими або об’ємними R-групами електростатично або механічно запобігають формуванню α -спіралі.
Отже, ми маємо чотири типи запобігань просторовій конформації поліпептидного ланцюга:
1. Жорсткість і транс-конфігурація пептидних зв’язків.
2. Електростатичне відштовхування (або при- |
|
|
|
тягнення) амінокислотних залишків, які містять |
|
|
|
заряджені R-групи. |
|
|
|
3. Близьке розміщення в ланцюгу громіздких |
|
|
|
R-груп. |
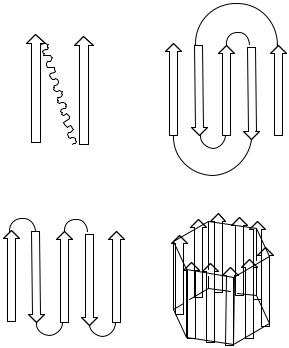
β -α -β -ділянки |
грецький ключ |
|
4. Наявність у поліпептидному ланцюзі за- |
|
|
|
лишків проліну. |
|
|
|
Для кожного білка характерний певний тип |
|
|
|
спіралізації його поліпептидного ланцюга, |
|
|
|
α -спіральний тип структури мають глобулярні |
|
|
|
білки. |
|
|
|
β -Структура — другий тип структури, вияв- |
|
|
|
лений у ряді фібрилярних білків. У цьому випад- |
|
|
|
ку два або більше лінійних поліпептидних лан- |
|
|
|
цюги зв’язуються між собою водневими зв’язка- |
|
|
|
ми, утворюючи структуру типу складчастого ли- |
β -звивина |
β -бочонок |
|
ста, тобто водневі зв’язки міжланцюгові, але не |
|||
внутрішньоланцюгові, як у α -структурі. У ре- |
Рис. 2.5. Основні типи вторинних структур |
||
зультаті цього радикали амінокислот розміщені |
|||
над і під площиною складчастого шару, стабіль- |
|
|
|
ність вторинної структури в основному забезпе- |
β -структура, послідовності, що не повторюють- |
||
чується водневими зв’язками, але певне значен- |
|||
ня в цьому мають і ковалентні, пептидні та ди- |
ся). Вони формують серцевину, пов’язану з ділян- |
||
сульфідні зв’язки. |
ками петель (наприклад β |
-вигин) на зовнішній |
|
стороні білка. Основні типи вторинних структур |
|||
Існує різниця між α - та β -кератинами (α -спі- |
|||
раль і β -складчастий шар). У тих випадках, коли |
(motifs — напрямки) представлені на рис. 2.5. |
||
сусідні поліпептидні ланцюги складчастого |
ІІІ. Третинна структура |
|
|
Третинна структура — це спосіб укладання |
|||
β -шару йдуть у протилежних напрямках (від N- |
|||
до С-кінця або від С- до N-кінця), то структуру |
поліпептидного ланцюга в певному об’ємі (інша |
||
називають антипаралельним складчастим β -ша- |
назва — конформація білкової субодиниці в ціло- |
||
ром. Якщо сусідні ланцюги йдуть в одному на- |
му; тримірна структура білка). |
||
прямку, структуру α -кератину називають пара- |
Первинна структура поліпептидного ланцю- |
||
га визначає її третинну структуру (термін «тре- |
|||
лельною. |
тинний» означає укладання доменів — основної |
||
У формуванні таких структур беруть участь |
|||
від двох до п’яти сусідніх поліпептидних лан- |
структурної та функціональної одиниці — і ос- |
||
цюгів: β -структура може утворюватися тільки за |
таточне укладання доменів поліпептиду). |
||
наявності в складі поліпептиду відповідних амі- |
Домен — основна функціональна та просто- |
||
рова структурна одиниця поліпептиду. Поліпеп- |
|||
нокислот, розміщених у певній послідовності; R- |
|||
групи амінокислотних залишків повинні мати |
тидний ланцюг, який має значно більше 200 амі- |
||
порівняно невеликі розміри (гліцин, α -аланін). |
нокислот за довжиною, складається з двох або |
||
α -Вигин (від англ. β -bends, або reverse, turns |
більше доменів. Ядро домену побудоване з ком- |
||
— зворотний поворот) у поліпептидному лан- |
бінації супервторинних структурних елементів |
||
цюзі сприяє утворенню компактної, глобулярної |
(мотивів). Укладання поліпептидного ланцюга |
||
форми білка. β -Вигини звичайно утворюються |
в домен звичайно здійснюються незалежно від |
||
на початку білкової молекули. Назва «β -вигин» |
укладань (фолдингу) інших доменів. Тому кож- |
||
пов’язана з антипаралельними β -структурами, |
ний домен — маленький компактний глобуляр- |
||
що слідують одна за одною. Ця композиція зви- |
ний білок, що структурно не залежить від інших |
||
чайно складається з 4 амінокислот, одна з яких |
доменів у поліпептидному ланцюзі. |
||
(пролін) — причина «петлі» (вигину). У поліпеп- |
Взаємодії, що стабілізують |
||
тидному ланцюзі для β -вигину також необхід- |
|||
ний гліцин. Структура β -вигину стабілізована |
третинну структуру |
||
за рахунок водневих та іонних зв’язків. |
Третинна структура кожного поліпептиду |
||
Супервторинні структури |
визначається його амінокислотною послідовніс- |
||
тю. Взаємодії між амінокислотами ланцюга — |
|||
|
|||
Глобулярні білки скручуються за допомогою |
причина укладання поліпептидного ланцюга з |
||
комбінації структурних елементів (α -спіраль, |
утворенням компактної структури. |
||
45

Стабільність тривимірної структури забезпечують усі можливі типи зв’язків (дисульфідні, водневі, гідрофобні, іонні). Рушійною силою виникнення тривимірної структури є взаємодія радикалів амінокислот із молекулами води. Гідрофобні радикали амінокислот ніби вдаються всередину білкової молекули. Гідрофільні групи виявляються орієнтованими у бік води. В якийсь момент виникає термодинамічно найвигідніша конформація в ланцюзі, яка стабілізується. У такій формі молекула білка має мінімальну вільну енергію. Отже, в утворенні певної тривимірної структури важливу роль відіграють гідрофобні зв’язки і жорсткість пептидного зв’язку.
Гідрофобний зв’язок
Молекула білка містить гідрофільні групи:
C O,  NH, SH , COOH , NH2, OH ,
NH, SH , COOH , NH2, OH ,
а також гідрофобні: метильні (–СН3), етильні (–СН2СН3), фенільні (–С5Н6) та ін. У воді гідрофобні групи переміщуються до внутрішньої частини молекули білка, спричинюючи цим згортання поліпептидного ланцюга.
Отже, гідрофобний зв’язок утворюється в результаті зближення гідрофобних радикалів амінокислот (рис. 2.6).
H O
N CH C
CH CH3 Ізолейцин
CH2
CH3
 H3C CH3
H3C CH3
CH
CH2 Лейцин
C CH N
O H
Рис. 2.6. Гідрофобна взаємодія між амінокислотами з неполярними радикалами
Цей вид зв’язку має важливе значення у формуванні певної третинної структури білкової молекули.
Іонний зв’язок (сольовий, електровалентний)
Молекули білка мають залишки моноамінодикарбонових кислот (аспарагінова та глутамінова), у яких є вільні карбоксильні групи у вигляді аніона –СОО–, та діаміномонокарбонових кислот (аргінін і лізин) із вільними аміногрупами у вигляді катіона –NН3+ (рис. 2.7).
Аніони та катіони, як протилежно заряджені, притягаються, утворюючи іонні зв’язки. Вони можуть з’єднувати витки одного або різних ланцюгів, тобто утворювати внутрішньоланцюгові та міжланцюгові зв’язки.
Водневі зв’язки
Виникають у результаті електростатичного притягання між позитивно зарядженим атомом
Глутамат |
|
|
Аспартат |
|||||||||||||||||||
|
H |
|
|
O H |
|
|
|
|
O |
|||||||||||||
|
N CH C |
|
|
N CH C |
||||||||||||||||||
|
|
|
||||||||||||||||||||
|
|
|
|
|
CH2 |
|
|
CH2 |
||||||||||||||
|
|
|
|
|
CH2 |
|
|
C |
||||||||||||||
|
|
|
|
|
C |
O |
|
O- |
||||||||||||||
|
|
O |
|
O- |
|
|
|
|
|
Іонний зв’язок |
||||||||||||
Водневий зв’язок |
H |
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
+ |
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH3 |
||||||||
|
|
|
|
|
O |
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(CH2)4 |
|||||||
|
|
|
|
|
CH |
|
|
|
||||||||||||||
|
|
N |
|
|
2 |
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
CH |
|
C |
|
|
CH |
|
C |
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
O |
|
H |
|
|
|
|
O |
|||||||||
Серин Лізин
Рис. 2.7. Взаємодія амінокислот за допомогою водневих та іонних зв’язків
Гідрогену, ковалентно зв’язаним з атомом Нітрогену або Оксигену, та негативно зарядженим атомом Оксигену. Позитивно заряджений атом Гідрогену входить в аміногрупу пептидного зв’язку білкової молекули ( N–Н), аміногрупу (–NН2) діамінокарбонових амінокислот і гідроксильну групу (–ОН) залишків амінокислот серину, треоніну та ін. Негативно заряджений атом Оксигену входить до складу карбонільної групи пептидного зв’язку ( С=О), гідроксильної групи карбоксилу (–СООН) (див. рис. 2.7).
Дисульфідний зв’язок (цистиновий)
Він утворюється в результаті відщеплення двох атомів Гідрогену від сульфгідрильних груп двох залишків амінокислоти цистеїну (рис. 2.8):
Цистеїн
H |
|
|
O |
|
H |
O |
|||
|
|
|
|
|
|
|
|
N |
CH C |
N |
|
CH |
|
C |
|
||||
|
|
|
|||||||
|
|
CH2 |
Окиснення |
CH2 |
Дисульфідний |
||
|
|
||||||
|
SH |
S |
зв’язок |
||||
|
|
|
|
||||
|
SH |
|
|
|
S |
|
|
|
CH2 |
|
|
|
CH2 |
|
|
C CH N |
|
|
|
C CH N |
|||
O |
|
H |
|
|
|
O |
H |
Цистеїн Цистин
Рис. 2.8. Дисульфідний зв’язок
Дисульфідні зв’язки можуть бути як внутріш- ньо-, так і міжланцюговими.
Внутрішньоланцюгові зв’язки утворюються в межах одного поліпептидного ланцюга, що спричинює утворення та закріплення певних згинів і спіралей у поліпептидному ланцюгу.
Міжланцюгові дисульфідні зв’язки утворюються між залишками цистеїну двох поліпептидних ланцюгів, тобто з’єднуються між собою різні поліпептидні ланцюги.
Третинну структуру називають ще конформацією, оскільки будь-який вплив (фізичний, хімічний), що призводить до порушення цієї конформації молекули, супроводжується частковою або повною втратою білком його біологічних властивостей.
46
Різновидами третинної структури білкових молекул є глобулярна та фібрилярна структури. У глобулярній структурі переважають α -спіралі, а в фібрилярній — β -структури.
IV. Четвертинна структура
Четвертинна структура білкової молекули — це спосіб укладання та об’єднання кількох білкових частинок із третинною структурою (субодиниць) у макромолекулу білка.
Субодиниці в четвертинній структурі зв’язані між собою переважно водневими зв’язками. При додаванні до розчину гемоглобіну сечовини або солей його молекула в результаті розриву водневих зв’язків зворотно дисоціює (розпадається) на два α - та два β -ланцюги. Після видалення солей або сечовини автоматично відбувається асоціація (з’єднання) чотирьох субодиниць у початкову молекулу гемоглобіну.
Фермент фосфорилаза складається з двох ідентичних субодиниць, кожна з яких має по два поліпептидних ланцюги, тобто молекула фосфорилази є тетрамером. Окремі субодиниці цього ферменту не мають ферментативної активності.
Наявність усіх чотирьох рівнів структурної організації необов’язкова для кожного білка. Обов’язковою структурою для всіх білків є первинна структура. Багато біологічно активних білків (наприклад ферменти) мають третинну структуру, оскільки саме на цьому рівні структурної організації формуються активні центри, що характеризуються специфічністю дії ферментів.
Фізико-хімічні властивості білків
1. Молекулярна маса білків. Молекули білків мають певну форму, розміри й молекулярну масу. Відомі дві основні форми білкових молекул:
—глобулярні білки (куляста форма);
—фібрилярні білки (сильно видовжена фор-
ма).
Форма білкової молекули змінюється під впливом таких факторів: рН, природа розчинника, концентрація розчину, температура.
Розміри білкових молекул визначаються в трьох вимірах.
Молекулярна маса білків вимірюється в дальтонах (Да).
1 Да відповідає уніфікованій одиниці відносної атомної маси (1 Да = 1 а. о. м. = 1,66·10–27 кг).
Молекулярну масу білків визначають різними методами:
—осмометричним;
—електрофоретичним;
—ультрафільтраційним;
—віскозиметричним та ін.
Використання ультрацентрифуг дає змогу розділяти частинки з різною молекулярною масою за допомогою осадження (седиментації) білків.
Швидкість осадження молекул залежить від розмірів, форми та маси частинок і характеризується коефіцієнтом седиментації (S), який збільшується зі зростанням молекулярної маси.
Седиментаційний аналіз використовують для визначення молекулярної маси білків за рівнянням Сведберга:
SRT , М =—————
D(1 – vρ)
де М — молекулярна маса білка; R — газова стала;
Т — абсолютна температура, К; S — коефіцієнт седиментації;
ρ— густина розчинника;
v — парціальний питомий об’єм білка; D — коефіцієнт дифузії.
Визначати молекулярну масу білків за осмотичним тиском можна для гомогенних білків у стані ізоелектричної точки (оскільки концентрація електролітів у розчині впливає на осмотичний тиск), тому що молекулярна маса білка тим вище, чим нижче осмотичний тиск його розчину:
gRT , PV = ———
M
де Р — осмотичний тиск; V — об’єм розчину білка; g — маса білка.
Метод гель-фільтрації дозволяє оцінити гомогенність білка за розмірами, а також розділити білки з різними молекулярнами масами.
При гель-електрофорезі розчину білків у присутності детергента (додецилсульфату натрію) швидкість міграції білків Rf пропорційна логарифму молекулярної маси білка.
Електрофорез — це рух заряджених частинок дисперсної фази у полі постійного електричного струму до одного з електродів. Електрофоретична рухливість частинок залежить від заряду молекул, в’язкості середовища, розмірів молекул, їх молекулярної маси. Тому методи електрофорезу застосовують для визначення молекулярної маси білків.
2. Кислотно-основні властивості білків
Розміщені на кінцях поліпептидного ланцюга вільна аміногрупа та карбоксильна група незначно впливають на ці властивості. Завдяки наявності вільних NН2-груп залишків діамінокарбонових кислот і вільних СООН-груп залишків моноамінодикарбонових кислот білки, як і амінокислоти, виявляють усі властивості кислот та основ, тобто мають амфотерні властивості. Заряд білкової молекули виникає при іонізації функціональних груп залишків амінокислот.
Залежно від рН середовища та відношення кислих і основних амінокислот у структурі білка, білки в розчині мають позитивний або негативний заряд. У тих випадках, коли (+) та (–) електричні заряди білкової молекули врівноважуються і заряд її дорівнює нулю (як у цвітер-іоні), білок знаходиться в ізоелектричному стані. Те значення рН розчину, при якому білок знаходиться в ізоелектричному стані, називається ізоелектрич-
47
ною точкою білка (рІ). Для більшості білків ізо- |
ня використовують на практиці для виділення |
||||||||||
електрична точка знаходиться в межах рН=5,5– |
нативних білків, його проводять високими кон- |
||||||||||
7,0, що свідчить про часткове переважання в |
центраціями солей електролітів для зняття заря- |
||||||||||
складі білків кислих амінокислот. Але такий |
ду частинки (висолювання) та спиртом і ацето- |
||||||||||
білок, як пепсин, має рН=1,0. В ізоелектричній |
ном, для руйнування гідратної оболонки за схе- |
||||||||||
точці білки малостійкі, легко випадають в осад, |
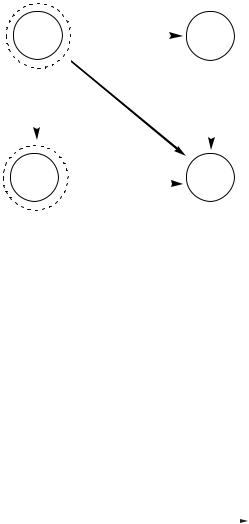
мою Кройта (рис. 2.9). Послідовність цих опе- |
||||||||||
не переміщуються в електричному полі. Більшість |
рацій суттєва для процесу осадження: |
|
|
|
|||||||
природних білків є кислими, вони містять знач- |
|
|
|
|
|
|
|
|
|
|
|
ну кількість дикарбонових кислот. |
|
|
|
|
|
|
|
|
|
|
|
3. Гідрофільність білків |
|
|
|
|
|
|
спирт |
|
|
|
|
Розрізняють два основних фактори стабілі- |
|
|
+ |
|
|
– |
|||||
|
|
|
|
|
|
||||||
|
|
|
|
|
|
||||||
зації білків у розчині: наявність заряду та гідрат- |
|
|
|
|
|
|
|
|
|
|
|
ної оболонки. У молекулі білка є гідрофільні гру- |
|
|
|
|
|
|
|
|
|
|
|
пи –СООН, –NН2, –ОН (здатні до дисоціації), |
|
електроліт |
|
|
|
|
електроліт + |
|
електроліт |
||
|
|
|
|
|
|
||||||
які притягують молекули води. У результаті цьо- |
|
|
|
|
|
спирт |
|
||||
|
|
|
|
|
|
|
|
|
|||
го навколо молекули білка утворюється гідрат- |
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
на оболонка, яка є другим фактором, що забез- |
|
|
|
|
|
|
|
|
|
|
|
печує стійкість розчинів білка. В ізоелектричній |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
точці розчинність білків мінімальна. Найменшу |
|
|
|
|
|
|
|
|
|
|
|
гідратну оболонку білки мають в ізоелектрично- |
|
|
|
|
|
|
|
|
|
|
|
му стані. Необхідно відмітити, що гідратна обо- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
лонка, яка оточує білкову молекулу, може бути |
|
|
|
|
|
|
спирт |
|
|
|
|
не суцільною. Наприклад, білки-ферменти мають |
|
|
|
|
|
|
|
|
|
|
|
невеликі гідрофобні (негідратовані) ділянки для |
|
|
|
|
|
|
|
|
|
|
|
зв’язування білка з іншими молекулами (суб- |
Рис. 2.9. Схема Кройта — осадження гідрофільних |
||||||||||
стратами, коферментами). Для осадження білків |
|
|
|
|
|
|
частинок |
|
|
|
|
у розчині необхідно змінити електричний заряд |
Ступінь осадження білків солями лужних і |
||||||||||
їхніх частинок і зруйнувати гідратну оболон- |
|||||||||||
ку: |
лужно-земельних металів залежить від радіуса та |
||||||||||
— рН: зсув рН у будь-який бік від рІ (ізоелек- |
заряду іонів, їх здатності до гідратації: чим |
||||||||||
трична точка) спричинює виникнення заряду, |
більше потрібно води для гідратації іона, тим мен- |
||||||||||
що підвищує розчинність білка; |
ше води залишається для розчинення і тим кра- |
||||||||||
— температура: для більшості білків роз- |
ще відбувається висолювання. За осаджуваль- |
||||||||||
чинність підвищується з підвищенням температу- |
ною здатністю іони розміщені в ряди, які назива- |
||||||||||
ри до межі, що викликає денатурацію білка. Ра- |
ють ліотропними рядами катіонів і аніонів (ряда- |
||||||||||
зом із тим, існують білки, розчинність яких зни- |
ми Гофмейстера): |
|
|
|
|||||||
жується з підвищенням температури (гемоглобін, |
Li+ > Na+ > K+ > Rb+ > Cs+ > Mg2+ > Ca2+ > Ba2+ |
||||||||||
альдолаза); |
|
|
|
|
|
|
|
|
|
|
|
— іонна сила розчину залежить від концент- |
SO42–> F > [цитрат]3– > [ацетат]– > Cl– > NO3– > |
||||||||||
рації та заряду розчинних у ньому солей. Нейт- |
|||||||||||
ральні солі у низьких концентраціях (іонна сила |
|
|
|
|
Br– > I– > CNS– |
|
|
|
|||
розчину невисока) підвищують розчинність |
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
білків за рахунок взаємодії іонів із полярними |
|
ступінь гідратації іонів зменшується |
|||||||||
групами білка. При цьому руйнуються іонні |
|
|
|
|
|
|
|
|
|
|
|
|
осаджувальна дія іонів зменшується |
||||||||||
зв’язки між окремими макромолекулами і роз- |
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
чинність білків підвищується. При високій кон- |
|
|
|
|
|
|
|
|
|
|
|
центрації іонів останні взаємодіють із гідратною |
Коагуляція (від лат. coagulation — згортання, |
||||||||||
оболонкою білкової молекули, руйнують її і білки |
затвердіння) — поділ колоїдного розчину на дві |
||||||||||
випадають в осад (осаджуються). |
фази. |
|
|
|
|
|
|
|
|
|
|
4. Набухання білків — процес проникнення |
Коагулювальна дія електролітів підпорядко- |
||||||||||
молекул розчинника між молекулами високомо- |
вується правилу Шульце — Гарді: коагуляцію |
||||||||||
лекулярних сполук, що супроводжується знач- |
спричинюють іони із зарядом, протилежним за- |
||||||||||
ним збільшенням об’єму та маси полімеру. На |
ряду гранули, і коагулювальна можливість тим |
||||||||||
ступінь набухання впливають такі фактори: |
вища, чим вищий заряд коагулюючого іона. |
||||||||||
температура, тиск, рН середовища, природа роз- |
При введенні в організм якого-небудь електролі- |
||||||||||
чинника. Зміна рН у кислий або лужний бік від |
ту слід враховувати не тільки його концентра- |
||||||||||
ізоелектричної точки приводить до зростання сту- |
цію, а й заряд іона. Так, фізіологічний розчин |
||||||||||
пеня набухання. рН знижується при укусі люди- |
хлориду натрію (NaCl) не можна замінити ізото- |
||||||||||
ни бджолами, комахами, тому тканина набря- |
нічним розчином MgCl2, оскільки Mg2+ має висо- |
||||||||||
кає за рахунок рідини сусідніх ділянок. |
ку коагулюючу дію. |
|
|
|
|||||||
5. Осадження білків (перехід білків із розчину |
6. Денатурація. При нагріванні розчинів |
||||||||||
в осад). Розрізняють оборотне та необоротне (де- |
білків вище 50–60 °С, при додаванні до них со- |
||||||||||
натурація) осадження білків. Оборотне осаджен- |
лей важких металів (Cu, Pb, Ag, Hg та ін.), силь- |
||||||||||
48