Материал: Біологічна та біоорганічна хімія_Мардашко О.О._ изд. 2008-342 с._ОНМедУ-2012

дизації. Тому такі цикли утворюються порівняно легко, додаткового напруження не виникає, не змінюється загальна геометрія молекул. Залежно від кількості атомів, що входять до циклу, їх підрозділяють на три-, чотири-, п’ятита шестичленні з одним, двома чи більше гетероатомами. Трита чотиричленні гетероцикли нестійкі. Тому клас гетероциклічних сполук утворюють, головним чином, п’ятита шестичленні гетероцикли, які здебільшого не змінюються у разі хімічних перетворень. Широко розповсюджені гетероциклічні сполуки, в яких гетероцикл конденсований з бензеновим ядром або іншим гетероциклом.
П’ятичленні гетероциклічні сполуки
З одним гетероатомом:
O S N H
Фуран Тіофен Пірол
З двома гетероатомами (азоли):
N N N
N N N O S H H
Піразол Імідазол Оксазол Тіазол
Шестичленні гетероциклічні сполуки
З одним гетероатомом:
5 |
4 |
3 |
5 |
4 |
3 |
5 |
4 |
3 |
6 |
1 |
2 |
6 |
1 |
2 |
6 |
1 |
2 |
|
N |
|
|
O |
|
|
NH |
|
Піридин |
Піран |
Піперидин |
||||||
З двома гетероатомами (діазини):
|
|
3N |
|
N |
|
|
|
|
5 |
4 |
5 |
4 |
3 |
5 |
4 |
3 |
|
|
|
|
|
|
|
|||
6 |
1 |
2 |
6 |
1 |
2 |
6 |
1 |
2N |
|
N |
|
|
N |
|
N |
|
|
Піримідин |
Піразин |
Піридазин |
||||||
Гетероциклічні сполуки з конденсованими ядрами
6 |
5 |
4 |
3 |
|
6 |
5 |
4 |
3 |
|
2 1 |
|
9 |
8 |
7 |
|
7 8 |
1 2 |
|
7 8 |
1 2N |
|
3 |
4 |
|
10 |
5 6 |
|||||
|
|
N |
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
Хінолін |
|
Ізохінолін |
|
|
Акридин |
|
|
|||||||
|
|
5 |
4 |
|
3 |
|
|
|
N |
6 |
5 |
7 |
N |
|
|
|
|
|
|
|
|
|
1 |
|
4 |
|
|
|
|||
|
|
6 |
7 |
1 |
2 |
|
|
|
2 |
3 |
9 8 |
|
|
||
|
|
|
|
N |
|
|
|
|
N |
|
N |
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
H |
|
|
|
|
|
|
Індол |
|
|
|
|
|
Пурин |
|
|
|||||
П’ятичленні ароматичні гетероцикли з одним гетероатомом
Група піролу
Пірол (від грецьк. piros — вогонь і лат. oleum
— олія) має дуже важливе значення для життєдіяльності тваринних і рослинних організмів. Його ядро міститься у гемі, хлорофілі та багатьох інших біологічно активних сполуках. Молекула піролу планарна, у спряженні беруть участь 6 електронів (4n+2): чотири р-електрони атомів Карбону взаємодіють із вільною електронною парою атома Нітрогену.
Участь неподіленої пари електронів гетероатома в утворенні π -електронного секстету знижує основність піролу порівняно з вторинними ароматичними амінами і призводить до ослаблення зв’язку N–H, тобто атом Нітрогену в піролі набуває кислотності. Останнє доводиться реакцією з сильними основами з утворенням солі, яка розкладається водою:
|
NaNH2 |
|
H2O |
+ NaOH |
|
NH3 |
|
|
|
|
N |
|
N |
|
N |
|
|||
H |
Na |
|
H |
|
Пірол Піролнатрій
Електрофільне заміщення в піролі відбувається в лужному середовищі або за наявності електрофільних реагентів з основами типу піридину. Відновлення перебігає поступово, найбільш реакційними у піролі є α -вуглецеві атоми:
β |
|
β |
2H |
|
|
|
2H |
|||
|
|
4 |
|
3 |
||||||
α |
N |
α |
|
5 |
1 |
2 |
|
|
N |
|
|
|
|
|
|
N |
|
|
|
||
|
H |
|
|
|
|
H |
|
|
|
H |
Пірол Піролін Піролідин
Піролідин — сильна основа. Його ядро входить до складу деяких природних сполук, лікарських засобів, алкалоїдів тощо.
Ядра піролу та продуктів його відновлення утворюють молекулу порфіну — циклічну тетрапірольну структуру. Похідні піролу (порфірини) в комплексі з атомами Феруму, Купруму, Магнію — металопорфірини — є компонентами складних білків (міоглобіну, цитохромів, каталази, пероксидази, гемоглобіну), які беруть участь у транспорті кисню та каталізі окисно-відновних реакцій у живих організмах.
|
|
R |
|
R |
|
N |
R |
|
N |
R |
|
|
H |
||||
H |
|
NH |
HN |
||
|
|
||||
NH |
HN |
H |
|||
|
|
||||
H |
R |
|
R |
||
|
N |
||||
N |
|
||||
|
|
|
|
||
|
|
R |
|
R |
Порфін Порфірин
64
|
|
|
H3C |
|
CH CH |
|
|
|
||
|
|
|
|
|
|
|
2 |
|
|
|
|
H3C |
N |
|
|
CH3 |
|
|
|
||
|
H |
|
|
|
Fe3+ |
|||||
|
|
|
NH |
H |
HN |
|
|
|||
|
H C |
|
|
CH |
CH |
|
|
|||
|
N |
|
|
|
||||||
|
2 |
|
|
|
|
2 |
|
|
||
H2C |
|
|
|
|
|
|
|
|||
HOOC |
|
|
H2C |
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
H2 C |
|
|
|
|
|
|
|
|
HOOC |
|
|
|
|
|
|
|
||
|
|
|
Протопорфірин ІІІ |
|
|
|
||||
|
|
|
|
|
H3C |
CH CH2 |
|
|||
|
|
|
H3C |
|
N |
|
CH3 |
|
||
|
|
|
|
|
|
|
|
|||
|
|
Fe3+ |
|
N Fe |
N |
|
|
|
||
|
|
|
H C |
|
|
|
|
CH |
CH |
|
|
|
N |
|
|||||||
|
2 |
|
|
|
|
2 |
||||
|
|
|
H2C |
|
|
|
|
|
|
|
|
HOOC |
|
H2C |
CH3 |
|
|
|
|||
|
|
|
|
|
|
|
|
|||
H2C
HOOC
Гем
Триптофан |
Триптамін |
||||||
CH2 |
CH COOH |
|
|
|
CO2 |
CH2 |
CH2 |
|
|
|
|||||
|
|
|
|
|
|
NH2 |
|
|
NH2 |
|
|
|
|
||
N |
N |
||||||
H |
H |
||||||
CH2 C
O
N
H
Індолілпіровиноградна кислота
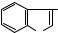 CH3
CH3
|
|
|
Фермент |
|
|
|
|
|
|
|
моноаміно- |
|
|
|
|
|
[ |
|
оксидаза |
COOH |
O] |
|
|
- C |
|
|
|
|
|
|
|
|
O |
|
CH2COOH |
|
2 |
|
|
|
|
|
N |
|
|
|
H |
|
O2 |
Індолілоцтова кислота |
|
C |
|
|
|
- |
|
(гетероауксин) |
|
|
|
||
N |
N |
H |
H |
Скатол |
Індол |
O |
|
O S OH |
OH |
O |
|
N |
N |
H |
H |
Порфіни, частково чи повністю заміщені в |
Індоксилсульфат |
Індоксил |
|
|
|||||
|
|
|
|
|
|
||||
пірольних циклах, називаються порфіринами. |
|
|
|
|
|
|
|||
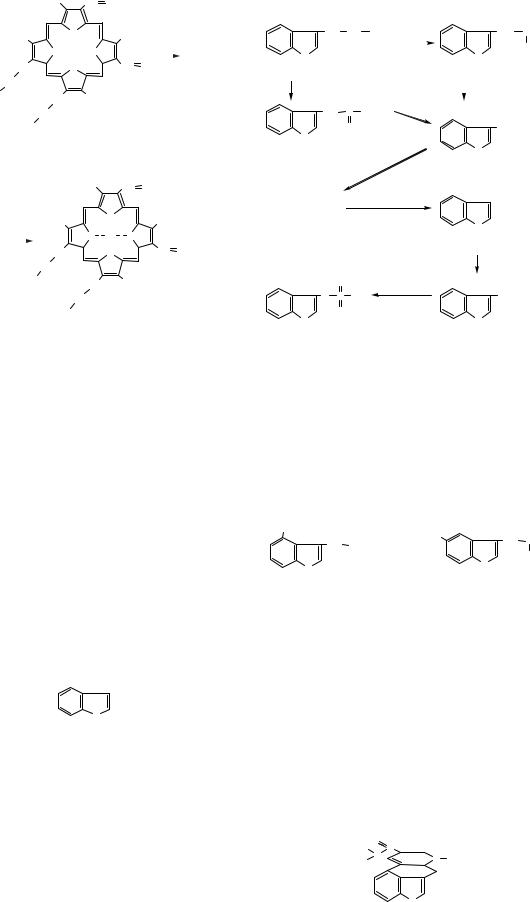
Похідною порфірину, що входить до складу ге- |
Концентрація індикану в сечі є біохімічним |
||||||||
моглобіну, є гем — комплекс протопорфірину III |
показником активності процесів гниття білків у |
||||||||
(за старою номенклатурою Фішера — протопор- |
кишечнику та функціонального стану печінки. |
||||||||
фірин IX) з іоном Феруму (ІІ). |
Похідними триптаміну є псилоцин (4-гідрокси- |
||||||||
Гемоглобін, у якого гем є активним центром, |
диметилтриптамін) і серотонін. Псилоцин був |
||||||||
утворює з киснем нестійку молекулярну сполуку |
одержаний з отруйних шкірних виділень жаб, він |
||||||||
— оксигемоглобін, що легко дисоціює з виділен- |
є одним із найбільш сильнодіючих галюцино- |
||||||||
ням кисню. |
|
|
|
генів. |
|
|
|
||
Г. Фішер (1935) виявив структуру гему та |
|
|
|
||||||
синтезував його. Розщеплення гему спричинює |
OH |
|
|
|
|||||
утворення лінійних тетрапірольних структур, го- |
HO |
|
|
||||||
|
|
|
CH2 |
CH2 |
|||||
ловна з яких — білірубін. |
|
|
|
|
|
|
|||
|
|
CH2 CH2 N(CH3)2 |
|||||||
|
|
NH2 |
|||||||
|
|
|
|
|
|
|
N |
||
Група індолу |
N |
|
|
||||||
H |
|
|
|||||||
H |
|
|
|||||||
|
|
|
|
|
|
|
|||
Індол (або бензопірол) — конденсований ге- |
Псилоцин |
Серотонін |
|||||||
тероцикл із ядрами піролу і бензену. Багато фізіо- |
|
|
|
|
|
|
|||
логічно активних сполук містять ядра індолу. У |
Галюциногени спричиняють у людини стан, |
||||||||
природі індол зустрічається, головним чином, у |
подібний до сну, що супроводжується зоровими |
||||||||
вигляді похідних, здебільшого утворених із трип- |
(кольоровими) та слуховими галюцинаціями. |
||||||||
тофану внаслідок різних біохімічних перетворень. |
Серотонін (5-гідрокситриптамін) відіграє |
||||||||
|
4 |
|
|
роль одного з медіаторів нервової системи у |
|||||
5 |
|
3 |
людини і вищих тварин, регулює кров’яний |
||||||
|
|
||||||||
6 |
7 |
1 |
2 |
тиск. |
|
|
|
||
|
|
N |
|
|
|
|
|||
|
|
H |
|
До групи речовин, що містять ядро індолу, та- |
|||||
|
Індол |
|
кож належать алкалоїди: стрихнін, резерпін, |
||||||
|
|
|
|
||||||
Індол — це кристалічна сполука з неприєм- |
лізергінова кислота. Так, діетиламід лізергінової |
||||||||
ним запахом екскрементів. Але в дуже малих кон- |
кислоти (ЛСД) — найактивніший із галюцино- |
||||||||
центраціях індол має запах жасмину, тому за- |
генів і найбільш сильнодіючий наркотик, його |
||||||||
стосовується у виробництві парфумів. Ядро індо- |
діюча доза — близько 1 мг. |
|
|
||||||
лу міститься у ряді важливих сполук: триптофан, |
|
|
|
|
|
|
|||
серотонін, триптамін, індоксил, алкалоїди, лі- |
H5C2 O |
|
|
|
|||||
карські засоби. Індол утворюється при гнитті |
C |
|
|
||||||
білків. У клітинах печінки індол, що надходить |
H5C2 N |
N CH3 |
|
|
|||||
із кишечнику, піддається детоксикації шляхом |
|
|
|
|
|
|
|||
мікросомального окиснення (індоксил) та утво- |
|
|
|
N |
|
|
|||
рення складного ефіру з сульфатною кислотою |
|
|
|
|
|
||||
(реакція кон’югації), який екскретується нирка- |
|
|
|
H |
|
|
|||
Діетиламід лізергінової кислоти |
|
|
|||||||
ми у вигляді калієвої солі — індикану: |
|
|
|||||||
65

П’ятичленні гетероцикли з двома гетероатомами
Група імідазолу
За наявності кількох гетероатомів у циклі з спряженими подвійними зв’язками електронна густина в кільці розподілена неоднаково, що позначається на хімічних властивостях цих сполук. Вони менш активні в реакціях електрофільного заміщення порівняно з п’ятичленними циклами з одним атомом Нітрогену, утворюють водневі зв’язки і мають схильність до таутомерних перетворень.
Молекули імідазолу утворюють водневі зв’язки за рахунок атома Гідрогену в положенні 1 і неподіленої електронної пари атома Нітрогену в положенні 3, що приводить до виникнення асоціатів:
H N N - - - - H N N - - - - H N N
- - - - H N N
Наслідком такої асоціації є швидкий міжмолекулярний обмін атомами Гідрогену, наявність якого доводиться прототропною таутомерією для деяких похідних імідазолу:
H3C 4 |
|
3N |
|
|
|
H3C 5 |
|
1N H |
|
|
|
|
|
||||
|
|
|
|
|||||
5 |
1 |
2 |
|
4 |
3 |
2 |
||
|
N |
|
|
|
|
|
N |
|
H
4-Метилімідазол 5-Метилімідазол
Багато похідних імідазолу зустрічається в природі. Вони мають велике біологічне значення. Найважливішими є α -амінокислота гістидин і продукт її декарбоксилювання — гістамін.
N |
|
|
|
CO2 |
N |
|
|
|
|
CH2 CH2 |
COOH |
|
CH2 |
CH2 |
|||
N |
|
N |
||||||
|
|
|
|
|
|
|
||
H |
NH2 |
|
|
H |
|
NH2 |
||
Гістидин Гістамін
Гістидин (незамінна амінокислота) бере участь у біосинтезі білків, у тому числі й глобіну.
Імідазольне ядро входить до складу пуринових основ, кофеїну, теоброміну, сечової кислоти і пілокарпінових алкалоїдів.
Група піразолу
Піразол можна розглядати як похідне піролу, в якого група СН= заміщена одним гетероатомом Нітрогену. В піразолі в α -положенні перебуває другий атом Нітрогену, внаслідок чого він має основні властивості на відміну від піролу, але ароматичність ядра зберігається. За відновлення піразолу на першій стадії утво-
рюється піразолін, а потім піразолідин:
|
[2H] |
[2H] |
|
N |
|
NH |
N H |
N |
|
N |
N |
H |
|
H |
H |
Піразол Піразолін Піразолідин
Ядро піразолідину є основою бутадіону, що
має анальгезуючі, жарознижувальні та протизапальні властивості. За протизапальною активністю він значно сильніший, ніж амідопірин або похідні саліцилової кислоти.
CH3 CH2 CH2 CH2 |
CH |
3 |
C |
O |
|
4 |
|
|
O C 5 1 2 N
N
Бутадіон 1,2-дифеніл-4-бутилпіразолідиндіон-3,5
Ядро піразолу у вигляді оксопохідного є основою таких лікарських препаратів, як анти-
пірин, амідопірин і анальгін, що використовують-
ся як аналгетики та жарознижувальні засоби.
|
|
HO |
N |
|
|
|
|
O |
|
C |
|
NH |
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
C N |
|
|
|
|
|
|||||||||||||||
|
|
N |
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
N |
|
|
|
|
|
|
||
|
|
H |
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
H |
|
|
|
|
|
|
||
|
Гідроксиформа |
|
|
|
|
|
Оксоформи |
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
Піразолон-5 |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
H3C |
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
SO3Na |
|
|
|
|||||
HC |
|
C CH3 |
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
|
|
|
||||||
|
|
|
|
N C |
4 3 C CH3 |
2 |
|
|
N C |
|
|
|
|
C CH3 |
||||||||||||
4 |
3 |
H3C |
|
|
|
|
|
4 3 |
||||||||||||||||||
O C 5 1 2 N CH3 |
O |
|
C |
5 |
1 |
2 |
N CH |
|
|
H |
C |
|
|
|
|
|||||||||||
|
N |
|
|
|
|
|
|
3 |
|
|
O C |
5 |
1 |
2 |
N |
CH3 |
||||||||||
|
|
|
|
|
|
|
|
|
N |
|
3 |
|
|
|
|
|
|
|
||||||||
|
C6H5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
C6H5 |
|
|
|
|
|
|
|
C6H5 |
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
Антипірин |
|
|
|
Амідопірин |
|
|
|
|
Анальгін |
|
||||||||||||||||
Слабка розчинність амідопірину у воді робить неможливим його застосування у вигляді ін’єкцій, тому в молекулу амідопірину ввели залишок гідросульфату натрію і отримали новий препарат — анальгін.
Група тіазолу
Тіазольне ядро входить до складу найважливіших природних і синтетичних біологічно активних і лікарських речовин: вітаміну В1 (тіамін), пеніциліну та сульфаніламідних препаратів. Деякі сульфаніламідні препарати (у тому числі норсульфазол) мають високу активність проти кокових бактерій і кишкових інфекцій.
O N
H2N |
S N |
O H S
Норсульфазол 2-(пара-амінобензенсульфамідо)-тіазол
Тіамін (В1) — один із найважливіших вітамінів. У його молекулі два гетероциклічних ядра
— піримідинове та тіазольне, які з’єднані метиленовою групою.
NH2
|
|
|
N 3 4 5 |
|
CH2 |
+ |
|
|
|
|
|
|
|
||
|
|
|
|
N |
CH3 |
|
|
|
|
|
|||||
|
|
|
|
2 1 6 |
|
|
|
|
|
CH CH OH |
|
|
|||
H3C |
N |
|
|
|
|
S |
2 |
2 |
|
|
|||||
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
Тіамін (вітамін В1) |
|
|
|
|
|
||||||
|
|
NH2 |
|
+ |
|
|
|
|
|
|
|
|
|
||
|
|
4 |
|
|
|
|
|
|
|
|
|
|
|
||
N |
3 |
5 |
CH |
|
N |
|
|
CH |
|
|
O |
OH |
|||
|
|
|
|
||||||||||||
|
|
2 |
|
|
3 |
|
|
||||||||
|
2 |
1 6 |
|
|
|
|
|
CH CH O |
|
|
|
|
|||
|
|
|
|
|
P O P O |
||||||||||
|
|
|
|
|
|
|
|||||||||
H3C |
|
N |
|
|
|
S |
2 |
2 |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
OH |
OH |
|||||
Кокарбоксилаза
66

Дефіцит вітаміну В1 у продуктах харчування призводить до тяжкої хвороби під назвою берібері, що виявляється нервовими розладами, порушенням серцевої діяльності та захворюваннями шкіри. Потреба у вітаміні В1 пов’язана з тим, що він у вигляді тіамінпірофосфату (кокарбоксилаза) входить до складу кількох ферментних систем, які каталізують процеси окиснювального декарбоксилювання багатьох α -кетокислот, і бере участь у синтезі ацетилкоензиму А. Кокарбоксилаза — складній ефір тіаміну та пірофосфорної кислоти.
Шестичленні гетероцикли з одним і двома гетероатомами
Група піридину
Ядро піридину входить до складу багатьох природних сполук, наприклад, алкалоїдів (нікотин, анабазин), вітамінів, коферментів, численних лікарських препаратів. До цієї групи належать гетероциклічні сполуки, які мають одне ядро з одним гетероатомом Нітрогену (піридин), а також сполуки з конденсованими ядрами — хінолін, ізохінолін і акридин.
54 3
61 2
N
Піридин
Піридин — ароматична сполука. Порівняно з бензеном він є менш реакційноздатним щодо електрофільних реагентів і більш реакційноздатним — щодо нуклеофільних реагентів.
Наприклад, бромування, гідроксилювання піридину — реакція електрофільного заміщення:
+ Br2 300 °C |
|
Br |
|
|
+ HBr |
||
N |
|
N |
|
+ K+OH- ≈ |
400 °C |
|
|
|
|
|
|
N |
|
N |
O-K+ |
|
|
||
Реакція нуклеофільного заміщення відбувається тільки з сильними нуклеофільними реагентами (луги реагують із піридином тільки при t=400 °С з утворенням солі α -піридинів). Із біохімічної точки зору, важливими є такі похідні піридину, як нікотинова й ізонікотинова кислоти, амід нікотинової кислоти і деякі інші похідні.
Ізонікотинова кислота
Широкого застосування у фтизіатрії сьогодні набув протитуберкульозний препарат тубазид
—гідразит ізонікотинової кислоти (ізоніазид). Ізонікотинову кислоту отримують окисненням
γ -піколіну:
CH3 |
COOH |
O C |
Cl |
O C |
OC2H5 |
O C NH NH2 |
[O], t° |
SOCl2 |
|
C2H5OH |
|
H2N NH2 |
|
|
HCl |
|
HCl |
|
C2H5OH |
|
N |
N SO2 |
N |
|
N |
|
N |
γ -Піколін |
|
|
|
|
|
Тубазид |
Високою протитуберкульозною активністю, що перевищує активність пара-аміносаліцилової кислоти (ПАСК) і антибіотика стрептоміцину, характеризуються продукти конденсації ізоніазиду з оксосполуками — це фтивазид, салюзид, ласуран тощо. Фтивазид є продуктом конденсації ізоніазиду (тубазиду) та ваніліну:
O C NH NH2 |
O |
|
O C NH N |
|
|
|
|
C |
OH |
||
+ |
C |
OH - H2O |
|||
H |
|
||||
N |
H |
OCH3 |
N |
OCH3 |
|
Ізоніазид |
|
Ванілін |
Фтивазид |
|
Нікотинова кислота, нікотинамід
Вітамін РР, або амід нікотинової кислоти, застосовується як протипеларгічний засіб, він є складовою частиною близько 100 ферментів, структурною одиницею коферментів НАД+ (нікотинамідаденіндинуклеотид) та НАДФ+ (нікотинамідаденіндинуклеотидфосфат), які разом із відповідними білками каталізують процес перенесення Гідрогену. Амід нікотинової кислоти одержують із β -піколіну:
|
|
|
O |
O |
CH3 |
|
COOH |
C Cl |
C NH2 |
[O] |
|
SOCl2 |
NH3 |
|
|
|
HCl |
HCl |
|
N |
N |
SO2 |
N |
N |
β -Піколін Нікотинова |
Хлорангідрид |
Амід |
||
нікотинової |
нікотинової |
|||
|
кислота |
кислоти |
кислоти |
|
|
|
|
||
Діетиламід нікотинової кислоти (кордіамін) є ефективним стимулятором ЦНС. Кордіамін одержують із хлорангідриду нікотинової кислоти:
O |
O |
C2H5 |
|
C Cl |
C N |
||
C2H5 |
|||
(C2H5)2NH |
|
||
HCl |
|
|
|
N |
N |
|
Кордіамін
Вітамін В6
Піридинове ядро міститься в піридоксалі, піридоксаміні та піридоксолі (піридоксині). Фосфорильовані похідні вітаміну В6 (піридоксальфосфат і піридоксамінфосфат) виконують коферментні функції в реакціях обміну амінокислот.
|
O |
|
O |
O |
|
C H |
|
C H |
|
|
|
|
||
HO |
CH2OH |
HO |
|
CH2 O P OH |
|
|
|
|
OH |
H3C |
N |
H3C |
N |
|
Піридоксаль Піридоксальфосфат
Ядро піперидину лежить в основі деяких синтетичних замінників морфіну — промедолу та ін.:
|
|
|
|
|
O |
|
|
C2 H5OH, Na |
H5C6 |
O C C2H5 |
|
|
|
H3C |
|
||
|
|
|
C2H5ONa |
CH3 |
|
|
|
|
|
||
N |
|
|
|
N |
|
|
|
|
|
H |
N |
|
|
|
|
CH3 |
|
|
|
|
|
|
|
Піридин Піперидин Промедол
67
За своєю дією на ЦНС промедол близький до морфіну: він знижує чутливість ЦНС до больових імпульсів, знижує умовні рефлекси, але меншою мірою, ніж морфін, пригнічує дихальний центр і збуджує центр блукаючого нерва. Піперидинове ядро міститься в алкалоїдах, які мають різний вплив на ЦНС.
|
OH |
O |
N |
C6H5 CH CH2 |
CH2 C C6H5 |
CH2 CH2 CH3 |
N |
|
H |
|
CH3 |
Коніїн Лобелін
Коніїн токсичний, він паралізує нервові закінчення. Лобелін та алкалоїди, близькі до нього за структурою, застосовують у вигляді гідрохлоридів як ефективні засоби, що стимулюють дихання.
Група хіноліну
Хінолін та ізохінолін належать до конденсованої системи піридину і бензенового ядра. Похідними хіноліну є деякі природні алкалоїди, наприклад, хінін і цинхонін — протималярійні та жарознижувальні засоби. Гідроксильований хінолін — структурний компонент деяких ліків, що характеризуються антибактеріальною та протигрибковою активністю. Препарати, що містять ядро хіноліну, застосовуються як хіміотерапевтичні й антисептичні засоби (ентеросептол, нітроксолін):
6 |
5 |
10 |
4 |
3 |
|
7 |
8 |
9 |
1 |
2 |
N |
|
|
|
N |
|
Ізохінолін |
Хінолін |
|
||||
|
Cl |
|
|
NO2 |
|
I |
|
|
N |
N |
|
|
|
|
|||
|
OH |
|
|
OH |
|
Ентеросептол 5-НОК (або нітроксолін)
CH3O |
|
CH3O |
|
CH3O |
N |
||
|
|||
|
CH2 |
CH3O |
Папаверин
Ізохінолінове ядро входить до складу деяких алкалоїдів, що мають знеболювальний (морфін) і протисудорожний (папаверин) ефект.
Група піримідину
Шестичленні гетероциклічні сполуки з двома гетероатомами називаються азинами. Наявність другого атома Нітрогену в ядрі значно знижує його електронну густину, особливо в положенні 2, 4, 6. У реакції електрофільного заміщення азини практично не вступають. Їх реакційна здатність помітно збільшується у разі введення електронодонорних замісників (–ОН, –NH2).
N
3 4 |
5 |
N3 4 |
5 |
N3 4 |
5 |
|||
N2 |
1 |
6 |
2 |
1 |
6 |
2 |
1 |
6 |
|
N |
|
|
N |
|
|
N |
|
1,2-Діазин |
1,3-Діазин |
1,4-Діазин |
||||||
(піридазин) |
(піримідин) |
(піразин) |
||||||
Ядро піримідину входить до складу багатьох біологічно активних сполук: деяких вітамінів, ліків, нуклеїнових кислот тощо. Особливо важливі гідроксита амінопохідні піримідину: урацил, тимін і цитозин — компоненти нуклеїнових кислот. Їм притаманна лактимлактамна таутомерія:
|
|
OH |
|
|
OH |
|
|
|
O |
|||||||||||
N3 4 |
5 |
|
|
|
|
|
N |
|
|
H N |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
HO |
2 |
1 |
6 |
|
|
|
|
O N |
O N |
|||||||||||
|
N |
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
H |
||||||
Урацил (2,4-дигідроксипіримідин) |
||||||||||||||||||||
|
OH |
|
|
|
|
|
|
|
|
OH |
|
|
|
|
O |
|||||
N |
|
|
CH3 |
|
|
N |
|
|
H |
|||||||||||
4 |
|
|
|
|
|
|
|
N |
||||||||||||
3 |
|
5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
1 |
6 |
|
|
|
|
|
|
|
O N |
|
|
|
O N |
||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||
HO |
N |
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
H |
||||
Тимін (2,4-дигідрокси-5-метилпіримідин)
NH2 NH2
N3 4 |
5 |
|
N |
|
2 |
1 |
6 |
O |
|
HO |
N |
|
N |
|
|
|
|
||
H
Цитозин (4-аміно-2-гідроксипіримідин)
Урацил, тимін, цитозин — тверді сполуки, мають високу температуру плавлення, розчинні у воді, але нерозчинні в неполярних органічних розчинниках. Для них характерна наявність міжмолекулярних водневих зв’язків, які відіграють значну роль у формуванні просторової структури нуклеїнових кислот.
O |
|
H |
|
|
|
.... |
O N |
|
N H |
||
.... |
H |
N |
|
||
N O: |
|
|
H O
Урацил (димер)
У нуклеїнових кислотах урацил, тимін і цитозин перебувають у вигляді β -глікозидів рибози чи дезоксирибози — нуклеозидів. Фосфорильовані нуклеозиди утворюють групу нуклеотидів:
|
|
|
|
H |
O |
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
O |
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
N3 4 5 |
|
|
|
|
|
|
|
|
|
|
|
|
N 3 4 |
5 |
||||||||
|
|
|
|
|
2 |
1 6 |
|
|
OH |
|
|
|
|
|
|
2 |
1 |
6 |
|||||||||
5' |
|
|
|
|
O |
N |
|
|
|
|
|
|
5' |
|
|
|
O |
|
|
|
N |
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
HOCH2 |
|
|
|
O |
HO |
|
P |
|
|
O |
|
CH2 |
|
|
O |
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
4' |
|
|
|
|
|
1' |
|
|
|
|
4' |
|
|
|
1' |
|
|||||||||||
|
H |
H |
|
|
|
|
O |
|
|
H |
H |
|
|||||||||||||||
|
|
|
|||||||||||||||||||||||||
H |
|
|
3' |
2' |
|
|
H |
|
|
|
|
|
|
|
H |
|
|
3' |
2' |
|
|
H |
|
||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
OH OH |
|
|
|
|
|
|
|
|
|
OH OH |
|
||||||||||||||
Уридин |
|
|
|
|
Уридилова кислота |
||||||||||||||||||||||
(нуклеозид) |
|
|
|
|
|
|
(нуклеотид) |
|
|||||||||||||||||||
Фторпохідні урацилу та тиміну застосовуються в онкології для лікування деяких форм он-
68