Материал: Preparaty_-_proizvodnye_tsiklopentanpergidrofenantrena__1
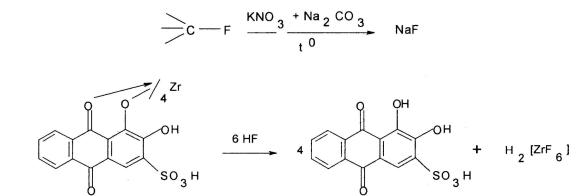
ализаринат циркония |
ализариновый красный |
красно-фиолетовый цвет |
желтый цвет |
Для идентификации флюоцинолона ацетонида ЕФ рекомендует использовать реакцию с хромовой смесью (раствор бихромата калия в концентрированной серной кислоте). При нагревании реакционной смеси на пламени горелки выделяются белые пары и стекло пробирки над жидкостью становится матовым. Реакция основана на образовании в результате минерализации препарата фтороводородной кислоты (HF), которая растворяет стекло.
17β-спиртовый гидроксил (метилтестостерон, метандриол) обнаруживают по реакции этерификации с уксусным ангидридом в присутствии безводного пиридина. Измеряют температуру плавления образующихся сложных эфиров (tпл метилтестостерона ацетата = 173–176 °С, tпл метандриола ацетата = 174–180 °С).
Лекарственные вещества, содержащие сложноэфирную группу (кортизона ацетат, дезоксикортона ацетат, эстрадиола дипропионат, тестостерона пропионат и др.), с гидроксиламином в щелочной среде образуют гидроксамовую кислоту, которая при добавлении раствора хлорида железа (III) окрашивается в вишнево-красный цвет.
Препараты, представляющие собой сложные эфиры, можно идентифицировать по продуктам щелочного гидролиза. Так, tпл тестостерона, полученного в результате гидролиза тестостерона пропионата, составляет 150–153 °С, a tпл эстрадиола, выделенного из эстрадиола дипропионата, – 173–179 °С.
ЕФ рекомендует использовать для идентификации лекарственных препаратов, представляющих собой эфиры уксусной кислоты (ципротерона ацетат, гидрокортизона ацетат, дезоксикортона ацетат и др.) реакцию с нитратом лантана и йодом. Субстанцию помещают в колбу, смешивают с 0,15 мл 85% раствора фосфорной кислоты, на колбу помещают предметное стекло, с которого свисает капля 5% раствора лантана нитрата и нагревают в течение 5 мин. Предметное стекло осторожно снимают, переворачивают и
41
после охлаждения последовательно добавляют по 1 капле 0,01 М раствора йода и раствора аммиака. Через 1–2 мин появляется синее окрашивание, обусловленное адсорбцией йода основным ацетатом лантана
([CH3COO]3La) 2J2 KJ.
Частные реакции препаратов стероидных гормонов
Стероидные гормоны вступают в следующие виды реакций:
–в ципротерона ацетате после сплавления карбонатом натрия обнаруживают хлорид-ион реакцией с нитратом серебра (ЕФ);
–к спиртовому раствору прогестерона добавляют щелочной раствор 1,3-динитробензола, появляется розовое окрашивание, постепенно переходящее в красно-коричневое (ГФ);
–2 мг этинилэстрадиола растворяют в 2 мл концентрированной серной кислоты, через 1–2 мин появляется оранжево-красное окрашивание с желто-зеленой флюоресценцией, добавляют 1 каплю раствора сульфата железа (III) аммония (квасцы железоаммониевые) и воды – раствор темнеет и через некоторое время образуется красновато-коричневый осадок (ГФ);
–тестостерона пропионат, этистерон (прегнин) и норэтистерон идентифицируют реакцией со спиртовым раствором бутилгидрокситолуола (2,6-ди-трет-бутил-n-крезол) в щелочной среде, при нагревании на водяной бане (t = 70–80 °С) в течение 30 мин. После охлаждения раствора до комнатной температуры тестостерона пропионат и этистерон (прегнин) образуют продукты реакции, окрашенные в интенсивный синий цвет, а норэтистерон – в желто-розовый (ЕФ).
5.2.Методы количественного анализа стероидных гормонов
всубстанциях и лекарственных формах
5.2.1. Титриметрические методы
Молекулы стероидных гормонов содержат ограниченное количество функциональных групп, которые можно было бы использовать для их титриметрического определения в субстанциях и лекарственных формах. Чаще всего количественный титриметрический анализ проводят по следующим группам:
– этинильной группе, используя ее способность образовывать двойные соли с нитратом серебра. Выделившееся эквивалентное количество азотной кислоты оттитровывают ОДМ раствором NaOH, точку эквивалентности определяют потенциометрически или с помощью индикатора бром крезолового синего (Мм эквивалента = Мм).
42
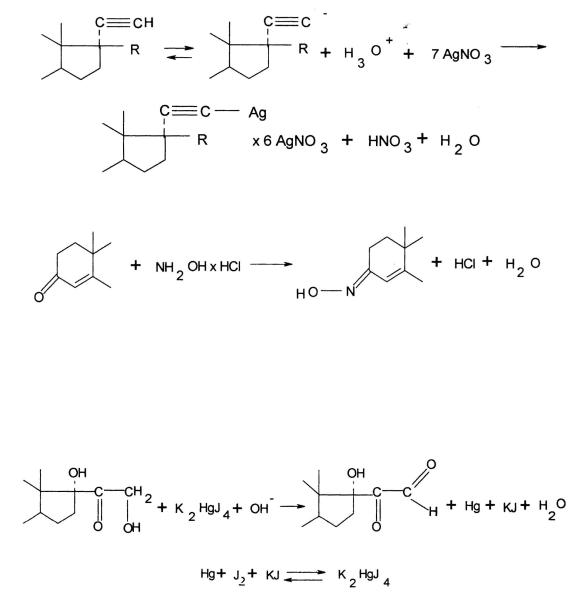
Данный метод включен в ЕФ для количественного определения этистерона, норэтистерона, левоноргестрела, этинилэстрадиола и местранола;
– 3-кетогруппе методом косвенной ацидиметрии, после реакции присоединения с гидроксиламина гидрохлоридом (Мм экв = Мм):
HCl + NaOH →NaCl + Н2O
– α-кетольной группе, используя ее способность к восстановлению. Тетрайодмеркуриат калия (реактив Несслера) взаимодействует с кортикостероидами в щелочной среде, при этом выделяется эквивалентное количество металлической ртути, которую окисляют избытком титрованного раствора йода в кислой среде в присутствии избытка калия йодида:
Избыток титранта оттитровывают раствором натрия тиосульфата (Мм экв = Мм/2);
–фторпроизводные глюкокортикоидов определяют после гидропиролитического отщепления фтора методом ториметрии, используя для установления точки эквивалентности индикатор метилтимоловый синий или потенциометрию;
–в основе обратного алкалиметрического определения сложноэфирной группы эстрадиола дипропионата лежит реакция щелочного гидролиза, который проводят в присутствии избытка 0,1 М спиртового раствора КОН. Избыток щелочи оттитровывают кислотой (индикатор – фенолфталеин). Параллельно проводят контрольный опыт (Мм экв = Мм/2).
43
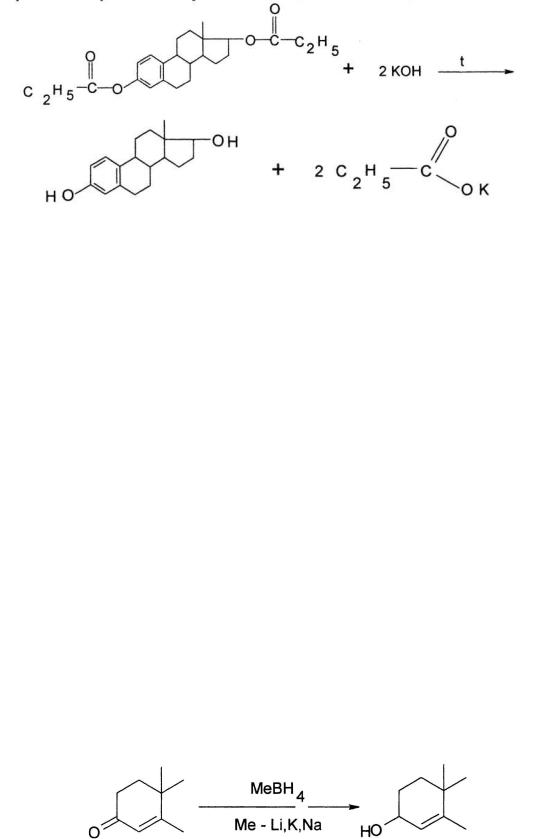
КОН + HCl→ KCl + Н2О
Основное применение титриметрические методы находят при определении субстанций стероидных гормонов. К недостаткам метода можно отнести использование большой навески вещества, поэтому данный метод не находит применения в анализе низкодозированных лекарственных форм стероидных гормонов.
5.2.2. Спектральные методы
Как отмечалось выше, УФ-спектроскопия, в том числе и количественная, является унифицированным методом анализа стероидных гормонов, содержащих следующие функциональные фрагменты в молекуле.
1. α, β-ненасыщенные кетоны (андрогены, анаболики, гестагены, кортикостероиды), которые имеют в этанольных растворах сходные УФспектры с максимумом поглощения в области 230–245 нм различной интенсивности. Метод УФ-спектроскопии рекомендован ГФ XI, МФ и ЕФ для контроля качества как субстанций стероидных гормонов, так и лекарственных форм на их основе.
В случае анализа масляных инъекционных растворов, низкодозированных таблеток, суспензий и мазей можно использовать более чувствительный метод дифференциальной спектроскопии, основанный на восстановлении стероидов борогидридами щелочных металлов до соответствующих спектрально неактивных 3-гидроксипроизводных.
44
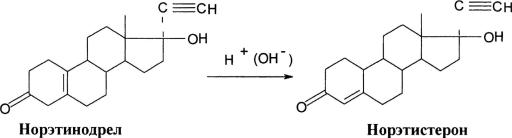
Если в кювету сравнения поместить раствор восстановленного 4-3- кетостероида, а в рабочую – раствор невосстановленного соединения с той же концентрацией, то разница оптических плотностей при 240 нм отвечает содержанию ненасыщенного соединения.
Определение спектрально неактивных 5(10)-3-кетостероидов, например норэтинодрела, можно проводить после его превращения в соответствующие спектрально активные 4-3-кетопроизводные путем кислотного или щелочного гидролиза:
Количественное превращение позволяет проводить избирательное определение норэтинодрела в контрацептивных препаратах методом дифференциальной спектроскопии.
2. фенольное кольцо А – спектры очень характеристичны (λmax = 280 нм), но из-за низкой интенсивности поглощения практически не используются для количественного анализа. Для повышения чувствительности метода ЕФ рекомендует проводить количественное определение эстрадиола в 0,1 М растворе гидроксида натрия, измеряя оптическую плот-
ность при 238 нм (Е 1%1см = 335).
Содержание стероидных гормонов в субстанции или лекарственных формах рассчитывают на основании приведенной в частных статьях величины удельного показателя поглощения (Е 1%1см, табл. 6) или с использованием раствора стандартного образца.
Таблица 6
Значения удельного показателя поглощения (Е 1%1см) стероидных гормонов, используемые в НД для количественного определения
|
|
Максимум поглощения |
Удельный показатель |
Препарат |
|
в УФ-спектре препарата |
|
|
поглощения Е 1%1см |
||
|
|
(нм) |
|
1 |
|
2 |
3 |
|
|
Производные андростана |
|
Тестостерона пропионат |
|
241 |
490 |
Метилтестостерон |
|
241 |
540 |
|
45 |
|
|