Материал: Preparaty_-_proizvodnye_tsiklopentanpergidrofenantrena__1
|
|
Окончание табл. 6 |
|
1 |
2 |
3 |
|
|
Гестагены |
|
|
Прогестерон |
241 |
535 |
|
Медроксипрогестерона |
241 |
426 |
|
ацетат |
|||
|
|
||
Ципротерона ацетат |
282 |
414 |
|
|
Кортикостероиды |
|
|
Дезоксикортикостерона |
240 |
450 |
|
ацетат |
|||
|
|
||
Кортизона ацетат |
237 |
395 |
|
Гидрокортизон |
241,5 |
448 |
|
Гидрокортизона ацетат |
241 |
395 |
|
Преднизон |
238 |
425 |
|
Преднизолон |
243,5 |
415 |
|
Дексаметазон |
238,5 |
394 |
|
Бетаметазон |
238,5 |
395 |
|
Триамцинолон |
238 |
380 |
|
|
Эстрогены |
|
|
Эстрадиола бензоат |
231 |
500 |
Широкое применение в фармацевтическом и биоклиническом анализе стероидных гормонов находит фотоколориметрия, которая до использования в анализе стероидов хроматографии была единственным достаточно селективным и чувствительным методом анализа стероидных гормонов.
В количественном анализе кетостероидов (андрогены, анаболики, гестагены, кортикостероиды) используют два важнейших метода.
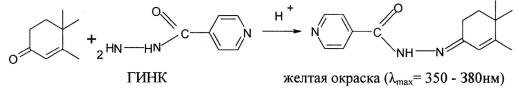
1. Метод с использованием гидразида никотиновой кислоты
(ГИНК) основан на реакции конденсации препарата в растворе метанола, содержащем хлористоводородную кислоту. Для стероидов, содержащих 4- 3-кетогруппы, реакция протекает в течение 20 мин при комнатной температуре. 1,4-3-кетостероиды менее реакционно-способны, поэтому определение проводят при нагревании до 50 °С в течение 1 часа или повышают концентрацию ГИНК.
Преимущества данного метода заключаются в том, что окраска раствора не зависит от природы используемого растворителя (этанол, хлоро-
46
форм и др.) и только для низкодозированных масляных растворов необходимо отделять масло на хроматографической колонке с флорисилом.
Метод ГИНК является унифицированным методом определения кетостероидов в лекарственных формах. ГФ IX использует данный метод для количественного определения преднизолона и гидрокортизона в мазях (ФС
42-3305-96 и ФС 42-1961-96 соответственно).
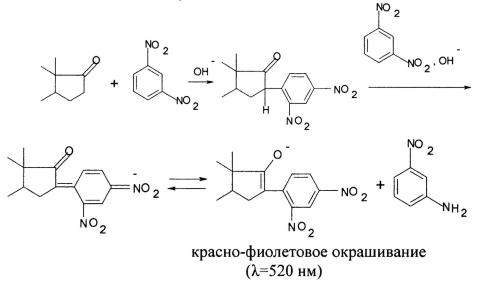
2. Метод Циммермана основан на взаимодействии 17-кетогрупп стероидных гормонов (эстрон, метаболиты тестостерона) с 1,3-динитро- бензолом в щелочной среде.
Необходимым условием протекания реакции является удобное стерическое расположение кетогруппы по соседству с метиленовой группой. В реакцию не вступают 4-3-кетостероиды и 21-незамещенные-20-кетосте- роиды. Метод Циммермана широко применяется в клиническом анализе для определения 17-кетостероидов в моче.
При фотоколориметрическом анализе эстрогенов находят применение цветные реакции на фенольное кольцо А:
–реакция азосочетания с диазотированными сульфаниловой кислотой, 3-нитроанилином, сульфатиазолом и другими ароматическими амина-
ми (λ = 540–550 нм);
–реакция нитрования ароматического кольца (λ = 400–435 нм);
–реакция восстановления молибдовольфрамофосфата (реактив Фолина) до окрашенного в синий цвет комплекса ((λ = 760 нм);
–реакция образования индофенолового красителя с реактивом Гиб-
бса (λ = 540 нм).
Гораздо большее значение в фармацевтическом фотоколориметрическом анализе эстрогенов имеет более чувствительный метод Кобера и его модификации, основанный на взаимодействии препаратов с минеральными
47
кислотами, в основном серной, или их растворами в различных растворителях (вода, этанол, метанол).
Основная роль кислоты заключается в дегидратации молекулы эстрогена с образованием двойной связи (связей), которые мигрируют к фенольному кольцу А. В ходе этого процесса метальная группа при С13 мигрирует в положение С17, кроме того, происходит сульфирование кольца А при С2. Окраска образующихся продуктов может возникать вследствие протонирования в сильно кислой среде, что приводит к образованию ионов карбонила, способных к резонансу. Вторая стадия метода Кобера носит окислительновосстановительный характер. В результате удлинения π-электронной системы в спектре окрашенного комплекса наблюдается батохромный сдвиг.
Данный метод широко применяется в анализе низкодозированных гормональных препаратов, содержащих этинилэстрадиол и местранол, так как эстрон, эстрадиол и гестагены не вступают в реакцию с серной кислотой в этих условиях.
Несмотря на удовлетворительную чувствительность и селективность реакции с участием реагентов, содержащих серную кислоту, разбавленную этанолом, а также простоту методики, в биофармацевтическом анализе чаще применяют более длительные двухстадийные реакции, обладающие еще более высокой чувствительностью и селективностью, с участием реагентов, содержащих серную кислоту, воду и различные добавки.
Первая стадия основана на классической методике Кобера – пробу лекарственной формы, содержащей эстроген, смешивают с 65 % раствором серной кислоты с добавкой фенола и нагревают – образуется продукт желтого цвета (λ = 450–500 им). На второй стадии смесь разбавляют водой до 40–50 % концентрации серной кислоты и вновь нагревают, окраска переходит в розовую (λ = 560 нм). Вместо фенола можно использовать гидрохинон. Другим важным вариантом метода Кобера является методика Хенни, предложившего реактив, содержащий, помимо серной кислоты, фенола и воды, еще и сульфат железа (III). Присутствие ионов Fe+3 повышает скорость развития окраски и ее стабильность. Метод Хенни включен в Фармакопею США для анализа эстрогенов и их конъюгатов в биожидкостях.
Для фотоколориметрического анализа кортикостероидов предложено множество методик, но основными в фармацевтическом анализе являются следующие.
1.Метод с использованием солей тетразолия рекомендован МФ III
иявляется основным методом анализа субстанций и лекарственных форм глюкокортикоидов и минералокортикоидов.
Ниже представлено уравнение химической реакции между α-кетоль- ной группой кортикостероидов и хлоридом трифенилтетразолия с образованием окрашенного формазана (Е1%1см = 400–405). Реакция 21-эфиров кор-
48
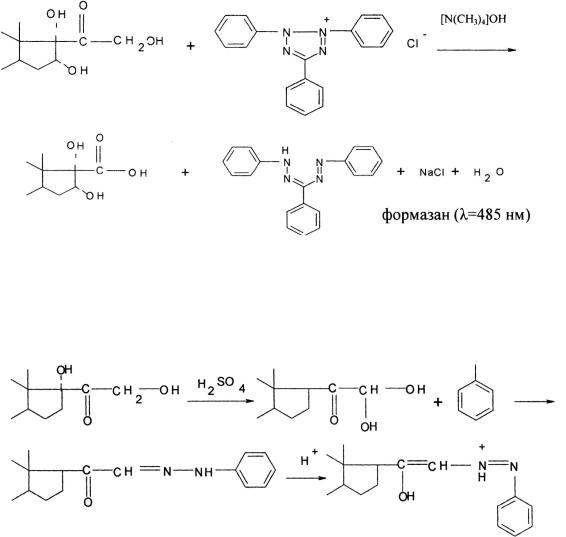
тикостероидов с солями тетразолия протекает медленно, поэтому необходимо провести предварительный гидролиз в щелочной среде. 11-кетопроиз- водные более реакционно-способны, чем 11β-производные. Основным недостатком реакции с солями тетразолия является влияние кислорода воздуха, вследствие чего ее следует проводить в атмосфере азота.
ЕФ рекомендует использовать данный метод для количественного определения флюоцинолона ацетонида в субстанции.
2. Метод Портера – Зильбера используется для анализа глюкокортикоидов в моче и других биопробах, так как в реакцию окисления фенилгидразином в присутствии серной кислоты вступают только 17α-гидрокси- производные:
Для всех классов стероидных гормонов известны методики спектрофлюориметрического количественного определения. В связи с высокой чувствительностью этот метод чаще всего используется для анализа содержания стероидных гормонов и их метаболитов в биологических объектах.
Из всех классов стероидных гормонов собственной флюоресценцией обладают только эстрогены, в структуре которых присутствует ароматическое кольцо А. Максимум возбуждающего излучения эстрогенов и их про-
49
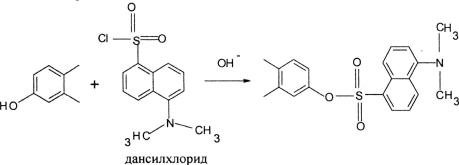
стых эфиров находится около 284 нм, а максимум испускания лежит в области 310–327 нм. Низкая интенсивность флюоресценции эстрогенов и малые длины волн возбуждения и испускания ограничивают возможности данного метода. Как правило, эстрогены переводят во флюоресцирующие производные с помощью химических реакций, например, с дансилхлоридом в щелочной среде:
У образующегося дансил производного максимум возбуждающего излучения находится в области 346–366 нм, а максимум спектра испускания – 502–525 нм. Данный метод рекомендован Британской фармакопеей (1980) для количественного анализа этинилэстрадиола в таблетках.
Появление окраски при взаимодействии стероидных гормонов с сильными минеральными кислотами (серной, фосфорной, трихлоруксусной и др.) обычно сопровождается флюоресценцией, это явление используется как для качественного, так и для количественного анализа. Флюоресценция под действием серной кислоты в присутствии этанола применяется для определения эстрогенов в низкодозированных лекарственных формах.
В основе флюориметрического определения метилтестостерона и метандиенона в таблетках лежит реакция с серной кислотой и 80%-ной фосфорной кислотой с добавлением трихлоруксусной кислоты соответственно.
Известны методики спектрофлюориметрического определения глюкокортикоидов в биопробах, основанные на образовании флюоресцирующих производных в присутствии серной кислоты и этанола. Максимумы возбуждения кортикостероидов находятся при длинах волн 470–780 нм, а максимумы испускания – 530–540 см.
5.2.3. Поляриметрия
Все стероидные гормоны являются оптически активными веществами, и их растворы в различных растворителях (этанол, диоксан, пиридин, хлороформ и др.) имеют характерную величину удельного вращения (см. приложение). Измерение величины угла вращения растворов стероидных гормонов проводят как для оценки их чистоты, так и для определения его концентрации в растворе. Однако метод поляриметрии включен только в
50