Материал: Preparaty_-_proizvodnye_tsiklopentanpergidrofenantrena__1
НД на субстанцию метандриола. Это связано с тем, что из-за отсутствия в молекуле метандриола хромофорной системы, возникающей вследствие сопряжения карбонильной группы при С3 и двойных связей кольца А, для него неприменимы унифицированные методики спектрофотометрии в УФ- и видимой областях спектра.
5.2.4.Хроматографические методы
Внормативной документации на субстанции и лекарственные формы стероидных гормонов, разработанной за последнее десятилетие, внедряются методики количественного определения с использованием ВЭЖХ. Этот метод введен в ФС 42-3464-97 «Таблетки метиландростендиола по 0,01 и 0,025 г» для определения примесей посторонних стероидов, однородности дозирования и количественного определения. Метандриол не имеет выраженного максимума поглощения в УФ-спектре, поэтому спектрофотометрическое определение для него невозможно, ранее в ГФ X использовался метод гравиметрии. Расчет количественного содержания проводится путем сравнения площадей пиков стандартного и анализируемого образца метиландростендиола.
Предложены методики количественного определения глюкокортикоидов в мазях (гидрокортизон и его ацетат, преднизолон, флюоцинолона ацетонид) методом ВЭЖХ в обращено-фазном режиме на колонках с сепа-
роном С18. В качестве элюента используется этанол. В сравнении с фармакопейными методами – спектрофотометрии в УФ- и видимой области спектра – относительная ошибка данного метода не превышает ± 4 %.
5.2.5. Полярография
Этот метод довольно распространен в фармацевтическом и биофармацевтическом анализе стероидных гормонов. Из всех функциональных групп стероидов только кетогруппа способна восстанавливаться на капельном ртутном электроде, поэтому основной класс стероидов, определяемый данным методом, это α,β-ненасыщенные кетостероиды – андрогены, анаболики, гестагены и кортикостероиды. Из-за разности потенциалов полуволн 4-3-кето- и 1,4-3-кетостероидов можно проводить их раздельное определение в одной пробе.
Полярографическое восстановление α,β-ненасыщенных 3-кетонов протекает с участием одного электрона и приводит к образованию пинакона:
51
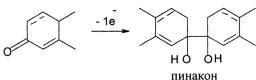
Полярографическое определение 3-кетостероидов проводят в растворе хлорида или гидроксида лития при различных величинах pH, а также в водно-спиртовых растворах на фоне буферного раствора Бриттона – Робинсона.
Для определения отдельных 4-3-кетостероидов (метилтестостерон, прогестерон) используется реакция с 3,5-динитробензоилхлоридом, а также процесс конденсации с раствором диметилглицилгидразида (реактив Жирара) с образованием полярографически активных диметилглицилгидразонов, которые в водно-спиртовых растворах на фоне буферного раствора Бриттона – Робинсона дают четкие полярографические волны.
17-кетостероиды (эстрон, андростерон и др.) не восстанавливаются на ртутном капельном электроде, но их гидразоновые производные обладают этой способностью, что делает возможным полярографическое определение этих соединений в биологических пробах и в культуральной жидкости при постадийном контроле получения эстрогенов, андрогенов и анаболиков.
Описан полярографический метод количественного определения гидрокортизона в мазях, содержащих тетрациклин и полимиксин. Метод основан на экстрагировании мази петролейным эфиром и 0,1 М раствором НСl с последующим полярографированием полученного экстракта гидрокортизона в смеси диметилформамида и (C2H5)4NBr с добавлением буферного раствора Бриттона – Робинсона до pH = 9,5.
Во ВНИИХФИ с помощью полярографического метода контролируют микробиологические реакции получения в полузаводских условиях преднизона из кортизона, преднизолона из гидрокортизона и дианобола из метилтестостерона, а также оптимальные условия экстракции получаемых стероидов из культуральных жидкостей.
Достоинства полярографического определения стероидных гормонов заключаются в следующем:
–высокая чувствительность метода (5–40 мкг/мл), что позволяет анализировать низкодозированные препараты с высокой степенью точности;
–при анализе лекарственных форм (мази, кремы, таблетки) не нужно отделять основу или экстрагировать препарат;
–в минимальных затратах труда.
52
5.2.6.Гравиметрия
Всвязи с трудоемкостью гравиметрического анализа и необходимостью использовать большую массу пробы данный метод редко используется
вколичественном анализе стероидов. ГФ X рекомендовала использовать гравиметрию для определения количественного содержания прогестерона в субстанции и сложных эфиров тестостерона в лекарственных формах.
Воснове определения прогестерона лежит реакция с 2,4-динитро- фенил гидразином в кислой среде, приводящая к образованию 3,20-биди- нитрофенилгидразона, малорастворимого в смеси этанола с водой.
Для надежного определения эфиров тестостерона (главным образом в масляных растворах для инъекций) служит реакция образования семикарбазона по 3-кетогруппе.
6.ОСОБЕННОСТИ КОНТРОЛЯ КАЧЕСТВА СТЕРОИДНЫХ ГОРМОНОВ В ЛЕКАРСТВЕННЫХ ФОРМАХ
Как правило, стероидные гормоны применяют в виде масляных растворов, суспензий или эмульсий для инъекций, таблеток, капсул, мазей и кремов. Основная сложность при проведении контроля качества этих лекарственных форм заключается в предварительной подготовке пробы.
Первым этапом пробоподготовки служит экстракция стероидных гормонов, которые являются, как правило, неполярными веществами. Экстракция гормонов из таблеток не вызывает затруднений, для этого используют метанол, этанол или водно-хлороформные смеси. Из водных суспензий гормоны извлекают хлороформом или дихлорэтаном, из масляных растворов гормоны отделяют с помощью этанола или метанола, для эстрогенов пользуются водными или спиртовыми растворами едкого натра.
При извлечении кортикостероидов из мазей и кремов применяют менее трудоемкую процедуру распределения лекарственной формы между полярным и умеренно полярным органическим растворителем. В первый растворитель переходит наполнитель, а во второй – лекарственное вещество. Чаще всего для экстракции глюкокортикоидов из мазей используют хлороформ, смесь гексан – ацетонитрил. Ацетонитрильную фазу можно непосредственно вводить в жидкостной хроматограф или анализировать спектральными или электрохимическими методами.
На втором этапе проводят идентификацию и количественное определение действующего вещества лекарственной формы. В последнем случае пользуются наиболее чувствительными и точными физикохимическими методами – спектрофотометрией в УФ- и видимой областях, а также ВЭЖХ на нормальных и обращенных фазах. Особые требования к точности и избирательности метода предъявляются при анализе низкодозированных комбинированных таблетированных форм – эстроген – гестаген, андроген – гестаген и др.
53
7. ТЕСТОВЫЕ ЗАДАНИЯ
Выберите правильный вариант ответа.
1.Гидрокортизона ацетат является производным
1)эстрана;
2)прегнана;
3)андростана;
4)холестана.
2.Этистерон (прегнин) является производным
1)эстрана;
2)прегнана;
3)андростана;
4)холестана.
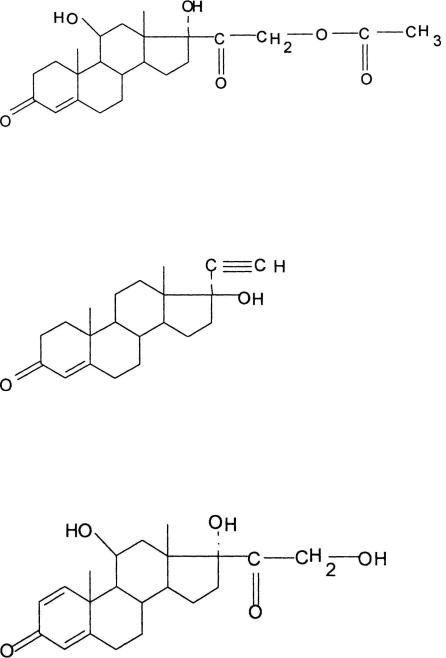
3.Химическое название лекарственного вещества
1)17α-гидроксиандростен-1,4-диол-3β, 11α;
2)прегнен-4-диол-17α, 21-дион-3,20;
3)прегнадиен-1,4-диол-17α, 21-дион-3,20;
4)прегнадиен-1,4-триол-17α, 11β, 21-дион-3,20;
5)прегнадиен-1,4-диол-17α, 21-трион-3,11,20.
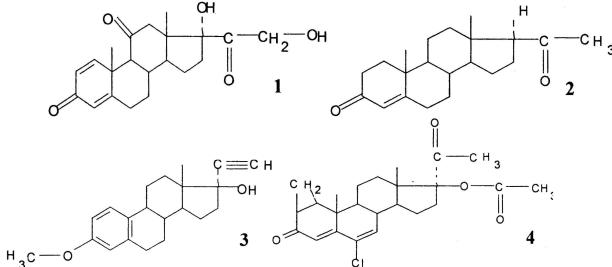
4.К производным андростана относится:
54
5.Сочленение колец стеранового цикла стероидных гормонов:
1)АВ-транс, ВС-цис, СД-транс;
2)АВ-цис, ВС-транс, СД-транс;
3)все – цис;
4)все – транс.
6.5α-стероиды обладают специфической гормональной активностью:
1)верно;
2)неверно.
7.Циклогексановый скелет АВС природных стероидов имеет конформацию:
1)ванны;
2)кресла;
3)полукресла;
4)конверта.
8.Введение этинильной группы в 17α-положение тестостерона:
1)усиливает андрогенную активность;
2)приводит к появлению антиандрогенной активности;
3)приводит к появлению гестагенной активности;
4)усиливает анаболическую активность;
5)приводит к появлению пролонгированного эффекта действия.
9.Образование ацетонидов глюкокортикоидов:
1)повышает глюкокортикоидную активность;
2)снижает резорбтивное действие при местном применении;
3)приводит к получению водорастворимого соединения;
55