Материал: Melnuchuk_Promuslova biotexnologij

РОЗДІЛ 5. ПРИНЦИПИ ТА МЕТОДИ ОТРИМАННЯ ПРОМИСЛОВИХ ШТАМІВ ПРОДУЦЕНТІВ
кількості в порівнянні з плоскою поверхнею, а значить, підвищити чутливість аналізу. В якості носія для осередків використовуються звичайні предметні скла, тобто тверді, непористі підкладки.
ДНК-проби - штучно синтезовані олігонуклеотиди, що складаються зазвичай з 15 - 20 основ. Кожна з таких проб повністю відповідає (комплементарна) ділянці гена одного певного мікроорганізму чи вірусу, що і дозволяє проводити їх ідентифікацію. Чим більше таких проб на біочіпі, тим більший спектр мікроорганізмів або функцій можна проаналізувати на їх наявність або відсутність у зразку.
Для здійснення аналізу на мікрочіпі НК, що міститься в досліджуваному зразку, повинна бути відповідним чином підготовлена. У разі аналізу геномної ДНК застосовують підхід ПЛР (полімеразна ланцюгова реакція) для того, щоб збільшити вміст в зразку даного дослідника фрагмента ДНК. Якщо ж для аналізу вибирається РНК, зазвичай застосовують зворотну транскрипцію з наступною ампліфікацією (ЗТ-ПЛР). При цьому праймери, використовувані в ПЛР, «несуть мітку (частіше флуоресцентну), що дозволяє повністю позначити всі утворювані ДНК-мішені. Альтернативним підходом є фарбування ДНК після ПЛР спеціальними барвниками. В даний час є можливість готувати чіпи з різнокольоровими флуоресцентними барвниками.
Після підготовки досліджуваного матеріалу необхідно провести гібридизацію ДНК-мішеней з пробами, іммобілізованими на мікрочіпі. Процес гібридизації проводять у гібридизаційній камері. Час інкубації, температуру і вологість в камерах підбирають експериментально, здійснюючи процес при кімнатній або при підвищеній температурі, наприклад при 62 ºС, з формамідом або без і т.д. Причому реакція йде лише з тими пробами, які відповідають присутній у зразку НК. Після закінчення цього часу препарат промивають і далі спостерігають світіння. Оскільки НК, що містяться у зразку, «перекладені» в форму порівняно коротких ДНК-мішеней, несучих флуоресцентну мітку, осередки, де пройшла реакція, починають світитися. Досліднику залишається лише врахувати, які клітинки засвітилися, і зробити висновок про наявність у зразку тих або інших мікроорганізмів або вірусів. При аналізі (візуальному під флуоресцентним мікроскопом або після мікросканування і використання відповідної програми - імідж-аналізу) будуть виявляться ті свічені мікроплями, де відбулося зв'язування мішені з пробою. Сигнали розглядають як значущі, якщо їх світіння перевищує певний пороговий рівень, який встановлюється в попередніх експериментах.
Для виготовлення біологічних мікрочіпів повинна бути проведена велика підготовча робота. Спочатку формулюється завдання дослідження, окреслюється спектр об'єктів, ідентифікація яких представляє інтерес. Після цього проводиться вибір генетичних мішеней - ділянок всередині геномів мікроорганізмів, послідовності яких характерні лише для
101

РОЗДІЛ 5. ПРИНЦИПИ ТА МЕТОДИ ОТРИМАННЯ ПРОМИСЛОВИХ ШТАМІВ ПРОДУЦЕНТІВ
представників того чи іншого виду або роду. Можна обрати найбільш консервативні послідовності в генах, відповідальних за синтез, наприклад 16S - 18S або 23S-28S рДНК і, отже, відповідно в майбутньому виготовлений чіп буде розпізнавати певну філогенетичну групу мікроорганізмів, тому його можна назвати «філочіпом». Можна обрати послідовності, які характеризують певний організм за його деякими, цікавлячими дослідника функціями, наприклад по гену, відповідальному за синтез верогоксіна у бактерії Е. coli 0157: Н7. Тоді виготовлений чіп слід називати «функціональним».
Вибрані нуклеотидні послідовності в подальшому використовуються для конструювання праймерів. Основна вимога до праймерів, - їх специфічність тільки до представників одного таксона (виду або роду). Для перевірки такої специфічності проводять так званий BLAST-аналіз, тобто порівняння певних послідовностей з послідовностями інших мікроорганізмів і вірусів. Якщо виявляється гомологія обраного праймера з ділянками геномів інших організмів, такий праймер бракується і процес вибору повторюється.
Після цього здійснюють синтез праймерів, введення в них флуоресцентної мітки, а також синтез проб для іммобілізації.
Олігонуклеотидні проби зазвичай мають такі характеристики, як назва (умовна, дається розробником), специфічність, наприклад універсальна (тобто для всіх бактерій), або групоспецифічна (наприклад, для α-підгрупи протеобактерій), або функціонально-специфічна і т.д., сіквенс проби в напрямку від 5'-до 3'-кінця, 16S рРНК зв'язує сайт (зазвичай місцеположення вказується по місцезнаходженню в гені 16S РНК Е. coli), процентний склад ГЦ-проби, а також номер невідповідності з мішенню, в тому випадку якщо така невідповідність є.
Подальший етап підготовки мікрочіпа - імобілізація синтезованих ДНК-проб, по завершенні якої чіп формально можна вважати готовим. Однак з цього моменту дослідник приступає до його тестування, після чого можуть бути змінені послідовності проб, схема підготовки матеріалу, умови проведення гібридизації, тобто формується остаточний варіант методу аналізу.
За допомогою технології мікрочіпів, за наявності готових чіпів і відповідного обладнання, кваліфікований фахівець може провести аналіз досить великої кількості зразків всього лише протягом декількох годин.
102

РОЗДІЛ 5. ПРИНЦИПИ ТА МЕТОДИ ОТРИМАННЯ ПРОМИСЛОВИХ ШТАМІВ ПРОДУЦЕНТІВ
5.2. Визначення чутливості мікроорганізмів до антибіотичних речовин
Метод агарових блоків
1.Після застигання агару продуцент антибіотичних речовин висівають суцільним газоном. Для цього спори актиноміцетів переносять петлею на агарову пластинку, розподіляють по всій поверхні шпателем і витримують у термостаті при 28 - 30°С протягом 8-10 діб.
2.Потім стерильним пробочним свердлом (діаметр 6-8 мм) вирізують агарові блоки з газоном актиноміцетів і переносять їх на поверхню агаризованого середовища, наприклад МПА, засіяного тест-організмом. Агарові блоки розкладають за шаблоном на рівній відстані один від іншого
іна відстані 1,5 - 2,0 см від краю чашки міцелієм вгору і щільно притискають до агарової пластинки. Для кращої дифузії антибіотичних речовин в товщу поживного середовища, засіяного тест-організмом, блоки можна розкладати безпосередньо в лунки, попередньо вирізані тим же свердлом. На одній чашці Петрі з тест-організмом можна розмістити 4-5 агарових блоків з різними продуцентами антибіотиків.
3.Чашки витримують 1 год. при кімнатній температурі для дифузії антибіотичних речовин в товщу агару, потім поміщають в термостат при температурі, сприятливій для розвитку тест-організму на добу і більше в залежності від швидкості його росту.
4.Якщо тест-організм чутливий до антибіотичних речовин продуцента, то після інкубації навколо агарових блоків утворюються зони відсутності його росту. Чим більше виділяється антибіотика і чим він активніший, тим більше буде діаметр зони відсутності росту тесторганізму. Тест-організм, не чутливий до антибіотичних речовин даного продуцента, росте по всій поверхні середовища, біля блоку продуцента.
Метод паперових дисків
Чутливість мікроорганізмів до антибіотиків зручно визначати за допомогою готових паперових дисків, просочених певними антибіотиками. Концентрація антибіотиків у дисках підібрана з таким розрахунком, щоб діаметри зон затримки росту стандартних тест-організмів становили 28 -
32мм.
1.Досліджувані мікроорганізми вирощують на відповідному щільному живильному середовищі.
2.Готують однорідну суспензію клітин у стерильній водопровідній воді. В 1 мл суспензії повинно міститися близько 2 млрд. клітин (визначають за стандартом мутності).
3.Вносять 1 мл суспензії в пробірку з 20 мл стерильного розплавленого і остудженого до 50°С агаризованого середовища,
103

РОЗДІЛ 5. ПРИНЦИПИ ТА МЕТОДИ ОТРИМАННЯ ПРОМИСЛОВИХ ШТАМІВ ПРОДУЦЕНТІВ
наприклад МПА. Якщо мікроорганізми вирощували в рідкому живильному середовищі, то в агар вносять відповідний обсяг культури.
4.Вміст пробірки швидко і ретельно перемішують і виливають у стерильну чашку Петрі. Коли середовище застигне, на його поверхню поміщають паперові диски на рівній відстані один від одного і на 1,5 - 2,0 см від краю чашки.
5.Чашки витримують 2 год. при кімнатній температурі для кращої дифузії антибіотиків у товщу агаризованого середовища, а потім 24
год. при 28 – 30°С.
6.Якщо досліджувані мікроорганізми чутливі до даних антибіотиків, то навколо дисків утворюються зони відсутності росту. Діаметр зони вимірюють міліметровою лінійкою. Зона більше 30 мм свідчить про високу чутливість мікроорганізму до антибіотика, а менше 12
мм- про слабку чутливість.
При наявності розчинів антибіотичних речовин або культуральних рідин, що містять антибіотик, використовують метод із застосуванням лунок в товщі агару. У цьому випадку в застиглому агаризованому середовищі, засіяному випробуваним мікроорганізмом, стерильним пробочним свердлом (діаметр 6 - 8 мм) роблять лунки на відстані 1,5 - 2,0 см від краю чашки. В лунки вносять розчини антибіотиків або культуральну рідину. Цей метод дозволяє також виявити здатність до утворення антибіотичних речовин мікроорганізмами, вирощеними в рідкому середовищі.
Робота № 20. Визначення антагоністичної активності штамів
Для виявлення мікробів-антагоністів і вивчення їх антибіотичної активності існують різні методи. Багато з них засновані на здатності антибіотиків дифундувати в щільних середовищах. Метод агарових блоків полягає в наступному: поверхня живильного середовища, придатного для розвитку випробуваного організму і утворення антибіотичної речовини, засівається суцільним «газоном» антагоніста (рис.31).
Після того, як мікроорганізми утворять колонії, у кінці експоненціальної фази почне утворюватись антибіотична речовина, яка дифундує в товщу агару (для бактерій - 4-5 діб, для грибів - 6-8 діб, для актиноміцетів - 8-10 діб). Після цього стерильним пробочним свердлом вирізають агарові блочки і переносять їх на поверхню іншої агарової пластинки в чашці Петрі, попередньо засіяної тест-організмом. Після інкубації в термостаті (час інкубації залежить від швидкості росту тесткультури) навколо агарових блоків утворюються зони відсутності росту
104
РОЗДІЛ 5. ПРИНЦИПИ ТА МЕТОДИ ОТРИМАННЯ ПРОМИСЛОВИХ ШТАМІВ ПРОДУЦЕНТІВ
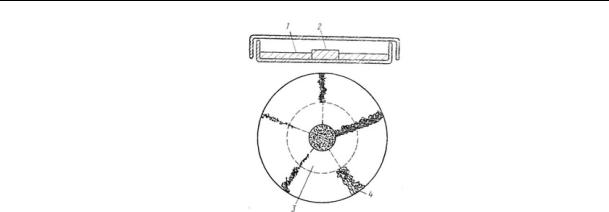
Рис. 31. Визначення антагоністичної активності мікроорганізмів - антагоністів:
1 – середовище для розвитку тест-організму; 2 – агаровий блок з антагоністом; 3 – зона дифузії антибіотику; 4 – штрих тест-організму.
тест-організму, якщо антибіотичну речовину, що виділяється досліджуваним організмом, пригнічує ріст тест-мікроорганізма. За діаметром зон встановлюють антибіотичну активність досліджуваного мікроорганізму.
Мета роботи: дослідити антагоністичні відношення між різними групами мікроорганізмів, виділених з грунту. Дослідити антагоністичні властивості тест-культур.
Обладнання та матеріали: чисті культури мікроорганізмів-антагоністів – Ваcillus subtillis та ін. Чисті культури бактерій в пробірках або чашках Петрі з МПА, бактеріологічні петлі, спиртівки, стерильні пробірки, предметні скла, чашки Петрі з МПА, термостат.
Хід виконання роботи
1.З агаризованого середовища з культурою актиноміцетів вирізати пробковим свердлом блок і перенести його (культурою догори) у центр іншої чашки Петрі з агаризованим середовищем;
2.Радіальними штрихами до агарового блоку (колонії-антагоніста)
підсіяти суспензії тест-культур. Штрих починати від центру до периферії чашки.
3. Інкубувати посіви при температурі 37°С протягом 24 год. Через 24 год. виміряйте діаметр зони затримки росту культури навколо кожного диска з антибіотиком і визначте ступінь чутливості культури за наступними критеріями:
а) діаметр зони затримки росту більше 25 мм - культура високочутлива; б) від 15 до 25 - чутлива;
в) від 10 до 14 - малочутлива; г) менше 10 мм і повна відсутність - стійка.
4. Результати оформіть у вигляді табл. 15.
105