Материал: Melnuchuk_Promuslova biotexnologij

РОЗДІЛ 5. ПРИНЦИПИ ТА МЕТОДИ ОТРИМАННЯ ПРОМИСЛОВИХ ШТАМІВ ПРОДУЦЕНТІВ
супроводжується появою запаху, пігментацією середовища, виділенням газу.
3.Крохмаль-йодна реакція на нітрити заснована на тому, що нітрити в кислому середовищі окислюють йодистий цинк з виділенням йоду, присутність якого виявляють за допомогою крохмалю. Для проведення реакції до краплі культуральної рідини додають краплю розчину, що
містить ZnCI2, KI і крохмаль, і краплю розчину НСl. При наявності в середовищі нітритів з'являється синє забарвлення.
4.Протеолітична активність визначається наявністю ферментів (протеази), які каталізують розщеплення білків на полі-і олігопептиди. Протеази виділяються різними видами бацил, актиноміцетів, міцеліальних грибів та іншими мікроорганізмами. Активність позаклітинних протеаз визначають, використовуючи як субстрат желатину, казеїн або інші білки.
5. Визначення чутливості мікроорганізмів до антибіотичних речовин.
Чутливість мікроорганізмів до антибіотиків зручно визначати за допомогою паперових дисків, просочених певними антибіотиками. Концентрація антибіотиків в дисках підібрана з таким розрахунком, щоб діаметри затримки росту стандартних тест-організмів були 28 - 32 мм. Якщо досліджувані мікроорганізми чутливі до даних антибіотиків, то навколо дисків утворюються зони відсутності росту. Діаметр зони вимірюють міліметровою лінійкою. Зона більше 30 мм свідчить про високу чутливість мікроорганізму до антибіотика, а менше 12 мм - про слабку чутливість.
На сьогодні актиноміцети є одними з найважливіших об’єктів сучасної генетики та промислової біотехнології. Дві третини антибіотиків є метаболітами актиноміцетів, 80% із яких синтезують представники роду Streptomyces. Ці бактерії активно вивчаються на предмет генетичного контролю біосинтезу антибіотиків, що сприяє активному розвиткові методів генетичної інженерії та селекції їх продуцентів. Актиноміцети родів Nocardia є продуцентами нокардіоміцину, ріфаміцину (некласичні β- лактамні антибіотики), Streptomyces griseus – стрептоміцину (аміноглікозидний антибіотик), протеолітичних ферментів. S. antibioticus – олеандоміцину (макролідний антибіотик), протипухлинних хіміотерапевтичних препаратів. S. aureofaciens – тетрациклінових антибіотиків, вітамінів групи В; S. olivaceus – β-лактамних антибіотиків, вітамінів групи В; Saccharopolispora erythreae – еритроміцину (макролідний антибіотик); Micromonospora purpurea – гентаміцину (аміноглікозидний антибіотик); M. olivoasterospora – фортицину (аміноглікозидний антибіотик) (Див.Додатки).
Мета роботи:
1. Приготувати та розглянути препарат-відбиток Streptomyces griseus.
76
РОЗДІЛ 5. ПРИНЦИПИ ТА МЕТОДИ ОТРИМАННЯ ПРОМИСЛОВИХ ШТАМІВ ПРОДУЦЕНТІВ
2.Розглянути морфологію колоній та будову конідієносців грибів
(Aspergillus niger, Penicillium notatum та Mucor nigricans) у препараті роздавлена крапля.
3.Дослідити морфологію Saccharomyces cerevisiae та Candida albicans у
фіксованих та фарбованих препаратах.
4.Досліджувані препарати замалювати в альбомах.
Матеріали та обладнання: Голки препарувальні, ланцети, предметні скельця, покривні скельця, мікроскопи, розчин метиленової синьки, суміш спирт + гліцерин + метиленова синька.
Культури мікроорганізмів: Streptomyces griseus, Aspergillus niger, Penicillium notatum, Mucor nigricans, Saccharomyces cerevisiae, Candida albicans.
Хід роботи:
1.Приготувати препарат-відбиток актиноміцетів.
-Скальпелем вирізати невеликий фрагмент агаризованого середовища з колонією актиноміцетів.
-Перенести цей блок на предметне скло (колонією донизу!) і злегка притиснути. Блок зняти, а відбиток підсушити на повітрі.
-Наступні етапи виготовлення препарату, як для фіксованого забарвленого мазка (зафіксувати над полум’ям пальника, фарбувати фуксином 2-3 хв., промити водою, висушити).
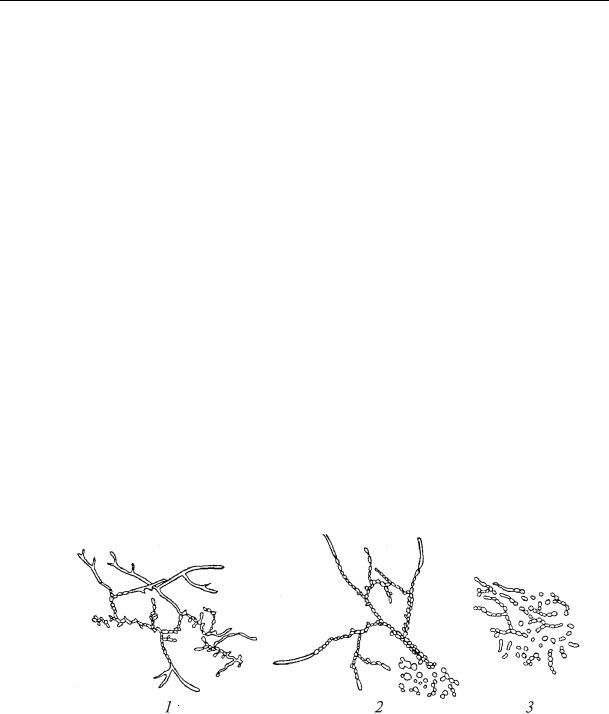
-Розглянути з імерсією. Замалювати (рис.26).
Рис. 26. Культура актиноміцетів після розвитку протягом, днів: 1- 2; 2 – 4-5; 3 – 7-8.
2.Виготовити препарат роздавлена крапля для дослідження будови конідієносців грибів.
-На предметне скло нанести краплину суміші “спирт + гліцерин + метиленовий синій”.
-Обережно, за допомогою двох препарувальних голок перенести частину повітряного міцелію у краплину суміші й розправити його.
77
РОЗДІЛ 5. ПРИНЦИПИ ТА МЕТОДИ ОТРИМАННЯ ПРОМИСЛОВИХ ШТАМІВ ПРОДУЦЕНТІВ
-Накрити покривним скельцем і розглядати з об’єктивом 40х. Замалювати (рис.27).
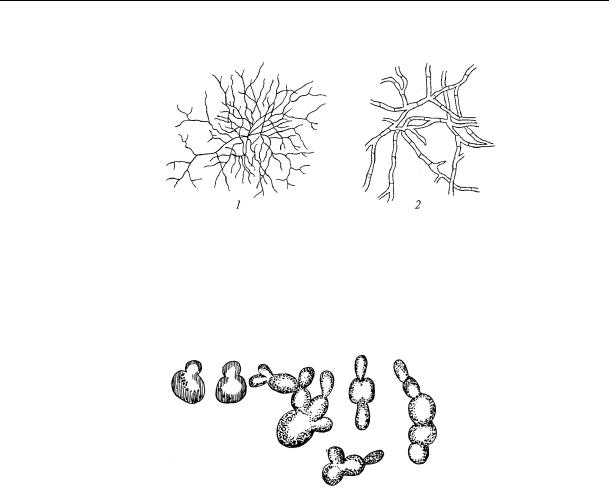
Рис. 27. Міцелій актиноміцетів (1) та грибів(2) при однаковому збільшенні
3.Для дослідження морфології дріжджів виготовити фіксований та забарвлений препарат (фарбують розчином метиленового синього). Звертають увагу на клітини із бруньками. Замалювати (рис.28).
Рис. 28. Клітини дріжджів Saccharomyces cerevisiae
Контрольні питання:
1.Назвіть типові ознаки актиноміцетів.
2.Як можуть розмножуватись актиноміцети?
3.В чому полягає практичне значення актиноміцетів?
4.Особливості морфологічної будови дріжджів.
5.Охарактеризуйте типи розмноження дріжджів.
6.Опишіть морфологічні особливості мукорових, пеніцилів та аспергилів.
7.Практичне значення цвільових грибів, дріжджів та дріжджеподібних грибів.
Лабораторна робота № 17. Визначення біохімічних властивостей
Bacillus subtilis
Визначення здатності синтезувати цільовий продукт - головний критерій при відборі продуцентів. Мікроорганізми повинні відповідати наступним вимогам:
1)володіти високою швидкістю росту;
2)використовувати для життєдіяльності дешеві субстрати;
3)бути стійкими до зараження сторонньою мікрофлорою.
78

РОЗДІЛ 5. ПРИНЦИПИ ТА МЕТОДИ ОТРИМАННЯ ПРОМИСЛОВИХ ШТАМІВ ПРОДУЦЕНТІВ
Мета роботи. Освоїти методики проведення біохімічних тестів для визначення ферментативних властивостей та ідентифікації бактерій. Матеріали та обладнання. Чиста культура Bacillus subtilis в чашках Петрі з МПА, бактеріологічні петлі, спиртівки, стерильні пробірки, предметні скельця, перекис водню, середовища з моно-, ди-, полісахаридами і спиртами, що містять індикатори; пробірки з МПБ; пробірки з 2 - 3%-ною пептонною водою; розчини цистину і цистеїну, лакмусовий папір; стерильний фізіологічний розчин, термостат з температурою 37°С.
Хід виконання роботи
1.Розлийте стерильний фізіологічний розчин в стерильні пробірки по 0,3 мл (по дві пробірки на один тест: одна контрольна, інкубується без бактерій, а друга - дослідна), внесіть в ряд дослідних пробірок однакову кількість (одна петля агарової культури або 0,1 мл бульйонної культури) досліджуваної культури бактерій.
2.Відповідно до інструкції внесіть в пробірки паперові диски тестів та інкубуйте пробірки при температурі 37°С. 3. Засійте чисту культуру досліджуваних бактерій бактеріологічною петлею на середовища з моно-, ди- , полісахаридами та спиртами, наданих викладачем, і інкубуйте їх протягом
18-24 год. при температурі 37°С.
4.Для визначення каталазної активності на предметне скло нанесіть краплю 3%-ного розчину перекису водню, внесіть в неї петлю досліджуваної агарової або бульйонної культури бактерій і ретельно перемішайте. При позитивній реакції (наявності каталази) перекис водню буде розкладатися з утворенням води і кисню в вигляді бульбашок.
5.Через 24 год. уважно перегляньте всі контрольні та дослідні пробірки з тестами і посіви на середовища з цукрами і спиртами. Результати визначення ферментативних властивостей Bacillus subtilis оформити у вигляді табл. 12.
Ідентифікація мікроорганізмів базується на вивченні морфологічних, цитологічних, культуральних і фізіолого-біохімічних властивостей. У роботі з ідентифікації мікроорганізмів необхідно дотримуватись наступних правил: використовувати чисті культури, застосовувати при вивченні стандартні методи, використовувати для інокуляції діагностичних середовищ культури, що знаходяться в активному фізіологічному стані.
|
Ферментативні властивості Bacillus subtilis |
|
Таблиця 12 |
|||||||
|
|
|
|
|||||||
Сахаролітичні властивості |
|
Протеолітичні властивості |
|
Наявність |
||||||
|
|
|
|
|
|
|
|
|
|
каталази |
Глюкоза |
Лактоза |
Манніт |
|
Сорбіт |
Індол |
Н2S |
|
NH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
79

РОЗДІЛ 5. ПРИНЦИПИ ТА МЕТОДИ ОТРИМАННЯ ПРОМИСЛОВИХ ШТАМІВ ПРОДУЦЕНТІВ
Лабораторна робота № 18. Ідентифікація мікроорганізмів за визначником бактерій Берджі
До останнього часу систематика мікроорганізмів базувалася переважно на фенотипових ознаках: морфологічних, фізіологічних, біохімічних та ін., тому існуючі системи класифікації носять значною мірою штучний характер. Однак вони дозволяють порівняно легко ідентифікувати деякі знову виділені види та штами мікроорганізмів (вид - сукупність особин, що характеризуються низкою спільних морфологічних, фізіолого-біохімічних, молекулярно-генетичних ознак; під терміном «штам» розуміють чисту культуру мікроорганізмів, виділену з певного місця проживання (води, ґрунту, організму тварини і т.д.). Різні штами одного виду мікроорганізмів можуть відрізнятися за деякими ознаками, наприклад чутливості до антибіотиків, здатності синтезувати деякі продукти метаболізму і т.д., але ці відмінності менші, ніж видові.
Вивчення генотипу мікроорганізмів стало можливим в результаті успішного розвитку молекулярної біології і призвело до виникнення геносистематики. Дослідження генотипу, засноване на аналізі нуклеїнових кислот, в принципі дає можливість побудувати з часом природну (філогенетичну) систему мікроорганізмів. Філогенетичні взаємини бактерій оцінюють визначенням молярного вмісту ГЦ в ДНК, методами ДНК-ДНК і ДНК-рРНК-гібридизації, за допомогою ДНК-зондів, а також вивченням послідовності нуклеотидів в 5S, 16S і 23SрРНК.
Визначення молярного вмісту ГЦ від загальної кількості основ ДНК у прокаріотів, як уже вказувалося, коливається від 25 до 75%. Кожен вид бактерій має ДНК з характерним середнім вмістом ГЦ. Однак оскільки генетичний код вироджений, а генетичне кодування грунтується не тільки на змісті нуклеотидних основ в одиницях кодування (триплети), але і на взаємному розміщенні, то однаковий середній вміст ГЦ в ДНК двох видів бактерій може супроводжуватись їх значним генотиповим поділом. Якщо два організми дуже близькі за нуклеотидним складом, це може бути свідченням їх еволюційної спорідненості тільки за умови, що вони володіють великим числом загальних фенотипових ознак або генетичною схожістю, підтвердженою іншими методами. У той же час розбіжність (більше 10-15%) в нуклеотидному складі ДНК двох штамів бактерій з загальними фенотиповими властивостями показує, що вони відносяться до різних видів.
Метод ДНК-ДНК-гібридизації є більш важливим для оцінки генетичної спорідненості бактерій. При ретельному проведенні експериментів можна отримати цікаву інформацію про ступінь їх генетичної гомології. Усередині одного виду бактерій ступінь генетичної гомології штамів досягає 70 - 100%. Однак якщо в результаті еволюційної дивергенції послідовності нуклеотидних основ геномів двох бактерій
80