Материал: 3292596

Обмен билирубина у здоровых новорожденных
Источники и механизм образования билирубина
Основным источником образования свободного билирубина в организме как взрослого человека, так и новорожденного является гемоглобин (Hb) эритроцитов, стареющих и разрушающихся в клетках мононуклеарно-фагоцитарной системы организма (преимущественно в печени и селезенке). Продолжительность жизни эритроцитов у взрослого человека составляет 110–120 дней, у доношенного новорожденного — 80–90 дней, а у недоношенного, в зависимости от гестационного возраста, колеблется в пределах 40–70 дней.
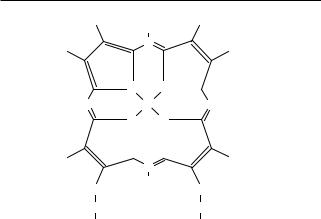
Гемоглобин входит в состав группы белков гемопротеинов, которые являются подвидом хромопротеинов и подразделяются на неферментативные белки (гемоглобин, миоглобин) и ферменты (цитохромы, каталазу, пероксидазу). Небелковой частью этих сложных молекул является гем — структура, включающая порфириновое кольцо (состоящее из четырех пиррольных колец) и ион Fe2+ (рис. 1). Железо связывается с порфириновым кольцом двумя координационными и двумя ковалентными связями.
Гемоглобин представляет собой белок, включающий четыре гемсодержащие белковые субъединицы.
20  ОБМЕН БИЛИРУБИНА У ЗДОРОВЫХ НОВОРОЖДЕННЫХ
ОБМЕН БИЛИРУБИНА У ЗДОРОВЫХ НОВОРОЖДЕННЫХ
|
CH=CH |
2 |
CH |
3 |
|
|
|
H |
|
||
|
|
|
|
|
|
H |
C |
|
C |
CH=CH |
|
|
|
2 |
|||
3 |
|
|
|
|
NN 
HC |
Fe2+ |
CH |
NN
H3C |
|
CH3 |
|
|
|||
|
|
C |
|
|
CH2 |
H |
|
|
|
CH2 |
|
|
CH2 |
|
CH2 |
COOH |
|
COOH |
|
|
|
Гем |
|
Рис. 1. Химическое строение гема
Между собой протомеры соединяются гидрофобными, ионными, водородными связями. При этом они взаимодействуют не произвольно, а определенным участком — контактной поверхностью. Контакт происходит одновременно в десятках точек по принципу комплементарности. Взаимодействие осуществляют разноименно заряженные группы, гидрофобные участки, неровности на поверхности белка (рис. 2 на цветной вклейке).
Белковые субъединицы в нормальном гемоглобине могут быть представлены различными типами полипептидных цепей: α, β, γ, δ, ε, ξ (соответственно альфа, бета, гамма, дельта, эпсилон, кси). В состав молекулы гемоглобина входят по две цепи двух разных типов.
Гем соединяется с белковой субъединицей, вопервых, через остаток гистидина координационной связью железа, во-вторых, через гидрофобные связи пиррольных колец и гидрофобных аминокислот.

ИСТОЧНИКИ И МЕХАНИЗМ ОБРАЗОВАНИЯ БИЛИРУБИНА  21
21
Гем располагается как бы в кармане своей цепи, и формируется гемсодержащий протомер.
Существует несколько нормальных вариантов гемоглобина:
•HbР — примитивный гемоглобин, содержит 2ξ- и 2ε-цепи, встречается в эмбрионе между 7–12-й неделями;
•HbF — фетальный гемоглобин, содержит 2α- и 2γ-цепи, появляется через 12 нед внутриутробного развития и является основным после 3 мес;
•HbA — гемоглобин взрослых, доля составляет 98%, содержит 2α- и 2β-цепи, у плода появляется через 3 мес и к рождению составляет 80% всего гемоглобина;
•HbA2 — гемоглобин взрослых, доля составляет 2%, содержит 2α- и 2δ-цепи;
•HbO2 — оксигемоглобин, образуется при связывании гемоглобина с кислородом в легких, в легочных венах его 94–98% всего количества гемоглобина;
•HbCO2 — карбогемоглобин, образуется при свя-
зывании гемоглобина с углекислым газом в тканях, в венозной крови составляет 15–20% всего количества гемоглобина.
Гемоглобин A содержит четыре полипептидные цепи (2α и 2β), каждая из них состоит из 146 аминокислотных остатков. Вся молекула белковой части гемоглобина включает 574 аминокислоты. Фетальный гемоглобин состоит также из четырех полипептидных цепей (2α и 2γ), но отличается от гемоглобина взрослого человека как составом аминокислот, так и физико-химическими свойствами. Важно отметить что гем одинаков не только у всех видов гемоглобина, но и является простетической группой миоглобина и железосодержащих ферментов.
Образование билирубина. За счет биохимической трансформации гемоглобина стареющих эритро-

22  ОБМЕН БИЛИРУБИНА У ЗДОРОВЫХ НОВОРОЖДЕННЫХ
ОБМЕН БИЛИРУБИНА У ЗДОРОВЫХ НОВОРОЖДЕННЫХ
цитов в организме образуется 75–80% свободного билирубина. Остальные 20–25% образуются в результате разрушения незрелых форм эритроцитов непосредственно в костном мозге, а также из гемовой части железосодержащих ферментов (цитохрома Р-450, каталазы, пероксидазы) и миоглобина.
В одном эритроците содержится примерно 340 млн молекул гемоглобина. В крови взрослого человека в среднем содержится около 750 г гемоглобина. В течение суток у взрослых из 1 г гемоглобина образуется 34 мг билирубина, еще 1 мг билирубина образуется из негемовых источников. Средняя скорость образования билирубина у взрослых составляет около 4–5 мг/кг в сутки. У новорожденных скорость образования билирубина значительно выше и составляет 8–10 мг/кг в сутки. Более высокая скорость у новорожденных связана с относительно большим количеством эритроцитов, циркулирующих в крови, и более короткой продолжительностью их жизни.
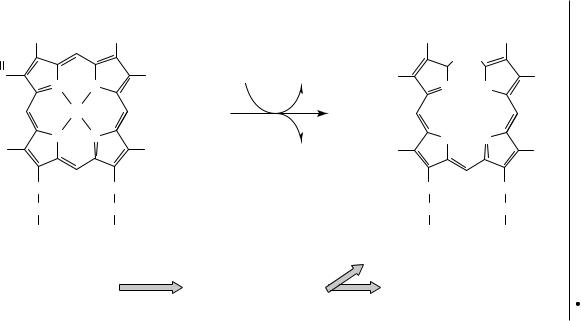
Процесс разрушения гема происходит преимущественно по месту α-метиновой связи при участии микросомального фермента — гемоксидазы. В результате последовательных окислительных реакций вначале образуется вердоглобин, а затем биливердин (рис. 3).
На стадии образования биливердина происходит отщепление глобина и атома железа (Fe2+), которые используются для ресинтеза нового гема, а биливердин при участии фермента биливердинредуктазы и аденозинтрифосфата превращается в билирубин IXα (рис. 4).
Пространственная структура молекулы билирубина такова, что полярные группировки обращены внутрь и образуют стабилизирующие внутренние водородные связи. В результате билирубин плохо растворим в воде за счет отталкивания ее молекул гидрофобными группами молекулы билирубина.
80% из гемоглобина
CH3 |
HC=CH2 |
CH2 |
|
HC |
CH3 |
N |
N |
|
Fe2+ |
NN
H3C |
CH3 |
CH2 CH2
CH2 CH2
COOH COOH
Гем
Гем
|
|
|
|
|
CH2 |
||||
O |
2 |
+ НАДФН |
2 |
Н |
O + НАДФ+ |
|
|
|
|
|
|
||||||||
|
|
2 |
HC |
||||||
CO2+Fe3+ H3C
Гемоксигеназа
Fe2+
Вердоглобин
CH3 HC=CH2 OH HO
N |
CH3 |
HN |
|
NH |
N |
|
CH3 |
CH2 |
CH2 |
CH2 |
CH2 |
COOH |
COOH |
Биливердин
Биливердин
Рис. 3. Схема образования биливердина
23 БИЛИРУБИНА ОБРАЗОВАНИЯ МЕХАНИЗМ И ИСТОЧНИКИ