Материал: 2018_02_15_01
Зависимость повышения температуры кипения (∆Ткип) разбавленного
раствора от моляльной концентрации m выражается уравнением: |
|
∆Ткип = Т – То = Кэ ∙ m , |
(4.2) |
где То, Т – температуры кипения растворителя и раствора; |
Кэ – |
эбулиоскопическая постоянная, зависящая от свойств растворителя. |
|
Зависимость понижения температуры замерзания (∆Тз.) разбавленного
раствора от моляльной концентрации m выражается уравнением: |
|
∆Тз = Тзо – Т = Ккр.∙ m , |
(4.3) |
где Тоз, Т – температура замерзания растворителя и раствора; |
|
Ккр – криоскопическая постоянная, зависящая от свойств растворителя.
Криоскопическую постоянную можно рассчитать по уравнению
|
·T2 |
|
|
Ккр= |
пл |
, |
(4.4) |
1000∙ |
|||
|
пл |
|
|
где Тпл - температура плавления чистого растворителя; lпл – удельная теплота плавления растворителя.
Эбулиоскопическую постоянную можно рассчитать по аналогичному
уравнению:
Кэ= |
·Tн2.т.к |
, |
(4.5) |
|
1000∙ |
||||
|
|
|
||
|
исп |
|
|
где Тн.т.к – нормальная температура кипения чистого растворителя; lисп.-
удельная теплота испарения растворителя.
Зависимость осмотического давления от молярной концентрации
раствора (закон Вант-Гоффа) описывается уравнением: |
|
π = с∙R·T, |
(4.6) |
где π – осмотическое давление;
с – молярная концентрация раствора, моль/л;
R – универсальная газовая постоянная;
T – температура раствора.
21
Задача 4.1
Дано:
При температуре Т = 149 К давление пара раствора концентрации
3 % неизвестного нелетучего вещества в жидком растворителе Р = 12420 Па; плотность этого раствора ρ = 1780 кг/м3. Зависимости давления насыщенного пара от температуры над жидким и твердым чистым растворителем приведены в задаче 3.1 (тема 3).
1)вычислите молекулярную массу растворенного вещества;
2)определите молярную и моляльную концентрации раствора;
3)вычислите осмотическое давление раствора;
4)постройте кривую Р = f (T) для данного раствора и растворителя;
5)определите графически температуру, при которой давление пара над чистым растворителем будет равно Р Па;
6)определите графически повышение температуры кипения при давлении Р раствора данной концентрации с;
7)вычислите эбулиоскопическую постоянную всеми возможными способами и сравните эти величины между собой при нормальной температуре кипения (Тн.т.к);
8)определите понижение температуры замерзания раствора;
9) вычислите криоскопическую постоянную.
Решение задачи 4.1
|
|
|
|
Таблица 4.1 |
|
Исходные данные для решения задачи 4.1 |
|
|
|||
|
|
|
|
|
|
Массовая доля |
Молярная |
|
|
|
|
нелетучего |
масса |
Р,Па |
Т,К |
ρ .10-м3 |
|
вещества, % |
растворителя |
|
|
|
|
|
|
|
|
|
|
3 |
68 |
12420 |
149 |
1,780 |
|
|
|
|
|
|
|
22
1. Согласно закону Рауля относительное понижение давления пара над растворителем прямо пропорционально мольной доле растворенного вещества:
∆ |
= |
|
в−ва |
|
, |
|
|
|
в−ва |
+ |
|
||
|
р |
|||||
0 |
|
|
|
|||
где ∆ - абсолютное понижение давления;
P0 - давление пара над чистым растворителем;
в−ва - количество молей растворенного вещества;
р - количество молей растворителя.
Вычислим мольную долю растворенного вещества:
в−ва |
= |
0 − |
= |
12663 − 12420 |
= 0,0192, |
||
|
+ |
|
12663 |
|
|||
|
|
|
|
||||
в−ва |
р |
|
0 |
|
|
|
|
где P – давление пара над раствором.
С другой стороны, мольная доля может быть вычислена по массовой доле:
|
|
|
|
|
|
|
|
|
|
|
|
|
= 0,0192, |
100 − |
+ |
|
||||
|
|
|
|
|||
|
|
|
|
|
||
где M – молярная масса растворенного вещества;
– масса растворенного вещества в 100 граммах;
– молярная масса растворителя.
Отсюда:
|
∙ |
1 |
|
|
|
68 ∙ 3 |
1 |
|
|
|
г |
||||||
= |
|
|
− 1) = |
|
|
|
|
|
− 1) = 107,4 |
|
. |
||||||
|
( |
|
|
( |
|
|
|
||||||||||
100 − |
0,0192 |
100 − 3 |
0,0192 |
моль |
|||||||||||||
2. Молярная концентрация раствора вычисляется следующим |
|||||||||||||||||
образом: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
10 ∙ ∙ |
|
10 ∙ 3 ∙ 1,78 |
|
|
моль |
||||||||
|
= |
|
= |
|
|
|
|
= 0,497 |
|
, |
|||||||
|
|
107,4 |
|
|
|
л |
|||||||||||
где ω – процентная массовая концентрация растворенного вещества.
23
Моляльная концентрация вычисляется следующим образом:
|
10 ∙ |
|
|
10 ∙ 3 |
|
моль |
|||||
= |
|
|
= |
|
|
|
|
= 0,288 |
|
. |
|
|
|
|
3 |
|
|
кг |
|||||
|
(1 − |
|
) ∙ |
|
(1 − |
|
) ∙ 107,4 |
|
|
|
|
|
100 |
|
|
|
|
||||||
|
|
100 |
|
|
|
||||||
3.Осмотическое давление раствора неэлектролита (π)
= с ∙ ∙ .
Рассчитаем осмотическое давление раствора при температуре 149 K
= с ∙ ∙ = 0,497 ∙ 103 ∙ 8,31 ∙ 149 = 6,15 ∙ 105 Па.
4.В нашей задаче давление над раствором будет следующим образом зависеть от давления над чистым растворителем P0:
= 0(1 − 0,0192) = 0,9808 ∙ .
Это следует из закона Рауля.
Таблица 4.2
Данные для построения графика функции P = f (T)
T,K |
P0 |
|
|
|
|
137 |
6665 |
6537,0 |
141 |
7331,5 |
7190,7 |
145 |
8664,5 |
8498,1 |
146 |
9997,5 |
9805,5 |
149 |
12663 |
12419,9 |
151,4 |
15996 |
15688,9 |
|
|
|
24
P,Па |
|
|
|
|
|
|
18000 |
|
|
|
|
|
|
16000 |
|
|
|
С |
В |
|
14000 |
|
|
|
|
|
|
12000 |
|
|
|
|
|
|
10000 |
|
|
|
|
|
|
8000 |
|
|
|
О |
|
|
6000 |
|
D |
|
|
|
|
|
|
|
|
|
|
|
4000 |
|
|
|
|
|
|
2000 |
A |
|
|
|
|
|
0 |
|
|
|
∆t |
∆t |
|
|
|
|
|
|
|
|
125 |
130 |
135 |
140 |
145 |
150 |
155 |
|
|
|
T,K |
|
|
|
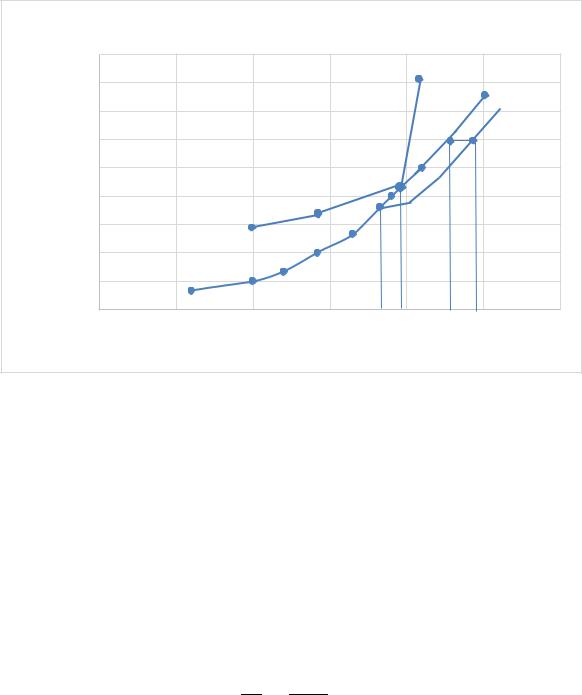
Рис. 4.1. Диаграмма состояния вещества – чистого растворителя А |
|
|||||
(рис. 3.2) с кривой испарения раствора |
|
|
|
|||
5. На графике (рис. 4.1) видно, |
что температура чистого растворителя, |
|||||
при которой давление пара составляет 12420 Па, равна 148,75 K. |
|
|||||
6.Определим графически увеличение температуры кипения:
= 149,0 − 147,0 = 2,0
7.Рассчитаем эбулиоскопическую константу по повышению температуры кипения:
= э
э = = 0,2882,0 = 6,94.
Эбулиоскопическая константа может быть вычислена также иным
образом: |
|
|
|
|
|
· |
2 |
∙ |
|
= |
кип |
|
, |
|
|
|
|
||
э |
1000 |
∙ |
исп |
|
|
||||
где MS – молярная масса растворителя в г/моль.
Из предыдущей задачи 3.1 известно, что = 19380 |
Дж |
. |
|
||
исп |
моль |
|
|
||
25