Материал: 2018_02_15_01
Таблица 3.2
К построению графика в координатах lg P от 1/T для твердого
состояния вещества
Т, К |
1/T·102 |
Р, Па |
lg P |
|
|
|
|
131 |
0,763 |
1333 |
3,125 |
135 |
0,741 |
1999,5 |
3,301 |
137 |
0,730 |
2666 |
3,426 |
139,2 |
0,718 |
3999 |
3,602 |
141,5 |
0,707 |
5332 |
3,727 |
144,0 |
0,694 |
7998 |
3,903 |
146 |
0,685 |
9997,5 |
4,000 |
|
|
|
|
Таблица 3.3
К построению графика в координатах lg P от 1/T для жидкого
состояния вещества
Т, К |
1/T∙102 |
Р, Па |
lg P |
|
|
|
|
137 |
0,730 |
6665 |
3,824 |
141 |
0,709 |
7331,5 |
3,865 |
145 |
0,690 |
8664,5 |
3,938 |
146 |
0,685 |
9997,5 |
4,000 |
149 |
0,671 |
12663 |
4,103 |
151,4 |
0,661 |
15996 |
4,204 |
|
|
|
|
1. Построим график в координатах lg P от 1/T, подготовив для
этого данные (табл. 3.2 и табл. 3.3).
16
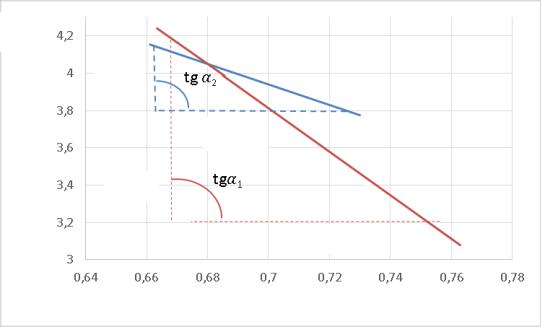
lg P
Y2
X2
Y1
X1
1/Т·10-2
Рис. 3.1. Зависимость графика в координатах lg P от 1/T
2. На графике положение тройной точки отмечено пунктиром (точка пересечения прямых).
Ее координаты: 1/T=0,694∙10-2, lg P = 4,02. Тогда: Tт.т=1/(0,694·10-2) = 144 K,
P= 104.02= 10471,29 Па.
3.Построим прямые на осях диаграммы и вычислим их параметры.
Сначала найдем наклон прямой, которая является границей между
жидким состоянием вещества и газообразным. Наклон прямой равен тангенсу угла а2 - отношению отрезков ∆ 1и ∆ 1:
tg |
2 |
= − |
∆ исп |
= |
∆ 1 |
= |
3,5−4,21 |
|
= −1014,2. |
|
|
2,3· |
∆ |
(0,73−0,66)∙10 |
−2 |
|
|
||||||
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
1 |
|
|
|
|
|
|
|
Отсюда теплота испарения: |
|
|
|
|
|
||||||
∆ исп = −2,303 ∙ ∙ 2 = −2,3 ∙ 8,31 ∙ (−887,5) = 19380 |
Дж |
. |
|||||||||
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
моль |
|
Найдем наклон прямой, которая является линией равновесия между
твердым состоянием вещества и газообразным. Наклон прямой равен тангенсу угла наклона a1 - отношению отрезков ∆ 2и ∆ 2:
tg a1 |
= − |
∆ возг |
= |
∆ 2 |
= |
3,2−4,2 |
= −1515,2. |
|
2,3· |
∆ |
(0,746−0,68)·10−2 |
||||||
|
|
|
|
|
||||
|
|
|
2 |
|
|
|
||
|
|
|
|
|
|
17 |
|
|
Отсюда теплота возгонки:
Дж
∆ возг = −2,3 · · = −2,3 · 8,31 · (−1515,2) = 28956 моль.
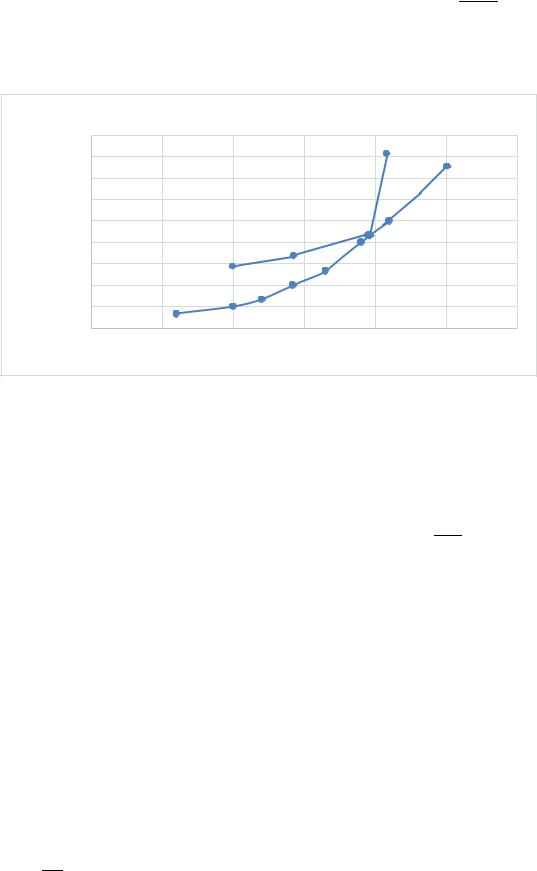
4. График зависимости давления насыщенного пара от температуры имеет следующий вид (рис. 3.2):
P,Па |
|
|
|
|
|
|
18000 |
|
|
|
|
|
|
16000 |
|
|
|
|
С |
В |
14000 |
|
|
|
|
|
|
|
|
|
|
|
|
|
12000 |
|
|
|
|
|
|
10000 |
|
|
|
|
|
|
8000 |
|
|
|
О |
|
|
6000 |
|
D |
|
|
|
|
4000 |
|
|
|
|
|
|
2000 |
A |
|
|
|
|
|
0 |
|
|
|
|
|
|
125 |
130 |
135 |
140 |
145 |
150 |
155 |
|
|
|
T,K |
|
|
|
Рис. 3.2. График зависимости давления насыщенного пара чистого вещества от температуры
5. Теплота плавления вещества при температуре тройной точки является разностью теплот возгонки и испарения этого вещества:
∆ пл = ∆ возг − ∆ исп = 28956 − 19380 = 9576 мольДж .
6. Из уравнения Клапейрона-Клаузиуса следует, что:
= ∆ пл ,·
где = |
1 |
− |
1 |
– разность молярных объемов фаз. |
|
|
|
||||
|
|
|
|||
|
ж |
|
тв |
|
Перед расчетом нам надо перевести теплоту плавления из Дж/моль в Дж/кг:
∆ пл = |
9576 |
1000 = 140823 |
Дж |
, |
68 |
|
|||
|
|
кг |
||
где 68 – молярная масса вещества.
Вычислим при температуре тройной точки:
18

|
= |
|
∆ пл |
|
|
|
= |
140823 |
|
|
= 1,224 ∙ 108 |
Па |
. |
|||||||||||
|
|
|
1 |
|
|
1 |
|
|
|
1 |
|
|
|
1 |
|
К |
||||||||
|
|
тр.т( ж− тв) 144∙(1434−1450) |
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|||||||||||||||||
Отсюда: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
= |
|
1 |
|
|
|
= 8,17 · 10−9 |
|
. |
|
|
|||||
|
|
|
|
|
|
|
|
|
|
1,224 ∙ 108 |
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
Па |
|
|
|||||||||
7. |
Рассчитаем |
|
температуру плавления вещества при давлении |
|||||||||||||||||||||
300 105 Па, допустив, что величина dT/dP постоянна. Тогда температура
плавления:
= тр.т + ( − тр.т) = 144 + 8,17 ∙ 10−9 ∙ (300 ∙ 105 − 7998) =
=144,5
.
8. Вычислим изменение энтропии, энергии Гиббса и Гельмгольца,
энтальпии и внутренней энергии для процесса возгонки 1 моль вещества в тройной точке.
Изменение энтальпии возгонки нами было вычислено ранее:
∆ возг = 28956 Дж/моль.
Изменение внутренней энергии:
Дж
∆ возг = ∆ возг − · тр.т = 28956 − 8,31 · 144 = 27759 моль.
Изменение энтропии при этом:
∆ |
= |
∆ возг |
= |
28956 |
= 201 |
Дж |
. |
|
|
|
|||||
возг |
|
тр.т |
144 |
|
моль∙ |
||
|
|
|
|||||
Изменение энергии Гиббса в фазовом переходе:
∆ возг = 0 Дж/моль.
Изменение энергии Гельмгольца:
∆ возг = ∆ возг − · тр.т = −8,31 · 144 = −1196,6 Дж/моль.
9. Для однокомпонентной системы правило фаз Гиббса будет
выражаться следующим уравнением:
C = 3 - Ф,
19
где С - число степеней свободы;
Ф - количество фаз.
а) для температуры и давления тройной точки число степеней свободы равно 0, так как в этой точке существует 3 фазы одновременно:
C = 3 - Ф = 3 – 3 = 0;
б) при нормальной температуре кипения (Тнтк) и давлении p=1атм
(нормальное давление) число фаз равно 2, так как эта точка является фигуративной. Число степеней свободы при этом:
C = 3 - Ф = 3-2 = 1.
в) при нормальной температуре кипения (Тнтк) и давлении тройной точки (Pтр.т) число фаз равно единице, так как интересующая нас точка находится в области газовой фазы и не является фигуративной. Число степеней свободы при этом:
C = 3 - Ф = 3 - 1 = 2.
Это означает, что произвольно можно менять оба параметра (до известных пределов), число фаз останется равным единице.
ТЕМА 4. РАЗБАВЛЕННЫЕ РАСТВОРЫ
Зависимость давления насыщенного пара над раствором твердых веществ в летучих растворителях выражается законом Рауля:
относительное понижение давления пара растворителя над раствором равно мольной доле растворенного вещества:
∆ |
= |
|
в−ва |
|
, |
(4.1) |
|
|
|
|
+ |
|
|||
0 |
|
|
в−ва |
|
р |
|
|
где Ро– давление пара над чистым растворителем; Р – давление растворителя над раствором данной концентрации; ∆Р/Ро – относительное понижение давления пара растворителя; nв-ва – количество молей растворенного вещества; nр – количество молей растворителя.
20