Материал: 2018_02_15_01
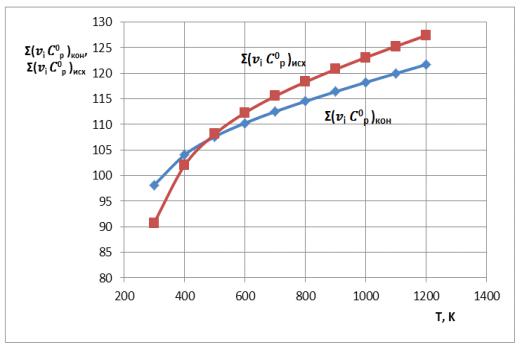
Таблица 2.2
Суммы теплоемкостей конечных и исходных веществ реакции А
при различных температурах
№ п/п |
Температура, К |
∑∆ Cр, кон, Дж/К |
∑∆ Cр, исх, Дж/К |
|
|
|
|
1 |
298 |
98,09 |
90,68 |
|
|
|
|
|
|
|
|
2 |
400 |
104,05 |
102,02 |
|
|
|
|
|
|
|
|
3 |
500 |
107,60 |
108,12 |
|
|
|
|
|
|
|
|
4 |
600 |
110,26 |
112,28 |
|
|
|
|
|
|
|
|
5 |
700 |
112,50 |
115,54 |
|
|
|
|
|
|
|
|
6 |
800 |
114,52 |
118,30 |
|
|
|
|
|
|
|
|
7 |
850 |
115,48 |
119,57 |
|
|
|
|
|
|
|
|
8 |
900 |
116,41 |
120,78 |
|
|
|
|
|
|
|
|
9 |
1000 |
118,22 |
123,09 |
|
|
|
|
|
|
|
|
10 |
1100 |
119,97 |
125,28 |
|
|
|
|
|
|
|
|
11 |
1200 |
121,70 |
127,39 |
|
|
|
|
|
|
|
|
Рис. 2.1. Зависимость сумм теплоемкостей конечных и исходных продуктов
реакции от температуры
11
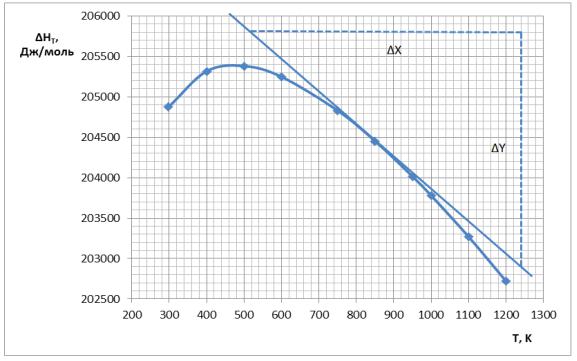
Таблица 2.3
К графическому определению производной (dН/dt) p
№ п/п |
Температура, К |
∆НоТ, кДж |
1 |
298 |
204875,0 |
|
|
|
2 |
400 |
205318,7 |
|
|
|
3 |
500 |
205381,5 |
|
|
|
4 |
600 |
205248,4 |
|
|
|
5 |
750 |
204830,4 |
|
|
|
6 |
850 |
204452,9 |
|
|
|
7 |
950 |
204016,0 |
|
|
|
8 |
1000 |
203778,5 |
|
|
|
9 |
1100 |
203269,6 |
|
|
|
10 |
1200 |
202719,7 |
|
|
|
Из данных табл. 2.1 и рис. 2.1 делаем вывод, что, поскольку
∆ = ∑∆ Cр, кон - ∑∆Ср,исх ˃ 0, в данном интервале температур зависимость
∆Ног,Т = f(T) является возрастающей функцией температуры.
Для графического определения производной (dН/dt p) при температуре Т1 (900 К) рассчитываем значения Н°г,T по уравнению аналитической зависимости:
Рис.2.2. Зависимость энтальпии реакции от температуры
12
∆Н г,Т = 114227,365 + 22,695 T – 0,5∙7,575∙10-3∙ T2 + 5,605∙105∙1/T
в интервале температур от 400 до 1000 К, помещаем их в табл. 2.3 и по касательной к кривой при температуре 900 К (рис. 2.2) определяем ∆ Н
реакции.
Расчет тангенса наклона касательной к кривой зависимости
∆Но г, Т = f(T) в точке Т1 = 900 К дает величину Cp = 20,21 Дж/(моль∙К).
Ответ: Графическое определение теплоемкости при 900 К дает значение Ср = 20,21 Дж/(моль∙К).
ТЕМА 3. ФАЗОВЫЕ РАВНОВЕСИЯ В ОДНОКОМПОНЕНТНОЙ
СИСТЕМЕ. УРАВНЕНИЕ КЛАУЗИУСА-КЛАПЕЙРОНА
Фазовыми равновесиями являются равновесия в гетерогенных системах, в которых не происходит химических изменений количества веществ, а происходит лишь переход компонентов из одной фазы в другую.
Для любых веществ известны три агрегатных состояния:
газообразное, жидкое и твердое. В фазовых равновесиях изучается переход веществ из одного агрегатного состояния в другое. Условием равновесия между фазами в гетерогенной системе является равенство химического потенциала данного компонента во всех фазах системы.
Основным законом фазового равновесия является правило фаз Гиббса,
согласно которому число степеней свободы равно числу условий
(температура, давление, концентрация), которые можно произвольно менять (в известных пределах), не изменяя этим числа или вида фаз системы.
Число степеней свободы (С) равновесной термодинамической однокомпонентной системы, на которую из внешних факторов влияют только температура и давление, равно числу независимых компонентов (К)
системы минус число фаз (Ф) плюс два:
13
С = К – Ф + 2. |
(3.1) |
Для двухкомпонентных систем при плоскостном графическом изображении диаграммы состояния один из внешних факторов (давление или температура) оставляют постоянным, и второй переменной величиной
будет концентрация компонентов. Тогда уравнение (3.1) переходит к виду:
С = К – Ф + 1. |
(3.2) |
Связь между основными термодинамическими |
параметрами |
однокомпонентной системы, находящейся в состоянии равновесия,
выражается уравнением Клаузиуса-Клапейрона. Дифференциальные формы этого уравнения записываются следующим образом:
|
|
|
= |
∆Hф.пр ; |
∆Hф.пр = Т |
|
|
∆Vm, |
(3.3) |
|||
|
|
|
|
|
||||||||
|
|
|
∙ |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
где ∆Hф.пр - |
теплота фазового |
перехода |
|
в условиях равновесия фаз |
||||||||
(испарение, |
плавление, |
возгонка); |
|
– |
температурный |
коэффициент |
||||||
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
давления насыщения пара; ∆Vm – разность молярных объемов фаз,
находящихся в равновесии.
Для равновесий: твердое вещество ↔ пар, жидкость ↔ пар в области
температур, далеких от критической, при условии: Vпар= R·T/P,
дифференциальное уравнение Клаузиуса-Клапейрона будет преобразовано следующим образом:
|
= |
∆Hф.пр |
|
|
·2 . |
(3.4) |
После интегрирования уравнения (3.4) при условии ∆Hф.пр. = const,
получаем:
lg P = |
− |
∆Hф.пр 1 . |
(3.5) |
|
2,303 |
2,303∙ |
|
Уравнение (3.5) представляет собой уравнение прямой – зависимость
lg P от 1/Т. |
(3.6) |
14

Задача 3.1
1. По зависимости давления насыщенного пара от температуры и плотности данного вещества А (табл.3.1) с молекулярной массой M в
твердом и жидком состояниях (dтв и dж в кг/м3) в тройной точке (тр.т):
1)постройте график зависимости lg P от 1/Т;
2)определите по графику координаты тройной точки;
3)рассчитайте среднюю теплоту испарения и возгонки;
4)постройте график зависимости давления насыщенного пара от температуры;
5)определите теплоту плавления вещества при температуре тройной точки;
6)вычислите dТ/dP для процесса плавления при температуре тройной точки;
7)вычислите температуру плавления вещества при давлении P, Па;
8)вычислите изменение энтропии, энергии Гиббса и Гельмгольца,
энтальпии и внутренней энергии для процесса возгонки 1 моль вещества в тройной точке; 9) определите число термодинамических степеней свободы при следующих
значениях температуры и давления:
а) Ттр.т , Pтр.т; б) Тнтк, P=1 атм; в) Тнтк, Pтр... т
|
|
|
|
|
|
Таблица 3.1 |
|
Исходные данные для решения задачи 3.1 |
|
||||
|
|
|
|
|
|
|
|
Состояние |
|
|
|
Условия |
|
|
|
|
|
|
|
|
твердое состояние |
|
жидкое состояние |
|
|
||
|
|
|
|
|
|
|
Т, К |
Р, Па |
|
Т, К |
Р, Па |
|
|
|
|
|
|
|
|
|
131 |
1333 |
|
137 |
6665 |
|
М= 68 |
135 |
1999,5 |
|
141 |
7331,5 |
|
Р = 300 105 Па |
137 |
2666 |
|
145 |
8664,5 |
|
dтв=1450 |
139,2 |
3999 |
|
146 |
9997,.5 |
|
dж=1434 |
141,5 |
5332 |
|
149 |
12663 |
|
|
144,0 |
7998 |
|
151,4 |
15996 |
|
|
146 |
9997,5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
15 |
|
|
|