Материал: 2018_02_15_01
Теперь рассчитаем эбулиоскопическую константу (4.5):
|
· |
2 |
∙ |
|
8,31 ∙ 1492 |
· 68 |
|
кг ∙ |
|
= |
кип |
|
= |
|
|
= 0,647 |
|
. |
|
|
|
|
|
|
|
||||
э |
1000 |
∙ |
исп |
|
1000 ∙ 19380 |
|
моль |
|
|
|
|
|
|
||||||
Рассчитаем повышение температуры кипения:
∆ = э ∙ = 0,710 ∙ 0,288 = 0,19 .
8. Рассчитаем температуру плавления растворителя при нормальном
давлении, пользуясь данными задачи 3.1:
пл = тр.т + |
|
( − тр.т) = 144 + 8,28 · 10−9 ∙ (105 − |
7998) |
= 144,0 . |
||||||||
|
||||||||||||
|
||||||||||||
Вычислим криоскопическую константу (4.4): |
|
|
|
|||||||||
|
|
|
|
· 2 |
∙ |
8,31 ∙ 1442 ∙ 68 |
|
|
кг · |
|
||
= |
|
пл |
|
= |
|
|
= 1,223 |
|
|
. |
||
|
|
|
|
|
|
|
||||||
|
кр |
|
1000 ∙ |
пл |
1000 ∙ 9576 |
|
|
моль |
|
|||
|
|
|
|
|
|
|||||||
Определим |
понижение |
температуры замерзания |
раствора, |
|||||||||
используя криоскопическую константу:
∆ = кр ∙ = 1,223 ∙ 0,288 = 0,35 .
ТЕМА 5. НЕОГРАНИЧЕННО СМЕШИВАЮЩИЕСЯ ЖИДКИЕ
СИСТЕМЫ
В идеальных растворах, состоящих из двух летучих компонентов,
концентрация компонента в паре и в жидкой фазе связана уравнениями:
п |
о |
ж |
; |
п |
о |
/Р)хВ |
ж |
, |
(5.1) |
хА |
= (РА |
/Р)хА |
хВ |
= (РВ |
|
где хАп и хВп - молярные доли компонентов А и В в паре;
хАж и хВж - молярные доли компонентов А и В в жидкой фазе;
РАо и РВо - давление насыщенного пара над чистыми компонентами А и В;
Р - общее давление над раствором.
Соотношение массы пара и массы жидкости при заданных условиях, если система гетерогенная, определяется по правилу рычага.
Если жидкости близки по химическим свойствам, то силы взаимодействия между однородными частицами (А - А, В - В) того же порядка, что и между разнородными (А - В). Полученный раствор
26
называется идеальным, и во всей области концентраций он подчиняется закону Рауля, т.е. парциальное давление пара каждого компонента при любой температуре пропорционально его молярной доле в растворе.
Общее давление пара над раствором равно сумме парциальных давлений:
Р = РАо хА + РВохВ . |
(5.2) |
Молярная доля компонента i в парообразной |
фазе равна его |
парциальному давлению, деленному на общее давление всех газов в смеси:
хiп |
= Рiохi/ Р . |
(5.3) |
Применив уравнение (5.3) |
к обоим компонентам бинарной системы, |
|
получим: |
|
|
хАп /хВп = РАо хАж/ (РВ хВж). |
(5.4) |
|
Из уравнения (5.4) следует, что у идеальных растворов состав пара
должен отличаться от состава жидкости (если только величины давления пара над чистыми веществами не равны друг другу). Состав пара отличается от состава жидкости также у неидеальных растворов, за исключением особых случаев образования азеотропных растворов.
Кривые зависимости общего давления от состава жидкой фазы для неидеальных растворов могут отклоняться в положительную или отрицательную сторону по сравнению с идеальными растворами.
Если отклонения от идеальности очень велики, то на кривых давление-состав может появиться максимум при положительных отклонениях от закона Рауля или минимум при отрицательных отклонениях.
Растворы, отвечающие по составу этим экстремальным точкам,
называются азеотропными, нераздельно кипящими, постоянно кипящими
или неразгонными. Состав их не меняется при кипении, и температура кипения при заданном внешнем давлении остается постоянной, как у чистых веществ. Изменение внешнего давления приводит к изменению
27
состава азеотропного раствора, что указывает на отсутствие в этих точках химического соединения.
При подсчете числа степеней свободы в азеотропной точке следует учитывать равенство составов жидкости и пара: С = 1 - 2 + 1 = 0.
Задача 5.1
Дана зависимость составов жидкой фазы и находящегося с ней в равновесии пара от температуры для двухкомпонентной жидкой системы
CH3OCH3 (А) – CH3OH (В) (табл. 5.1, табл. 5.2) при постоянном давлении.
Молярный состав жидкой фазы х и насыщенного пара у выражен в процентах вещества А. По приведенным данным:
1)постройте график зависимости состава пара от состава жидкости при постоянном давлении;
2)постройте диаграмму кипения системы CH3OCH3 (А) – CH3OH (В);
3)определите температуру кипения системы с молярным содержанием а % вещества А; каков состав первого пузырька пара над этой системой; при какой температуре закончится кипение системы;
каков состав последней капли жидкой фазы?
4)определите состав пара, находящегося в равновесии с жидкой фазой, кипящей при температуре Т1;
5)при помощи какого эксперимента можно установить состав жидкой бинарной системы, если она начинает кипеть при температуре Т1 при наличии диаграммы кипения системы?
6)какой компонент и в каком количестве может быть выделен из системы, состоящей из b кг вещества А и с кг вещества В?
7)какого компонента и какое количество надо добавить к указанной в п.6 смеси, чтобы получилась азеотропная система?
8)какое количество вещества А будет в парах и в жидкой фазе, если 2
кг смеси с молярным содержанием а % вещества А нагреть до
температуры Т1?
28

9) определите вариантность системы в азеотропной точке.
Таблица 5.1
Исходные данные для решения задачи 5.1
|
Р ·10-4, Па |
Молярный состав А, % |
|
||
Система |
|
|
Т, К |
||
х – жидкая фаза |
у – пар |
||||
|
|
||||
|
|
|
|||
|
|
|
|
|
|
|
|
0,0 |
0,0 |
337,7 |
|
|
|
4,8 |
14,0 |
335,9 |
|
|
|
17,6 |
31,7 |
333,1 |
|
А-CH3OCH3 |
|
28,0 |
42,0 |
331,3 |
|
|
40,0 |
51,6 |
330,2 |
||
|
10,133 |
||||
|
60,0 |
65,6 |
329,1 |
||
В-CH3OH |
|
||||
|
80,0 |
80,0 |
328,6 |
||
|
|
||||
|
|
90,0 |
94,0 |
328,8 |
|
|
|
99,0 |
9,0 |
329,1 |
|
|
|
100,0 |
100,0 |
329,5 |
|
|
|
|
|
|
|
Таблица 5.2
Исходные данные для решения задачи 5.1
Т1, К |
а, % |
b, кг |
с, кг |
|
|
|
|
329,25 |
60 |
73 |
27 |
|
|
|
|
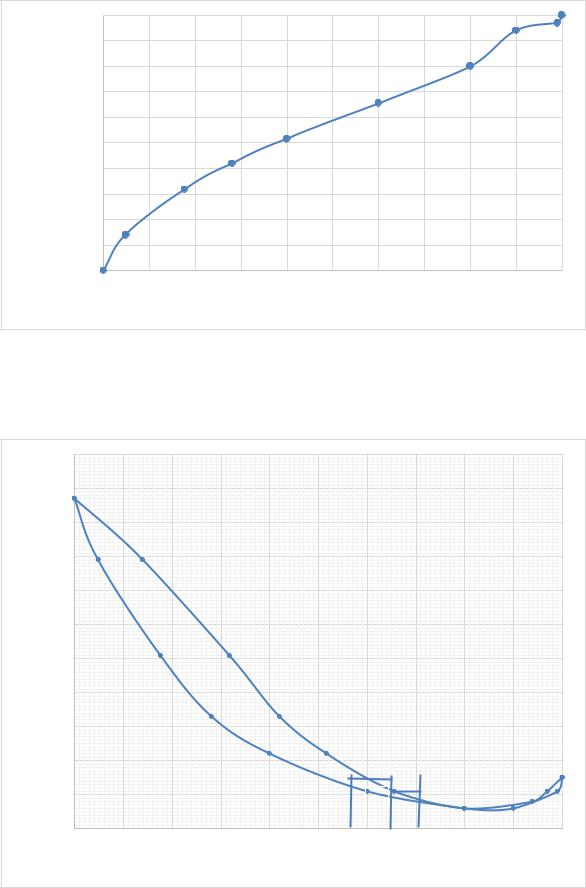
1. Построим график зависимости состава пара от состава жидкой фазы при постоянном давлении (рис. 5.1).
29
100
CH3OCH3 90
в пару, мол.% 80
70
60
50
40
30
20
10
0 |
|
|
|
|
|
|
|
|
|
|
0 |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
80 |
90 |
100 |
CH3OCH3 в жидкости, мол.%
Рис. 5.1. Диаграмма зависимости состава пара от состава жидкой
фазы при постоянном давлении
339 |
|
|
|
|
|
|
|
|
|
|
T, K 338 |
|
|
|
|
|
|
|
|
|
|
337 |
|
|
|
|
|
|
|
|
|
|
336 |
|
|
|
|
|
|
|
|
|
|
335 |
|
|
|
|
|
|
|
|
|
|
334 |
|
|
|
|
|
|
|
|
|
|
333 |
|
|
|
|
|
|
|
|
|
|
332 |
|
|
|
|
|
|
|
|
|
|
331 |
|
|
|
|
|
|
|
|
|
|
330 |
|
|
|
|
|
|
C |
|
|
|
329 |
|
|
|
|
|
D |
|
B |
|
|
|
|
|
|
|
A |
|
|
|
||
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
328 |
|
|
|
|
|
|
|
|
|
|
0 |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
80 |
90 |
100 |
CH3OCH3, мол.%
Рис. 5.2. Диаграмма состояния системы
30