Материал: 2018_02_15_01
2. На диаграмме 5.2 точкой А обозначена температура кипения смеси заданного состава (329,1 K). Состав первого пузырька пара (точка B): 65,5 мол. % CH3OCH3. При 329,5 K смесь состава в точке А полностью переходит в пар; состав последней капли жидкой фазы отвечает точке D
(52 мол. % CH3OCH3).
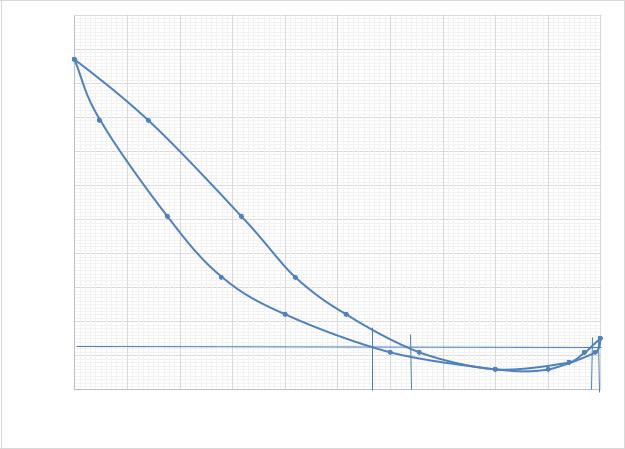
3. Определим состав на диаграмме состояния системы 5.3 (точка х),
находящегося в равновесии с жидкой фазой, кипящей при температуре
329,25 K.
Так как смесь содержит азеотропный состав (80 мол. % CH3OCH3,
Т = 328, 5), то 2 смеси имеют пар при температуре 329,5 K. Первая из них имеет 57 мол. % CH3OCH3 , а вторая – 98,0 мол. % вещества CH3OCH3.
339
T, K 338
337
336
335
334
333
332
331
330 |
|
|
|
|
|
x |
|
|
|
y |
329 |
|
|
|
|
|
|
|
|
|
|
328 |
|
|
|
|
|
|
|
|
|
|
0 |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
80 |
90 |
100 |
CH3OCH3, мол.%
Рис. 5.3. Диаграмма состояния системы
4. Как было показано ранее, при 329,5 K начинают кипеть пробы 2
составов. Для того чтобы выяснить состав пробы, которая на самом деле
31
кипит при этой температуре, надо экспериментально определить,
используя диаграмму состояния системы (рис. 5.3), добавление в пробу какого компонента будет расти или уменьшаться температура кипения системы. Поскольку из диаграммы видно, что при добавлении CH3OCH3
температура кипения этой пробы будет уменьшаться, то очевидно, что этой пробой будет состав жидкой фазы 57 мол.%.
5. Найдем молярную долю CH3OCH3 в смеси, содержащей 73 кг:
|
|
|
|
|
|
|
|
|
|
|
|
73 |
|
|
|
|
|
|
|
|
|
|
73 |
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
М 3 3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
хCH3OCH3 = |
|
|
|
|
|
|
|
|
= |
|
|
46,07 |
|
|
|
100 = 65,25 мол. %, |
|||||||||||||||||
|
73 |
|
|
|
+ |
27 |
|
|
|
|
|
73 |
|
+ |
27 |
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
М |
|
|
|
|
|
|
|
|
|
|
|
|
46,07 |
32 |
|
|||||||||||
|
|
|
|
|
|
|
|
3 |
3 |
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
27 |
|
|
|
|
|
|
|
|
|
|
27 |
|
|
|
|
|
|
||||||
х = |
|
|
|
|
|
М 3 Н |
|
|
|
|
|
= |
|
|
32 |
|
|
|
|
100 = 34,75 мол. % . |
|||||||||||||
|
27 |
|
|
|
|
|
|
73 |
|
|
27 |
|
|
73 |
|
|
|||||||||||||||||
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
+ |
|
|
|
|
|
|
|
|
|
|
|
32 + |
|
|
|
|
|
|
|
||||
|
|
|
|
|
М |
|
|
|
|
|
|
|
|
|
|
|
|
|
46,07 |
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
3 |
|
|
3 3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
где М – молярная масса CH3OCH3; |
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
3 |
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
– молярная масса . |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
Заданный |
состав |
|
|
имеет |
меньшее |
содержание CH3OCH3, чем |
||||||||||||||||||||||||||
азеотропный состав (80 мол. % эфира). Из этого следует, что можно
получить азеотроп в дистилляте и чистый метиловый спирт в кубовом
остатке.
6. Найдем массу ацетона в исходной смеси.
В смеси с содержанием метилового спирта 27 кг мольная доля спирта равна 34,75 мол. %, т.е. больше, чем в азеотропной смеси
(20 мол. % 3 ), значит, в чистом виде можно получить метиловый спирт, а в дистилляте будет смесь. Найдем массу спирта в исходной смеси:
32

|
|
|
|
|
20 |
|
|
|
|
|
|
20 |
|
32 |
|
|
||
|
|
= |
|
|
|
|
∙ |
|
3 |
|
= 73 ∙ |
|
|
∙ |
|
|
= 12,68 кг. |
|
|
|
|
100 − 20 |
М |
|
|
|
80 |
46,07 |
|||||||||
3 |
|
|
3 |
3 |
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
3 |
|
3 |
|
|
|
|
|
|
|
Масса CH3OH в кубовом остатке 27 – 12,68 = 14,32 кг.
7. Эфира в исходной смеси меньше, чем в азеотропе, поэтому для получения азеотропного состава надо в исходную пробу добавить ацетон.
Сначала вычислим массовую долю эфира в азеотропе:
80 ∙ 46,07= (100 − 80) ∙ 32 + 80 ∙ 46,07 100 = 85,20 масс. %.
Нам надо добавить некоторое количество эфира (x) в исходную смесь, чтобы получить азеотропную смесь:
73 +
85,20 = 73 + + 27 100.
Отсюда рассчитаем x:
|
1 |
|
|
= 0,852 |
||||||
|
|
|
|
|
|
|
|
|||
|
1 + |
|
|
|
27 |
|
||||
|
73 + |
|
|
|
||||||
|
1 |
|
|
|
|
27 |
|
|||
|
|
|
|
|
− 1 = |
|
|
|||
|
0,852 |
73 + |
||||||||
= |
27 |
|
|
− 73 = 82,4 кг. |
||||||
|
|
|
|
|
||||||
1 |
|
− 1 |
||||||||
|
0,852 |
|
|
|
|
|||||
8. Вычислим среднюю молярную массу смеси, состоящей на 60 % из эфира:
г
= 0,8 · М 3 3 + 0,2 · 3 = 0,8 · 46,07 + 0,2 · 32 = 43,26 моль.
Теперь вычислим количество молей в 2 кг смеси:
2000= 43,26 = 46,23 моля.
33
333
T, K
332
331
330
M N K
329
328
40 |
45 |
50 |
55 |
60 |
65 |
70 |
CH3OCH3, мол.%
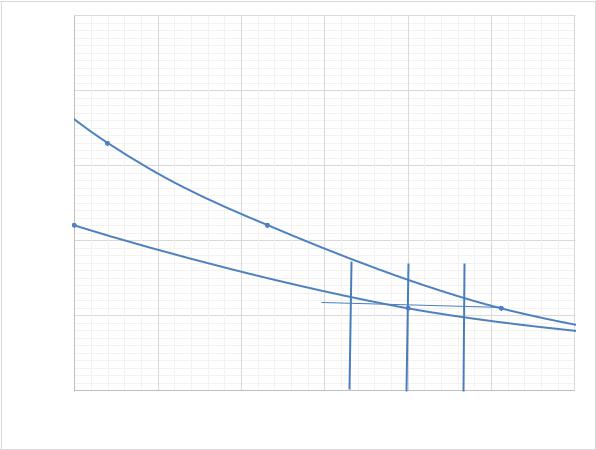
Рис. 5.4. Часть диаграммы кипения системы для расчета количества пара и жидкости по правилу рычага Пользуясь правилом рычага, вычислим количество пара (рис. 5.4):
пар = |
| | |
|
= 46,23 ∙ |
|
60 − 56,5 |
= 24,15 моля. |
|||||||||||
| | |
|
|
|
||||||||||||||
|
|
|
|
|
|
|
63,2 − 56,5 |
|
|||||||||
Рассчитаем количество молей жидкости: |
|
||||||||||||||||
жидк = − пар = 46,23 − 24,15 = 22,08 моля. |
|||||||||||||||||
Теперь рассчитаем массу CH3OCH3 |
в паре: |
|
|||||||||||||||
пар = пар ∙ |
63,2 |
∙ М |
= 24,15 ∙ |
63,2 |
∙ 46,07 = 703,16 г. |
||||||||||||
|
|
|
|
||||||||||||||
100 |
|
|
|
3 |
3 |
|
100 |
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Теперь рассчитаем массу CH3OCH3 |
в жидкости: |
|
|||||||||||||||
жидк = жидк ∙ |
56,5 |
∙ М |
= 22,08 ∙ |
56,5 |
|
∙ 46,07 = 574,73 г. |
|||||||||||
|
|
||||||||||||||||
100 |
|
|
|
3 |
3 |
100 |
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
9. Вариантность (число степеней свободы) при постоянном давлении
рассчитывается следующим образом (3.2):
С= K - Ф +1,
34
где С – число степеней свободы;
K – количество независимых компонентов;
Ф– количество фаз.
Вазеотропной смеси количество независимых компонентов равно
1, а количество фаз – 2, поэтому
С = 1 – 2 + 1 =0.
ТЕМА 6. ГЕТЕРОГЕННЫЕ РАВНОВЕСИЯ В БИНАРНЫХ
СИСТЕМАХ, СОДЕРЖАЩИХ ЖИДКУЮ И ТВЕРДУЮ ФАЗУ
Основным законом фазового равновесия является правило фаз Гиббса
(см. тему 3). Для предельно разбавленных растворов зависимость растворимости компонента в реальном растворе от температуры выражается уравнением Шредера:
ж = |
∆Нпл.1 |
|
∆Т, |
(6.1) |
|
· 2 |
(1−К |
|
|||
2 |
2 ) |
|
|
||
|
пл.1 |
|
|
|
|
где ∆Т – понижение температуры кристаллизации расплава (раствора)
концентрации 2ж:
|
|
∆Т = Тпл.1 - |
Т, |
(6.2) |
где Тпл.1- температура плавления растворителя; |
|
|||
∆Нпл.1 – теплота плавления растворителя; |
|
|||
К2 = х2тв/ х2ж;; |
|
|
||
х2тв |
- |
концентрация растворенного вещества в твердом растворе; |
|
|
х2ж |
- |
концентрация растворенного |
вещества в жидком |
расплаве |
(растворе). |
|
|
||
|
Для неизоморфно кристаллизующихся систем х2тв = 0 и К2 |
= 0. |
||
|
|
35 |
|
|