Материал: 1_metodichka_po_khimii
А + В → А... В → АВ
активированный
комплекс
Введем в эту систему катализатор К:
А + К → А... К → АК,
активированный
комплекс
АК + В → АК... В → АВ + К
Наличие катализатора в обратимом процессе не смещает равновесие. В этом случае катализатор в равной степени повышает скорость как прямой, так и обратной реакций.
Существуют вещества, которые, в отличие от катализаторов, замедляют или вообще прекращают ход химических реакций, - это ингибиторы. К ингибиторам можно отнести: вещества, выделяющиеся организмом и замедляющие развитие особей того или другого вида; естественные или синтетические соединения, угнетающие активность ферментов или полностью прекращающие их деятельность; любой реагент, тормозящий какой-либо биологический процесс. Например, пространственно экранированные фенолы ингибируют развитие злокачественных опухолей, а уротропин - коррозию металлов. В настоящее время известно много лекарственных препаратов, действующих как ингибиторы.
Вещества, активизирующие действие катализаторов, в частное биокатализаторов, называют активаторами. Некоторые вещества замедляют или прекращают действие катализаторов. Это ингибиторы катализаторов, каталитические яды. Есть вещества, восстанавливающие действие катализаторов, - реактиваторы катализаторов.
Активация и ингибирование проявляются и в ферментативных процессах. Так, наличие в реакционной среде примесей NaCl способствует быстрому гидролизу крахмала до глюкозы ферментами слюны - амилазой и мальтазой. Наличие в такой среде, например, CuSO4 ингибирует каталитический процесс расщепления крахмала ферментами слюны, так как их молекулы денатурируют и гидролиз не происходит.
Катализаторы, действующие в биосистемах, специфичны. Роль биокатализаторов (ферментов) часто выполняют белки, содержащие в активных центрах ионы металлов (металлоферменты). Например, в состав инсулина входит ион цинка, а витамина В12 - ион кобальта (III).
2.12. Химическое равновесие. Обратимые и необратимые реакции
Химические процессы происходят самопроизвольно, если в результате процесса уменьшается свободная энергия Гиббса, ΔG < 0. Если энтальпийный и энтропийный факторы действуют согласованно, направляя реакцию в сторону образования продуктов, то исходные вещества полностью превращаются в продукты реакции. Такие реакции называют необратимыми. Например:
2КСlО3 → 2КСl + 3О2;
Mg + 2НСl → MgCl2 + Н2.
Еcли же энтальпийный и энтропийный факторы направляют реакцию в противоположные стороны, то между исходными веществами и продуктами реакции существует минимальное значение энергии Гиббса. Исходные вещества реагируют между собой с образованием продуктов до тех пор, пока не образуется смесь исходных веществ и продуктов реакции, которой соответствует это минимальное значение G.
Если продукты реакции могут взаимодействовать между собой с образованием исходных веществ, то реакция происходит в двух противоположных направлениях. Такие реакции называют обратимыми. Например:
H2 + I2 ↔ 2HI,
N2 + 3H2 ↔ 2NH3.
В обратимых реакциях различают прямую реакцию, происходящую со скоростью V1, (ей соответствует константа скорости k1), и обратную, протекающую со скоростью V2 (ей соответствует константа скорости к2). Когда скорости прямой и обратной реакций станут равны, в системе установится состояние химического равновесия. Кинетическим условием химического равновесия является равенство скоростей прямой и обратной реакций. Химическое равновесие имеет динамический характер. Количественной характеристикой обратимой реакции служит константа равновесия.
2.13. Константа химического равновесия. Прогнозирование смещения химического равновесия
Если система находится в состоянии химического равновесия, то она будет в этом состоянии до тех пор, пока внешние условия сохраняются постоянными. Если эти условия изменяются, то система выходит из равновесия. Смещение равновесия происходит в соответствии с принципом Ле Шателье: если изменяется хотя бы одно из условий, при которых система находится в состоянии химического равновесия, то равновесие смещается в сторону того процесса, который уменьшает (ослабляет) это изменение.
Сместить равновесие можно, меняя концентрацию, давление, температуру.
1. В случае увеличения концентрации любого из веществ, принимающих участие в процессе, равновесие смещается в сторону убывания этого вещества, и наоборот. Например, если в системе: Н2 + I2 ↔ 2HI, находящейся в равновесии, увеличить концентрацию водорода, то равновесие сместится в сторону образования HI.
2. При повышении давления равновесие смещается в сторону образования меньшего числа молекул газа, т.е. в сторону снижения давления, и наоборот. Например, в реакции: 2СО + О2 → 2СО2 из трех молекул исходных газообразных веществ образуются две молекулы СО2, поэтому при увеличении давления равновесие сместится в сторону образования СО2.
3. Влияние температуры. Термодинамическим условием равновесия является ΔG = 0, т. е. и из уравнения Гибсса ΔG = ΔН - TΔS, при равновесии ΔН = TΔS, этропийный и энтальпийный факторы равны.
Чтобы в такой системе компенсировать повышение температуры, следует увеличивать энтальпийный фактор. Это возможно тогда, когда теплота поглощается, т.е. ΔН > 0. Система должна быть эдотермической. И, наоборот, уменьшение температуры система компенсирует увеличением теплоты, т.е. экзотермической реакцией.
Например, в системе: 2СО + О2 ↔ 2СО2, ΔН < 0 со снижением температуры равновесие смещается вправо, в сторону экзотермической реакции, а с повышением температуры – влево, в сторону эндотермической реакции.
Связывание гемоглобином (НЬ) кислорода (О2) с образованием оксигемоглобина (НЬ×О2) происходит в соответствии с уравнением
НЬ + О2 → НЬ×О2;
Кравн = [Hb×O2]/([Hb][O2]) = 1300
Увеличение концентрации О2 приводит к связыванию О2 с НЬ и смещению равновесия вправо - в сторону образования оксигемоглобина. Наоборот, если угарный газ СО связывается с гемоглобином, образуя более устойчивый комплекс, концентрация гемоглобина при этом уменьшается, и равновесие смещается влево - в сторону разрушения оксигемоглобина.
Равновесие смещается вправо, если какой-либо из продуктов выводится из сферы реакции, т.е. его концентрация уменьшается. Это происходит в случае образования газа, осадка или малодиссоциирующего вещества. Например, в желудке происходит реакция, снижающая кислотность его содержимого: NaHCO3 + НСl ↔ NaCl + Н2О + СО2
Умение использовать принцип Ле Шателье дает возможность прогнозировать многие изменения в организме, вызванные внешними воздействиями, и управлять ими.
3. Растворы: коллигативные свойства, способы выражения концентраций. Гетерогенные равновесия
3.1. Особенности физико-химических свойств воды
Организм взрослого человека на 65% состоит из воды, а новорождённого – на 75%. ⅔ от общего количества воды составляет внутриклеточная вода, ⅓ - внеклеточная.
Вода поступает в организм двумя путями: 1) алиментарным (еда, питьё) – 1,5-2,0 литра в сутки; 2) эндогенным (вода, образующаяся при метаболических превращениях) – 0,35-0,4 л в сутки.
Вода в организме участвует в:
процессах метаболизма;
терморегуляции как теплоноситель и хладагент;
трансформации энергии (синтез и гидролиз макроэргических соединений);
процессе диссоциации электролитов как полярный растворитель;
растворении минеральных и органических веществ, газов, жидкостей.
Свойства воды объясняются строением её молекул и структурированностью.
Молекула воды имеет 2 ковалентные полярные связи – О-Н. Электронная плотность в них сдвинута в сторону более электроотрицательного кислорода, имеющего 2 неподелённые электронные пары. Вследствие этого, на обоих атомах водорода локализуются частичный положительный заряд – δ+, а на атомах кислорода – частичный отрицательный – δ-. Т.о., молекулы Н2О – биполярные, что определяет взаимодействие между ними. Благодаря такому распределению зарядов, соседние молекулы Н2О могут притягиваться друг к другу за счёт сил электростатического взаимодействия между атомом кислорода одной молекулы Н2О и атомом водорода другой (рис. 3.1).
Р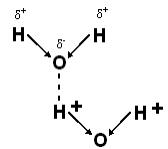 ис.
3.1. Водородные связи между молекулами
воды
ис.
3.1. Водородные связи между молекулами
воды
Такой тип электростатического притяжения называют водородной связью. Молекулы воды находятся в непрерывном движении, поэтому водородные связи постоянно быстро разрушаются и вновь образуются. За счёт водородных связей между молекулами воды образуются тетраэдры или кластеры. Молекулы воды, которые не образуют тетраэдры, могут входить и выходить из кластеров (рис. 3.2).
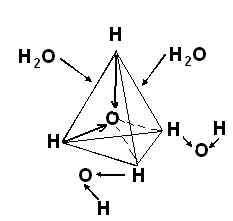 Рис.
3.2. Кластеры воды
Рис.
3.2. Кластеры воды
Водородные связи слабее ковалентных. Однако, благодаря их многочисленности, они обеспечивают многие аномальные физические свойства воды:
высокую удельную теплоёмкость;
высокую температуру кипения;
высокую температуру кристаллизации;
высокую удельную теплоту испарения;
Вода, как полярный растворитель, имеет хорошую растворяющую и диссоциирующую способность. Водородные связи образуются при растворении в воде кристаллических солей, способных ионизироваться молекулами Н2О, и многих органических соединений (альдегиды, аминокислоты, спирты, кетоны, углеводы). Растворимость этих веществ обусловлена способностью молекул Н2О образовывать водородные связи с функциональными группами этих соединений.
В воде могут находиться в диспергированном (раздробленном состоянии) вещества, содержащие в своём составе одновременно гидрофобные и гидрофильные группы. Такие соединения называют амфипатическими. Примерами могут служить калиевые и натриевые соли высших жирных кислот (ВЖК) – мыла. Ионизированная в воде карбоксильная группа ВЖК или её соли образует полярную головку, а углеводородный радикал – гидрофобный хвост (рис.3.3).
Р ис.
3.3. Строение амфипатических веществ
ис.
3.3. Строение амфипатических веществ
Соль ВЖК легко диспергируется в воде, образуя агрегаты, называемые мицеллами. В них гидрофобные хвосты жирной кислоты скрыты от водной фазы внутри мицеллы, а полярные головки обращены к Н2О, образуя с ней водородные связи (рис. 3.4). На этом свойстве основана способность амфипатических веществ поддерживать в диспергированном в воде состоянии даже неполярные вещества. Именно так происходит эмульгирование пищевых жиров в двенадцатиперстной кишке под действием амфипатических веществ, содержащихся в жёлчи – жёлчных кислот и фосфолипидов.
Р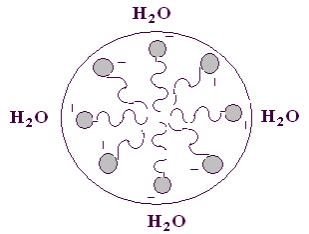 ис.
3.4. Диспергирование в воде амфипатических
веществ
ис.
3.4. Диспергирование в воде амфипатических
веществ
Водородные связи характерны не только для воды, они широко распространены в биологических системах. Водородные связи легко образуются между любым электроотрицательным атомом (F, О или N) и атомом Н, ковалентно связанным с другим электроотрицательным атомом. Приведём несколько примеров возникновения водородных связей в биологических системах:
1. Между комплементарными азотистыми основаниями нуклеиновых кислот, стабилизируя их вторичную структуру. Водородные связи возможны между А и Т, а также между Г и Ц.
2. Водородные связи стабилизируют вторичную, третичную и четвертичную структуры белковых молекул.