Материал: 1_metodichka_po_khimii
Одно из девяти сочетаний Г/Г не может соответствовать коллоидной системе, так как газы в обычных условиях при любых концентрациях дают истинные растворы (при очень высоких давлениях некоторые газовые системы образуют гетерогенные системы). Однако газовые смеси могут проявлять отдельные свойства гетерогенно-дисперсных систем благодаря непрерывным флуктуациям плотности и концентрации, вызывающим неоднородности в системе. Рассматривая жидкие растворы с молекулярной степенью дисперсности, к гетерогенно-дисперсным системам можно отнести растворы полимеров. Размеры макромолекул могут превышать размеры обычных коллоидных частиц. Эти системы обладают многими свойствами, характерными для типичных гетерогенно-дисперсных систем. Они как бы связывают в единое целое все дисперсные системы и указывают на непрерывность перехода от истинных молекулярных растворов к гетерогенным дисперсным системам.
Все дисперсные системы также можно разделить на два класса по кинетическим свойствам дисперсной фазы: свободнодисперсные системы, в которых дисперсная фаза подвижна, и связнодисперсные системы – системы с твердообразной дисперсионной средой, в которой частицы дисперсной фазы не могут свободно перемещаться.
И еще эти системы классифицируют по степени дисперсности. Свободнодисперсные системы подразделяют на ультрамикрогетерогенные, размер частиц которых лежит в пределах от 10-9 до 10-7 м (от 1 до 100 нм), микрогетерогенные с размером частиц от 10-7 до 10-5 м (от 0,1 до 10 мкм) и грубодисперсные с частицами, размеры которых превышают 10-5 м.
Ультрамикрогетерогенные системы часто называют истинно коллоидными или просто коллоидными, так как раньше только такие системы считались объектом коллоидной химии. С ростом числа молекул в частице она постепенно приобретает все свойства фазы. В современной литературе малоконцентрированные свободнодисперсные ультрамикрогетерогенные системы чаще называют золями (нем. Sole от лат. solutio – раствор). Среди них различают аэрозоли – золи с газообразной дисперсионной средой; лиозоли – золи с жидкой дисперсионной средой (греч. lios – жидкость). В зависимости от природы среды лиозоли называют гидрозолями (вода), органозолями (органическая среда) или, более конкретно, алкозолями (спирты) и т.д.
Cвязнодисперсные (структурированные) системы с жидкой дисперсионной средой называют гелями.
К микрогетерогенным системам относят суспензии (Т/Ж), эмульсии (Ж/Ж), пены (Г/Ж), порошки (Т/Г). Эти системы имеют большое значение в промышленности.
Из грубодисперсных систем наиболее распространены системы Т/Г (песок, щебень и др.).
По характеру взаимодействия между частицами дисперсной фазы и дисперсионной среды системы делят на лиофобные коллоиды и лиофильные коллоиды.
К лиофобным коллоидам относятся системы:
со слабым взаимодействием (или его отсутствием) частиц дисперсной фазы с дисперсионной средой;
с низкой смачиваемостью частиц вещества дисперсионной средой;
несамопроизвольностью диспергирования;
устойчивостью лишь в присутствии стабилизатора;
с особой структурой частиц, составляющих дисперсную фазу - мицеллами.
К лиофильным коллоидам относятся системы:
образующиеся самопроизвольно;
термодинамически устойчивые;
характеризующиеся сильным межфазным взаимодействием частиц дисперсной фазы с дисперсионной средой.
6.5. Получение лиофобных коллоидных растворов.
Образование и строение мицелл
Так как по размерам частиц коллоидные системы занимают промежуточное положение между грубодисперсными и молекулярными системами, поэтому их получают либо дроблением крупных частиц (диспергированием), либо ассоциацией (объединением) молекул или ионов в агрегаты (конденсацией). При получении коллоидных систем необходимо соблюдать условия:
-вещество дисперсной фазы должно быть нерастворимо в дисперсионной среде;
малая концентрация частиц дисперсной фазы;
наличие стабилизатора.
К диспергационным методам относят:
механическое диспергирование (растирание, дробление) при котором используются:
- шаровые мельницы (для измельчения тонкодисперсных порошков) и коллоидные мельницы позволяющие получать наибольшую степень дисперсности твердого вещества (коллоидную степень дисперсности);
- ультразвуковое диспергирование, основанное на прохождении ультразвуковой волны (частота 105 – 106 Гц) через грубосперсную систему и приводящие к кавитации.
Кавитация (cavitas – лат. - пустота) – образование в жидкости пузырьков с последующим их захлопыванием, приводящее к разрушению (измельчению) грубодисперсной системы.
Ультразвуковым диспергированием получают коллоидные растворы смол, красителей, серы, крахмала, лекарственных веществ и др. Преимущество метода в возможности получения стерильных лекарственных форм.
самопроизвольное диспергирование происходит при достаточно сильном взаимодействии между веществом дисперсной фазы и средой, что приводит к образованию лиофильных коллоидных систем (золи парафина в углеводородах, водные растворы углеводородов с большим содержанием ПАВ (до 40%).
К конденсационным методам относят:
физическую конденсацию:
а) конденсация из пара (образование облаков, тумана)
б) метод замены растворителя, в котором образование новой фазы происходит в результате замены «хорошего» растворителя на «плохой», в котором вещество не растворимо. Необходимым условием этого метода является полная смешиваемость «плохого» и «хорошего» растворителя.
химическую конденсацию, основанную на проведении в растворе химических реакций, сопровождающихся образованием нерастворимых или труднорастворимых веществ. При этом стабилизатором обычно служит электролит, взятый в избытке, или образующийся в результате побочной химической реакции.
К комбинированным методам, сочетающим в себе и диспергирование и конденсацию относят:
электрические методы, применяемые для получения золей металлов (золота, серебра, платины и др.):
а) дуговой метод (метод Бредига), основан на испарении металла электрода в электрической дуге (постоянный ток силой 5-10 А) в водной среде в присутствии стабилизатора с последующей конденсацией паров в коллоидные частицы;
б) искровой метод (метод Сведберга) основан на использовании переменного тока высокой частоты путем погружения электродов в металлический порошок, лежащий в органической дисперсионной среде. Применяется для получения органозолей металлов.
пептизация – распад агрегатов частиц в дисперсных системах с образованием коллоидных растворов. Используется в случае перевода свежеприготовленных рыхлых (аморфных) осадков в золь.
Различают несколько видов пептизации:
а) адсорбционная пептизация, (непосредственная) происходящая при физической адсорбции электролита, один из ионов которого способен достраивать кристаллическую решетку дисперсной фазы;
б) пептизация под действием ПАВ, способных адсорбироваться на частицах, придавать им заряд или образовывать сольватную оболочку, ослабляющую связь между частицами;
в) пептизация при отмывании осадка происходит при удалении из него электролита, вызывающего коагуляцию (объединение частиц осадка);
г) химическая (диссолюционная, посредственная) пептизация происходит с образованием золя при взаимодействии реагента с осадком и с образованием электролита (стабилизатора, пептизатора) придающего устойчивость золю;
д) пептизация при воздействии ультразвуковой волны, происходящая с высокой скоростью диспергирования.
Строение мицеллы лиофобных золей.
Элементарная коллоидная частица – мицелла – содержит нерастворимое в данной дисперсионной среде ядро, состоящее из диспергированного твердого вещества (агрегата) с адсорбированными ионами (потенциалопределяющими ионами – ПОИ). По правилу Панета – Фаянса «на поверхности твердого вещества адсорбируются ионы, способные достраивать его кристаллическую решетку, т.е. ионы, имеющие общую атомную группировку с агрегатом». Эти ионы и придают поверхности ядра электрический заряд. После возникновения заряда ядро притягивает из раствора ионы с противоположным знаком (противоионы), образуется двойной электрический слой. Часть противоионов прочно притягивается к ядру, образуя адсорбционный слой противоионов. Ядро вместе с адсорбционным слоем называется частицей или гранулой. Гранула характеризуется двойным электрическим слоем, который образуется из потенциалопределяющих ионов и противоионов. Противоионы,, которые находятся вне гранулы, образуют диффузный слой противоионов.
Схема строения мицеллы (рис. 6.7).
Пример: золь иодида серебра, полученного по реакции взаимодействия АgNO3 и KI при избытке KI.
АgNO3 + KI → АgI- + КNO3
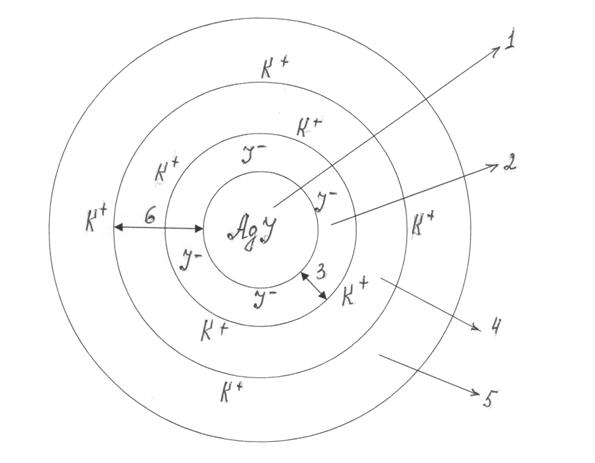
Рис. 6.7. Строение мицеллы:
1 – агрегат; 2 – потенциалопределяющие ионы; 3 – ядро; 4 – противоины адсорбционного слоя; 5 – противоионы диффузного слоя; 6 – гранула