Материал: 1_metodichka_po_khimii
Так, в комплексном соединении (NH4)2[Co2(C2O4)2(OH)2] мостиковыми служат бидентатные гидроксидные лиганды:
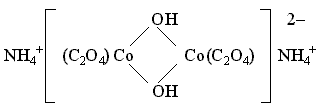
В роли мостикового лиганда может выступать полидентатный лиганд, имеющий несколько донорных атомов (например, NCS- с атомами N и S, способными участвовать в образовании связей по донорно-акцепторному механизму), либо лиганд с несколькими электронными парами при одном и том же атоме (например, Cl- или OH-.
В том случае, когда атомы комплексообразователя связаны между собой непосредственно, многоядерный комплекс относят к кластерному типу. Так, кластером является комплексный анион [Re2Cl8]2-
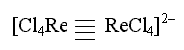
в котором реализуется четверная связь Re–Re: одна σ-связь, две π- связи и одна δ-связь. Особенно большое число кластерных комплексов насчитывается среди производных d-элементов.
Многоядерные
комплексы смешанного типа содержат как
связь комплексообразователь–комплексообразователь,
так и мостиковые лиганды.
Примером
комплекса смешанного типа может служить
карбонильный комплекс кобальта состава
[Co2(CO)8],
имеющий следующее строение:
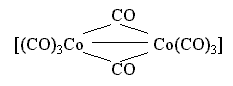
Здесь имеется одинарная связь Co-Co и два бидентатных карбонильных лиганда CO, осуществляющих мостиковое соединение атомов-комплексообразователей.
«Сандвичевые» («сэндвичевые») комплексные соединения – обширный класс, родоначальником которых является ферроцен. Ферроцен представляет собой желто-оранжевые кристаллы металлоорганического соединения, в котором атом железа располагается между двумя высокосимметричными пятичленными кольцами, образованными атомами углерода.
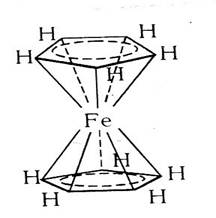
Рис. 5.4. Структура ферроцена
5.10. Устойчивость комплексных соединений в растворах.
Константа нестойкости комплекса
Внутренняя и внешняя сферы комплексного соединения сильно различаются по устойчивости; частицы, находящиеся во внешней сфере, связаны с комплексным ионом преимущественно электростатическими силами и легко отщепляются в водном растворе. Эта диссоциация называется первичной, она протекает почти нацело, по типу диссоциации сильных электролитов. Поэтому с помощью качественных химических реакций обычно обнаруживаются только ионы внешней сферы.
Лиганды, находящиеся по внутренней сфере, связаны с центральным атомом значительно прочнее и отщепляются лишь в небольшой степени. Обратимый распад внутренней сферы комплексного соединения носит название вторичной диссоциации (протекает по типу слабых электролитов). Например, диссоциацию комплекса [Ag(NH3)2]Cl имеет вид:
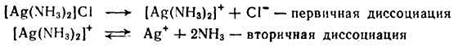
Вторичная диссоциация характеризуется наличием равновесия между комплексной частицей, центральным ионом и лигандами
Диссоциация ионов [Ag(NH3)2]+, согласно приведенному выше уравнению, как и диссоциация всякого слабого электролита, подчиняется закону действия масс и может быть охарактеризована соответствующей константой равновесия, называемой константой нестойкости комплексного иона:
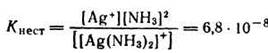
С учетом активности ионов уравнение констант нестойкости принимает следующий вид:
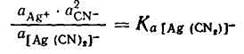
Полученная константа Ка называется термодинамической константой нестойкости.
Константы нестойкости для различных комплексных ионов весьма различны и могут служить мерой устойчивости комплекса. Чем устойчивее комплексный ион, тем меньше его константа нестойкости. Так, среди однотипных соединений, обладающих различными значениями констант нестойкости
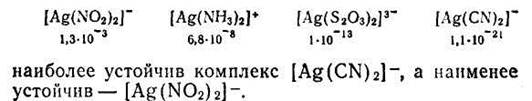
Величина, обратная константе нестойкости, называется общей или суммарной константой устойчивости. Следовательно,
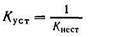
Последняя также характеризует устойчивость комплексных ионов.
Если ионизация комплексных ионов происходит по ступеням, то константы равновесия этих промежуточных реакций называются промежуточными или ступенчатыми константами нестойкости. Например, для комплексов кадмия с цианид-ионами известны следующие промежуточные константы нестойкости, которые нумеруются в порядке возрастания числа лигандов, связанных с центральным атомом комплекса, ионизирующего на одну ступень:
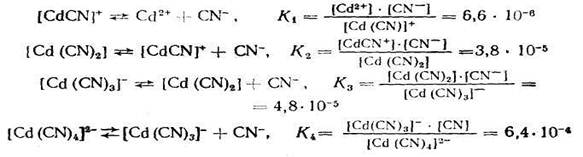
Однако практически пользуются общей суммарной константой нестойкости, равной произведению промежуточных констант нестойкости:
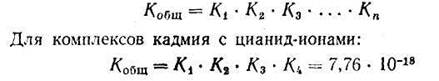
5.11. Представления о строении металлоферментов и других
биокомплексных соединений
Металлоферменты – это ферменты класса протеидов, для каталитического действия которых необходимы ионы металлов. Например, фермент каталаза, разрушающий перекись водорода (2Н2О2 → 2Н2О + О2), выполняет важную функцию в работе ферментативной антиоксидантной системы перовой линии защиты, обезвреживая активные формы кислорода, является железосодержащим ферментом.
Транспорт О2 в организме животных и человека осуществляется железосодержащими комплексами - гемоглобином и миоглобином. Это представители сложных белков, содержащие помимо белковой части, состоящей из аминокислотных остатков, небелковую часть – гем: порфириновый комплекс железа. Гем – это тетрапиррол (4 пиррольных кольца соединены метеновыми мостиками с образованием структуры - гема). В центре гемма содержится Fe2+, которое образует 4 координационные связи с атомоами азота пиррольных колец, 5 связь – с аминокислотой гистидин, расположенной в 8 положении спирали F белковой части гемоглобина или миоглобина (сокращенно, гис F8) – это связь белковой и небелковой части молекулы,, и 6 координационная связь образуется при присоединении молекуля кислорода к дезоксимио(гемо)глобину с образованием оксимио(гемо)глобина.
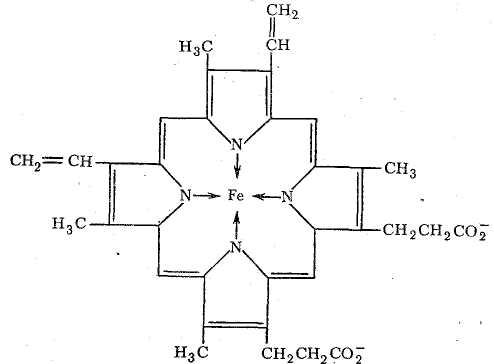
Созданию оптимального угла взаимодействия железа с кислородом, равного 120°, служит наличие в белковой части молекул мио- или гемоглобина гистидина Е7. В противном случае с атомом железа связывался бы СО (угол взаимодействия = 180°), который имеет более выраженное сродство к железу, чем кислород.
Таким образом, в координационную сферу иона железа входит пять атомов азота (четыре атома азота порфирина, один атом азота белкового гистидина). Шестое координационное место занимает О2.
Гемоглобин состоит из 4 субъединиц (имеет четвертичный уровень организации белковой части) и включает четыре гем-группы. Миоглобин сходен с гемоглобином по строению, но содержит только одну субъединицу (третичный уровень организации белковой части молекулы) и одну гем-группу. Гемоглобин является транспортером кисорода по крови, а миоглобин – запасает кислород в красных мышцах.
Теряя кислород, железо в гемоглобине (форма дезоксигемоглобина, КЧ железа = 5) переходит в высокоспиновое состояние. Ослабление связи с атомами азота порфирина приводит к выходу атома железа из плоскости кольца порфирина (на 0,7-0,8Ǻ). Напротив, вследствие присоединения кислорода к гемоглобину образуется низкоспиновый октаэдрический комплекс, железо в котором находится в плоскости порфиринового кольца (КЧ железа = 6). Хотя связывание молекулярного кислорода гемоглобином и миоглобином сопровождается ослаблением связи O=O в молекулярном кислороде из-за размещения π-дативных электронов железа на разрыхляющих орбиталях О2, этот процесс сам по себе не сопряжен с необратимым переносом электрона, поэтому его обычно не причисляют к ферментативным окислительно-восстановительным реакциям. Однако, разрыхление связи O=O не может не активировать окислительные реакции.
Связь кислорода с железом в макроциклическом комплексе молекулы гемоглобина не очень прочная и поэтому кислород в организме легко реагирует с восстановителями. Связывание гемоглобина молекулами угарного газа (СО) является аналогичным примером разрушения одного биокомплекса - оксигемоглобина за счет формирования в 300 раз более прочного другого биокомплекса – карбоксигемоглобина:
HbO2 + CO → HbCO + O2.
Недостаток железа в организме приводит к железодефицитной анемии.
Из других значимых в биологическом отношении комплексных соединений следует выделить витамин В12, участвующий в кроветоворении, синтезе ДНК и РНК, синтезе миелина и т.д.
К числу ферментов, катализирующих окислительно-восстановительные реакции, относятся гемсодержащие ферменты - цитохромы. Атомы железа в цитохромах, так же как в гемоглобине и миоглобине, координируют пять атомов азота (порфирина и гистидина), шестое координационное место занимает атом серы аминокислоты - метионина. Известно 50 видов ферментов этого типа, несколько различающихся по составу органической его части. Железо в цитохромах играет роль переносчика электронов - оно принимает электроны от восстановителя и передает их окислителю. Окислителем может быть и кислород, но он не участвует в координации железа, входящего в состав цитохромов, поскольку железо в цитохроме имеет полностью насыщенную координационную сферу. Так, цитохромы содержатся в дахательной цепи митохондрий, являясь переносчиками электронов; участвуют в обезвреживании токсических веществ в печени, превращая гидрофобные токсины в гидрофильные, способные поступать в желчь и затем с калом покидать организм.
Физико-химические основы дисперсных систем и поверхностных явлений
6.1. Поверхностная энергия Гиббса и поверхностное натяжение.
Сорбция. Абсорбция. Адсорбция
Частицы, находящиеся на поверхности каждой фазы, образуют особую поверхностную фазу, свойства которой существенно отличаются от свойств внутренних областей фазы. Частицы, расположенные на поверхности, взаимодействуют как с однородными частицами, так и с частицами другого рода (рис. 6.1).
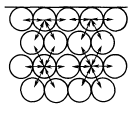 Рис.
6.1. Поверхностный слой вещества в
конденсированном состоянии
Рис.
6.1. Поверхностный слой вещества в
конденсированном состоянии
Следствием этого явления является то, что средняя энергия gs частицы, находящейся на поверхности раздела фаз, отличается от средней энергии такой же частицы в объеме фазы gv.. Важной характеристикой поверхностной фазы является поверхностная энергия Gs – разность средней энергии частицы, находящейся на поверхности, и частицы, находящейся в объеме фазы, умноженная на число частиц на поверхности N:
Gs=N(gs-gv) Под поверхностной энергией понимается энергия Гиббса (Gs) - образования поверхности. Она равна произведению удельной поверхностной энергии σ на площадь поверхности раздела фаз S:
Gs=σ×S
Удельная поверхностная энергия (Дж/м2) равна работе, необходимой для образования единицы площади свободной поверхности. Удельная поверхностная энергия определяется природой того или иного вещества. Чем выше энергия взаимодействия между частицами вещества, тем выше удельная поверхностная энергия. С увеличением температуры удельная поверхностная энергия уменьшается. Вблизи критической температуры поверхностное натяжение равно нулю.
Термин поверхностная энергия применяется к границе раздела газ - твердое тело. Для границы раздела конденсированных фаз (жидкость − жидкость, жидкость − твердое вещество) применяют термин межфазная энергия. Для границы раздела фаз жидкость − газ (пар) обычно используют термин удельная поверхностная энергия, называемая поверхностным натяжением.
Поверхностное натяжение σ − важнейшая термодинамическая характеристика поверхности раздела фаз, определяемая как работа обратимого изотермического образования единицы площади этой поверхности. В случае жидкой поверхности раздела поверхностное натяжение правомерно также рассматривать как работу, необходимую для увеличения единицы длины контура свободной поверхности:
Gs=σ×ΔL
где ΔL – увеличение длины контура свободной поверхности, м;
σ – поверхностное натяжение, н/м.
Благодаря поверхностному натяжению жидкость при отсутствии внешних силовых воздействий принимает форму шара, отвечающую минимальной величине поверхности и, следовательно, наименьшему значению свободной поверхностной энергии. Одним из путей понижения свободной поверхностной энергии является сорбция.
Сорбция (от лат. sorbeo – поглощаю) − поглощение твёрдым телом или жидкостью вещества из окружающей среды. Поглощающее тело называется сорбентом, поглощаемое им вещество − сорбатом (или сорбтивом). Различают поглощение вещества всей массой жидкого сорбента – это абсорбция; поверхностным слоем твёрдого или жидкого сорбента − это адсорбция.
Абсорбция − поглощение веществ из газовой смеси жидкостями. В технике абсорбция обычно пользуется для извлечения из газовой смеси какого-либо компонента. Абсорбция улучшается с повышением давления и понижением температуры.
Адсорбция − процесс концентрирования вещества из объема фаз на границе их раздела.
Адсорбент – вещество, способное адсорбировать другое вещество. Адсорбтив – вещество, которое может адсорбироваться. Адсорбат – адсорбированное вещество.
Процесс адсорбции является избирательным и обратимым. Адсорбция из растворов на твердом теле (имеющая поверхность раздела) бывает двух видов: