Материал: 1_metodichka_po_khimii
2.9. Зависимость скорости реакции от концентрации. Молекулярность элементарного акта реакции. Порядок реакции. Кинетические уравнения реакций первого и нулевого порядков. Период полупревращения
Молекулярность реакции определяется числом частиц, принимающих участие в элементарном акте столкновения. Реакции бывают мономолекулярными, би- и тримолекулярными. Вероятность столкновения трех частиц одновременно очень мала, четырехмолекулярные реакции неизвестны.
Примером мономолекулярной реакции является:
СH3-N=N-CH3 → C2H6 + N2;
бимолекулярной: H2 + I2 → 2HI.
Общий порядок реакции определяется как сумма показателей степеней концентраций в кинетическом уравнении реакции:
V = k[A]a[B]b.
Порядок реакции находят экспериментальным путем. Он может быть нулевым, целочисленным или дробным.
Если одно из реагирующих веществ находится в большом избытке, т.е. его концентрация практически не меняется, то порядок реакции по этому веществу равен нулю (нулевой порядок, V = kс0 = k). Примером такой реакции является инверсия водного раствора сахарозы:
С12Н22О11 + Н2О ↔ С6Н12О6 + С6Н12О6,
глюкоза фруктоза
в которой концентрация Н2О очень высока и в процессе реакции практически не изменяется, [Н2О] = const. Порядок реакции по воде является нулевым (n=0), а по сахарозе, как установлено экспериментально, первым. Общий порядок реакции равен n + m = 0 + 1 = 1 (V = kc).
Кинетическое уравнение имеет вид:
V = k [С12Н22О11].
Примером реакции второго порядка (V = kc2) является
H2 + I2 → 2HI;
V = k [H2][ I2];
n + m = 1 + 1 = 2.
Примерами биохимических реакций нулевого порядка служат ферментативные процессы, при которых субстрат находится в избытке, а количество фермента ограниченно. Реакциями первого порядка среди биохимических являются конечные стадии ферментативных процессов, реакции антигенов с антителами, изомерного превращения, гидролиза и т.д. Реакции, имеющие порядок больше чем два, среди биохимических процессов не встречаются.
Порядок реакции (экспериментальная величина) определяет зависимость скорости реакции от концентрации реагирующих веществ, а молекулярность (теоретическая величина) дает молекулярно-кинетическую характеристику процесса.
Численно для простых (элементарных) реакций молекулярность и порядок совпадают.
В кинетике часто пользуются понятием период полупревращения τ1/2.
Периодом полупревращения называют время, необходимое для того, чтобы прореагировала половина исходного количества вещества.
Период полупревращения используют также для характеристики процессов радиоактивного распада. И хотя эти процессы не являются химическими (их скорость не зависит от температуры), кинетически они описываются уравнением реакции первого порядка.
Характерной особенностью ферментативного катализа является возрастание скорости реакции до определенной постоянной величины (Vmax). Типичная кривая зависимости скорости ферментативной реакции и от концентрации субстрата [S] приведена на рис. 2.2.
В 1913 г. Михаэлис и Ментен предложили теорию, объясняющую эту зависимость. Для ферментативного процесса:
k1 k3
E
 + S ES E+P,
+ S ES E+P,
k2
где Е - фермент; S - субстрат; ES - промежуточный фермент-субстратный комплекс; Р - продукт реакции; k1, k2, k3 - константы скоростей соответствующих реакций.
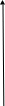

 Vmax
Vmax

 Vmax/2
Vmax/2

Km [S]
Рис. 2.2. Зависимость скорости ферментативной реакции от концентрации субстрата
Km = (k2 + k3)/ k1 - константа Михаэлиса.
На практике пользуются Vmax, т.е. скоростью, с которой реагирует фермент, полностью находящийся в виде комплекса ES.
Если V0 = Vmax/2, то Km = [S]
т.е.: значение константы Михаэлиса численно равно концентрации субстрата, при которой скорость реакции составляет половину максимальной.
Кинетическая константа k3 в уравнении Vmax = k3[E0] называется числом оборотов фермента; она показывает число молекул субстрата, которое превращается в продукт реакции в условиях, когда весь фермент находится в составе фермент-субстратного комплекса.
Величина константы Михаэлиса зависит от значения рН, температуры, природы субстрата и т.д. Ее значения, которые приводятся наряду с Vmax и числом оборотов фермента, являются количественные параметром ферментативной реакции при определенных условиях.
Уравнение Михаэлиса-Ментен:
V = Vmax×[S]/(Km+[S])
Закономерности химической кинетики используют в фармакокинетике и токсикокинетике, изучающих скорости действия и выведения из организма соответственно лекарственных средств и ядов.
Обычный путь действия лекарственного средства в организме можно рассматривать как последовательность двух процессов: всасывания из желудка в кровь (характеризуется константой всасывания kв) и выведения (элиминации) из крови в мочу (характеризуется константой выведения kэ).
Кинетика изменения массы лекарственного средства в желудке mж, в крови mк и в моче mм описывается системой трех дифференциальных уравнений, решаемой графически; на основании этого прогнозируют лечебную дозу лекарства m0 и время принятия очередной дозы.
2.10. Зависимость скорости реакции от температуры. Температурный коэффициент скорости реакции и его особенности для биохимических процессов. Энергия активации
С повышением температуры скорость химического процесса обычно увеличивается. В 1879 г. голландский ученый Я. Вант-Гофф сформулировал эмпирическое правило: с повышением температуры на 10 К скорость большинства химических реакций возрастает в 2-4 раза.
Математическая запись правила Я. Вант-Гоффа:
γ10 = (kт+10)/kт, где kт - константа скорости реакции при температуре Т; kт+10 - константа скорости реакции при температуре Т+10; γ10 - температурный коэффициент Вант-Гоффа. Его значение колеблется от 2 до 4. Для биохимических процессов γ10 изменяется в пределах от 7 до 10.
Все биологические процессы протекают в определенном интервале температур: 45-50°С. Оптимальной температура является 36-40°С. В организме теплокровных животных эта температура поддерживается постоянной благодаря терморегуляции соответствующей биосистемы. При изучении биосистем пользуются температурными коэффициентами γ2, γ3, γ5. Для сравнения их приводят к γ10.
Зависимость скорости реакции от температуры, в соответствии с правилом Вант-Гоффа, можно представить уравнением:
V2/V1 = γ ((T2-T1)/10)
Энергия активации. Значительное возрастание скорости реакции при повышении температуры нельзя объяснить только увеличением числа столкновений между частицами реагирующих веществ, т.к., в соответствии с кинетической теорией газов, с возрастанием температуры количество столкновений увеличивается в незначительной степени. Увеличение скорости реакции с повышением температуры объясняется тем, что химическая реакция происходит не при любом столкновении частичек реагирующих веществ, а только при встрече активных частиц, обладающих в момент столкновения необходимым избытком энергии.
Энергия, необходимая для превращения неактивных частичек в активные, называется энергией активации (Eа). Энергия активации – избыточная, по сравнению со средним значением, энергия, необходимая для вступления реагирующих веществ в реакцию при их столкновении. Энергию активации измеряют в килоджоулях на моль (кДж/моль). Обычно Е составляет от 40 до 200 кДж/моль.
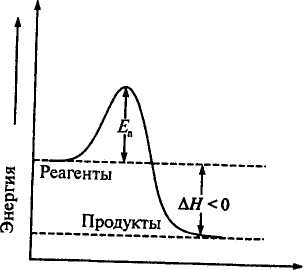
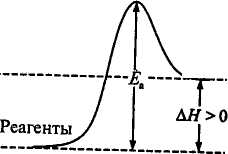
Энергетическая диаграмма экзотермической и эндотермической реакции представлена на рис. 2.3. Для любого химического процесса можно выделить начальное, промежуточное и конечное состояния. На вершине энергетического барьера реагенты находятся в промежуточном состоянии, которое называется активированным комплексом, или переходным состоянием. Разность между энергией активированного комплекса и начальной энергией реагентов равна Еа, а разность между энергией продуктов реакции и исходных веществ (реагентов) - ΔН, тепловому эффекту реакции. Энергия активации, в отличие от ΔН, всегда величина положительная. Для экзотермической реакции (рис. 2.3, а) продукты расположены на более низком энергетическом уровне, чем реагенты (Еа < ΔН).
Активированный
комплекс
А
Рис. 2.3. Энергетические
диаграммы реакций: А
– экзотермической Б - эндотермической
Еа является основным фактором, определяющим скорость реакции: если Еа > 120 кДж/моль (выше энергетический барьер, меньше активных частиц в системе), реакция идет медленно; и наоборот, если Еа < 40 кДж/моль, реакция осуществляется с большой скоростью.
Для реакций с участием сложных биомолекул следует учитывать тот факт, что в активированном комплексе, образовавшемся при соударении частиц, молекулы должны быть ориентированы в пространстве определенным образом, так как трансформации подвергается лишь реагирующий участок молекулы, небольшой по отношению к ее размеру.
Если известны константы скорости k1 и k2 при температурах Т1 и Т2, можно рассчитать значение Еа.
В биохимических процессах энергия активации в 2-3 раза меньше, чем в неорганических. Вместе с тем Еа реакции с участием чужеродных веществ, ксенобиотиков, значительно превышает Еа обычных биохимических процессов. Этот факт является естественной биозащитой системы от влияния чужеродных веществ, т.е. естественные для организма реакции происходят в благоприятных условиях с низкой Еа, а для чужеродных реакций Еа высокая. Это является генным барьером, характеризующим одну из главных особенностей протекания биохимических процессов.
2.11. Катализ гомогенный и гетерогенный. Ферментативный катализ
Катализ – явление повышения скорости химического процесса с помощью катализаторов.
Катализаторы - это вещества, которые увеличивают скорость химических процессов, не изменяясь при этом ни качественно (химический состав), ни количественно. Катализатор может изменять не только скорость химического процесса, но и его направление. В зависимости от природы катализатора из одних и тех же веществ образуются различные продукты:
(ZnO, Сг2О3)

 СН3ОН
СН3ОН
(ZnO, Сг2О3, КОН)
С О
+ Н2
С2Н5ОН
О
+ Н2
С2Н5ОН
(Ni)
 СН4
+ Н2О
СН4
+ Н2О
Существует явление автокатализа, когда катализатором является один из продуктов реакции.
Каталитические реакции - это процессы, в которых принимают участие катализаторы.
Биохимические процессы - это каталитические реакции, в которых в качестве катализаторов принимают участие специфические вещества - ферменты, или энзимы, и потому эти процессы част называют ферментативными.
В зависимости от того, в какой фазе находится катализатор, различают гетерогенный и гомогенный катализ. В случае гомогенного катализа катализатор и вещества, принимающие участие в реакции, образуют одну фазу. Например, разложение раствора пероксида водорода при наличии ионов меди (II) как катализатора:
Cu2+
2 H2O2
2H2O
+ O2
H2O2
2H2O
+ O2
В случае гетерогенного катализа катализатор находится в системе в виде самостоятельной фазы:
V2O5 или Pt
2 SO2 (г) + O2 (г) 2SO3 (г)
Ферменты относят к микрогетерогенным катализаторам. Мик-рогетерогенный - это такой тип катализа, когда катализатор и реагенты находятся в коллоидно-дисперсном состоянии. Размеры частичек ферментов близки к размерам мицелл коллоидных растворов – 1-100 нм. По отношению к субстратам, частички которых часто намного меньше, катализаторы являются гетерогенными.
Действие катализатора связано с тем, что он снижает энергию активации реакции. При наличии катализатора реакция проходит через другие промежуточные стадии, чем в его отсутствие, причем эти стадии энергетически более доступны. При наличии катализатора возникают другие активированные комплексы; при этом для их образования нужно меньше энергии, чем для образования активированных комплексов, возникающих в отсутствие катализатора.
Механизмы действия катализаторов исключительно сложны, почти каждому катализатору соответствует свой механизм, хотя присущи и общие черты: