Материал: 1_metodichka_po_khimii
3.2. Растворимость, коэффициент растворимости. Факторы, от которых зависит растворимость веществ
Растворимость веществ, т.е. способность растворяться в том или ином растворителе, различается; качественно по способности растворяться вещества можно разделить:
на хорошо растворимые (больше 1 г вещества в 100 г растворителя);
малорастворимые (0,1–1,0 г вещества в 100 г растворителя);
нерастворимые (меньше 0,1 г вещества в 100 г растворителя).
Однако следует иметь в виду, что абсолютно нерастворимых веществ в природе нет. Например, погруженная в воду серебряная монета частично поставляет в раствор ионы Ag+, благодаря чему вода приобретает целебные свойства.
Количественно растворимость характеризуют содержанием растворенного вещества в насыщенном растворе. Это содержание выражают с помощью коэффициента растворимости или массовой доли насыщенного раствора.
Коэффициент растворимости s (k) равен максимальной массе вещества (в г), которое можно растворить в данных условиях в 100 г (реже — в 1 дм3) растворителя, чтобы получить насыщенный при данных условиях раствор. В случае газов растворимость часто задают в кубических сантиметрах (или граммах) на 1 дм3: см3/дм3 или г/дм3.
При записи коэффициента растворимости обязательно указывается вещество, растворитель и внешние условия (для веществ в твердом состоянии обычно в качестве внешних условий указывают только температуру), например:
растворимость KNO3при 20°С равна 25 г в 100 г воды, или
растворимость KNO3 в воде при 20°С равна 250 г/л.
Рассмотрим факторы, влияющие на растворимость веществ.
1. Природа растворяемого вещества и растворителя. Подобное растворяется в подобном. Это означает, что энергия взаимодействия между частицами растворяемого вещества должна быть близка к энергии межмолекулярных сил в растворителе. Вода как полярный растворитель лучше растворяет ионные вещества или вещества молекулярного строения с полярными молекулами: соли, щелочи, галогеноводороды, серная кислота и др.; в то же время неполярные алканы, бензол в воде плохо растворимы. Напротив, хорошими растворителями неполярных веществ являются керосин, бензин, состоящие из неполярных молекул углеводородов; имеющий неполярные молекулы йод лучше растворим в бензоле, чем в воде. Растворимость веществ в воде возрастает, если они химически взаимодействуют с водой (SO3, P2O5, Na2O и др.) или образуют с ней водородные связи (спирты, аммиак, фтороводород, пероксид водорода).
2. Температура (принцип Ле Шателье).
Растворение газов - процесс чаще всего экзотермический, поскольку при растворении газов практически отсутствуют затраты энергии на разрыв связей между молекулами газа:
А (г) ⇄+H2O А (р-р)+Q .
Согласно принципу Ле Шателье, понижение температуры сместит это равновесие вправо, а повышение - влево. Таким образом, при повышении температуры растворимость газов в воде понижается, а при понижении температуры - возрастает.
По этой причине реки в северных широтах содержат больше кислорода и, следовательно, более богаты рыбой.
Повышение температуры на растворимость жидкостей влияет по-разному: иногда при нагревании жидкости смешиваются неограниченно, а иногда расслаиваются. В большинстве же случаев при повышении температуры взаимная растворимость жидкостей возрастает, вплоть до неограниченного по массе смешивания.
В случае твердых веществ влияние температуры на растворимость может быть различным (рис. 3.5); в большинстве случаев с ростом
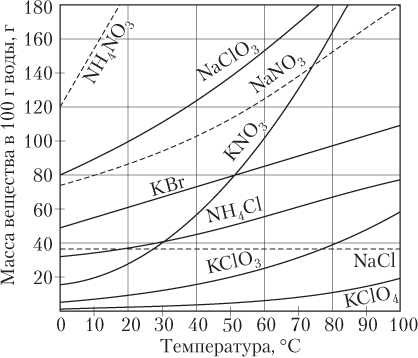
Рис. 3.5. Кривые растворимости некоторых солей в воде
температуры раствормость твердых веществ возрастает, однако растворимость Ca(OH)2, CaCO3, CaSO4 уменьшается. Растворимость NaCl от температуры зависит слабо.
3. Давление. При растворении твердых веществ в жидкостях (или жидкости в жидкости) объем существенно не изменяется, поэтому изменение давления на растворимость в этом случае практически не влияет. Растворение газа в жидкости всегда сопровождается уменьшением объема, поэтому в случае газов повышение давления увеличивает их растворимость в жидкостях, а понижение давления, наоборот, уменьшает.
Растворимость не следует путать со скоростью растворения. Например, растворимость кускового сахара и сахарного песка одинаковые, однако насыщенный раствор сахара в воде быстрее образуется в случае сахара-песка (сахар-песок растворяется быстрее, так как в этом случае больше поверхность соприкосновения растворителя и растворяемого вещества). Повышению скорости растворения твердого вещества в жидкости способствует перемешивание, однако на растворимость оно не влияет.
Отметим, что не для всяких веществ можно получить насыщенные растворы. Есть вещества, растворимость которых в воде неограниченна: метанол, этанол, пропанол-1 и пропанол-2, уксусная, серная, муравьиная, пропановая и азотная кислоты, этаналь, этиленгликоль, глицерин.
Для растворов веществ, неограниченно смешивающихся с водой, понятия «насыщенный» и «ненасыщенный» не применимы (нельзя, например, говорить: насыщенный раствор серной кислоты). Очевидно, понятия «разбавленный» и «концентрированный» для веществ, неограниченно растворяющихся в воде, применимы
Способы выражения концентрации растворов
Содержание растворенного вещества в растворе может быть выражено несколькими способами:
Массовая доля растворенного вещества: отношение массы растворенного вещества к массе раствора:
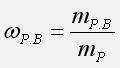
где
![]() –
массовая доля растворенного вещества,
–
массовая доля растворенного вещества,
![]() –
масса растворенного вещества,
–
масса растворенного вещества,
![]() –
масса раствора. Это частный случай
определения массовой доли.
–
масса раствора. Это частный случай
определения массовой доли.
Концентрация
(молярная концентрация, молярность):
отношение количества растворенного
вещества
![]() к
объему раствора V:
к
объему раствора V:
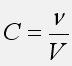
Молярная концентрация имеет принятую в химии размерность [моль/л], которая часто обозначается М и называется молярностью. Например, концентрация раствора 5 моль/л может быть записана как 5 М и такой раствор называется пятимолярным.
Молярная концентрация эквивалента (нормальность) показывает, какое количество моль эквивалентов растворенного вещества содержится в 1 л раствора.
Молярную концентрацию эквивалента Сэк(В) находят как отношение количества эквивалентов вещества nэк(В) к объему раствора Vp
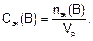
Размерность молярной концентрации эквивалента: моль×л. Сокращенная форма записи единицы молярной концентрации эквивалента – н. Например, 2н. означает, что в 1 л раствора содержится 2 моль эквивалента растворенного вещества.
Зная массу растворенного вещества m(B) и его молярную массу эквивалента Мэк(В), можно найти количество эквивалента вещества:
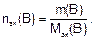
Молярная масса эквивалента вещества равна произведению фактора эквивалентности fэк(В) на молярную массу вещества М(В)
Мэк(В) = fэк(В)×М(В).
Эквивалент – это реальная или условная частица вещества, соответствующая в реакциях обмена одному атому или иону водорода (Н или Н+), а в окислительно-восстановительных реакциях – одному электрону.
Фактор эквивалентности – число, показывающее, какую часть от реальной частицы (молекулы, атома, иона и т.д.) вещества составляет эквивалент этого вещества.
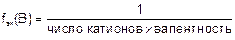 .
.
Например, для Na3PO4 заряд катиона Na+ равен 1, число катионов – 3, тогда
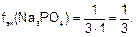
Пример. Вычислите молярную концентрацию эквивалента хлорида железа (III) в растворе, полученном при растворении 40 г FeCl3 в 200 мл воды. Плотность раствора 1,182 г/мл.
Решение.
Молярная масса хлорида железа (III):
M(FeCl3) = 162 г/моль.
Фактор эквивалентности fэк = 1/3.
Молярная масса эквивалента
Mэк(FeCl3) = fэк(FeCl3)×M(FeCl3) = 162 × (1/3) = 54 г/моль.
Количество эквивалента вещества, содержащегося в 40 г хлорида железа (III), составляет:
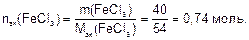
Масса раствора:
mp = m(FeCl3) + m(H2O);
ρ(H2O) = 1 г/мл; m(H2O) = 200 × 1 = 200 г;
mp = 40 + 200 = 240 г.
Объем
раствора:
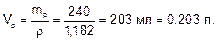
Находим молярную концентрацию эквивалента раствора хлорида железа (III):
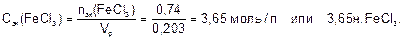
Моляльная доля растворенного вещества (Моляльность) [моль/кг] - безразмерная величина, равная отношению количества растворенного вещества к общему количеству веществ в растворе:
![]()
где N(Х) - мольная доля растворенного вещества X; v(Х) - количество растворенного вещества X, моль;
v(S) - количество вещества растворителя S, моль.
Коллигативные свойства растворов
Растворители под влиянием растворённых в них веществ изменяют свои физические свойства. Растворы, в отличие от чистых растворителей, проявляют особые свойства, известные под названием «коллигативные», что значит взаимосвязанные.
Коллигативные свойства – это свойства растворов, зависящие только от числа растворённых частиц в единице массы растворителя и от абсолютной температуры, и не зависящие от их природы. Например, все одномоляльные растворы неэлектролитов (содержащие 1 моль растворённого вещества на 1 кг растворителя), имеют одинаковые отличия в температуре замерзания и кипения от чистых растворителей, и одинаковое осмотическое давление.
К коллигативным свойствам относятся:
диффузия;
понижение давления насыщенного пара растворителя над раствором, по сравнению с насыщенным паром растворителя над чистым растворителем;
повышение температуры кипения раствора, по сравнению с чистым растворителем;
понижение температуры замерзания раствора, по сравнению с чистым растворителем;
осмотическое давление.
Диффузия – это самопроизвольный процесс выравнивания концентрации растворённого вещества в объёме.
Она обусловлена 2 факторами: 1) наличием рыхлой структуры и пустот в растворителе (например, в 1 л воды её молекулами занято только примерно 370 мл), 2) тепловым движением частиц раствора.
Диффузия прекращается, если концентрация во всех частях раствора становится одинаковой. Скорость диффузии зависит от:
абсолютной температуры;
градиента концентрации;
вязкости растворителя;
размера диффундирующих частиц.
Скорость диффузии возрастает при повышении температуры и градиента концентрации и уменьшается при увеличении вязкости растворителя, размера и массы диффундирующих частиц. Поэтому растворы высокомолекулярных соединений (ВМС - белков, полисахаридов и др.) имеют очень низкий коэффициент диффузии.
Диффузия может быть выражена количественно. Её описывает закон Фика: количество растворенного вещества m, проходящее за время t через площадь поперечного сечения сосуда S, которая разделяет растворы с разными концентрациями C1 и C2 определяется уравнением:
m / t = - DS ×(C2 –C1) / x2 – x1,
где: m/t – скорость диффузии, D – коэффициент диффузии, равный количеству вещества, диффундирующего через 1 см2 поверхности раздела за время t при градиенте концентраций, равном 1; S – площадь поперечного сечения сосуда; (C2–C1) – градиент концентраций; (x2–x1) – расстояние, пройденное диффундирующей частицей от дна сосуда из раствора с концентрацией C1 в раствор с концентрацией C2 (рис. 3.6).
Р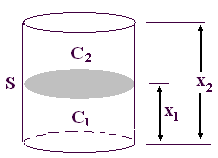 ис.
3.6. Закон Фика
ис.
3.6. Закон Фика
Для биологических мембран это уравнение имеет следующий вид:
m / t = - рS (C2 –C1),
где: р – коэффициент проницаемости мембраны, C1 и C2 – концентрации по обе стороны мембраны.
Диффузия играет важную роль в биологических системах. Благодаря диффузии осуществляется транспорт метаболитов внутри клеток и через мембрану. Так, например, в организме человека ежеминутно путём диффузии через стенки капилляров перемещается 1500 л жидкости.
2. Понижение давления насыщенного пара растворителя над раствором, по сравнению с насыщенным паром растворителя над чистым растворителем. При данной температуре давление насыщенного пара над каждой жидкостью – величина постоянная. При растворении в жидкости нелетучего вещества давление насыщенного пара этой жидкости над ней понижается. Т.о., давление насыщенного пара растворителя над раствором всегда ниже, чем над чистым растворителем при той же температуре. Разность между этими величинами называют понижением давления пара над раствором (или понижением давления пара раствора). Отношение величины этого понижения к давлению насыщенного пара над чистым растворителем называется относительным понижением давления пара над раствором.
Пусть давление насыщенного пара растворителя над чистым растворителем равно Р0, а над раствором – Р. Тогда относительное понижение давления пара над раствором будет представлять собою дробь: (Р0 – Р) / Р0.
Это относительное понижение давления насыщенного пара растворителя над раствором равно мольной доле растворённого вещества (закон Рауля). Математически закон Рауля можно выразить так:
(Р0 – Р) / Р0 = n / n+N,
где: Р0 – давление насыщенного пара над чистым растворителем, Р – давление насыщенного пара над раствором, n – число молей растворённого вещества, N – число молей растворителя в определенном объёме, n+N – молярная (мольная) доля растворённого вещества.
Следствием закона Рауля являются два свойства растворов: температура замерзания растворов ниже, а температура кипения – выше, чем у чистых растворителей. Причём повышение температуры кипения и понижение температуры замерзания растворов неэлектролитов прямо пропорциональны их моляльной концентрации. В результате при атмосферном давлении, например, водные растворы кипят при температуре выше 100°С и замерзают при температуре ниже 0°С.