Материал: 1_metodichka_po_khimii
4.10. Механизм сопряженного действия буферных систем
Защита от кислоты: при добавлении сильной кислоты (Н+) в работу вступает оснóвный компонент буфера, связывая протоны водорода в слабую кислоту – компонент буфера. Поэтому рН среды практически не меняется. Защита от кислоты будет продолжаться до тех пор, пока в буфере есть оснóвный компонент. Другими словами, буфер обладает определенной емкостью по кислоте.
Защита от щелочи: при добавлении щелочи (ОН−) в работу вступает кислотный компонент буфера, и, отдавая свои Н+ на ОН−, связывает их в воду, что не может повлиять на рН среды. В то же время кислотный компонент буфера превращается в сопряженное основание – компонент буфера. Поэтому рН среды практически не меняется. Защита от щелочи будет продолжаться до тех пор, пока в буфере есть кислотный компонент. Другими словами, буфер обладает определенной емкостью по основанию.
4.11. Понятие о кислотно-основном состоянии организма: рН крови, ацидоз, алкалоз, щелочной резерв крови
В поддержании кислотно-основного гомеостаза (баланс оптимальных концентраций кислотных и основных компонентов физиологических систем) участвуют все буферные системы организма. Действия их взаимосвязаны и находятся в состоянии равновесия. Наиболее связан со всеми буферными системами гидрокарбонатный буфер. Нарушения в любой буферной системе сказываются на концентрациях его компонентов, поэтому изменение параметров гидрокарбонатной буферной системы может достаточно точно характеризовать КОС организма.
КОС крови в норме характеризуется следующими метаболическими показателями:
рН плазмы 7,4±0,05;
[НСО3-]=(24,4±3) моль/л ― щелочной резерв кови;
рСО2=40 мм рт.ст.- парциальное давление СО2 над кровью.
Из уравнения Гендерсона-Гассельбаха для гидрокарбонатного буфера очевидно, что при изменении концентрации или парциального давления СО2 происходит изменение КОС крови.
Поддержание оптимального значения реакции среды в различных частях организма достигается благодаря согласованной работе буферных систем и органов выделения. Сдвиг реакции среды в кислую сторону называют ацидоз, а в оснóвную – алкалоз. Критическими значениями для сохранения жизни являются: сдвиг в кислую сторону до 6,8, а в оснóвную – 8,0. По происхождению ацидоз и алкалоз могут быть дыхательными или метаболическими.
Метаболический ацидоз развивается вследствие:
а) повышенной продукции метаболических кислот;
б) в результате потери гидрокарбонатов.
Повышенная продукция метаболических кислот происходит при:
1. сахарном диабете I типа, длительном, полном голодании или резком сокращении доли углеводов в рационе;
2. лактатацидозе (шок, гипоксия, сахарный диабет II типа, сердечная недостаточность, инфекции, отравление алкоголем).
Повышенная потеря гидрокарбонатов возможна с мочой (почечный ацидоз), или с некоторыми пищеварительными соками (панкреатический, кишечный).
Дыхательный (респираторный) ацидоз развивается при гиповентиляции лёгких, которая, независимо от вызвавшей её причины, приводит к росту парциального давления СО2 более 40 мм рт. ст. (гиперкапния). Это бывает при заболеваниях органов дыхания, гиповентиляции легких, угнетении дыхательного центра некоторыми препаратами, например, барбитуратами.
Метаболический алкалоз наблюдается при значительных потерях желудочного сока вследствие повторной рвоты, а также в результате потери протонов с мочой при гипокалиемии, при запорах (когда накапливаются щелочные продукты в кишечнике; ведь источником бикарбонат-анионов является поджелудочная железа, протоки которой открываются в 12-перстную кишку), а также при длительном приеме щелочной пищи и минеральной воды, соли которой подвергаются гидролизу по аниону.
Дыхательный (респираторный) алкалоз развивается вследствие гипервентиляции лёгких, приводящей к избыточному выведению СО2 из организма и понижению его парциального давления в крови менее 40 мм. рт. ст. (гипокапния). Это бывает при вдыхании разреженного воздуха, гипервентиляции легких, развитии тепловой одышки, чрезмерного возбуждения дыхательного центра вследствие поражения головного мозга.
При ацидозах в качестве экстренной меры используют внутривенное вливание 4 – 8 % гидрокарбоната натрия, 3,66%- ного раствора трисамина Н2NC(CH2OH)3 или 11 % лактата натрия. Последний, нейтрализуя кислоты, не выделяет СО2, что повышает его эффективность.
Алкалозы корректируются сложнее, особенно метаболические (связанные с нарушением систем пищеварения и выделения). Иногда используют 5 % раствор аскорбиновой кислоты, нейтрализованный бикарбонатом натрия до рН 6 – 7.
Щелочной резерв - это количество бикарбоната (NaHCО3) (точнее объем СО2, который может быть связан плазмой крови). Эту величину лишь условно можно рассматривать как показатель кислотно-щелочного равновесия, так как, несмотря на повышенное или пониженное содержание бикарбоната, при наличии соответствующих изменений Н2СО3 рН может оставаться совершенно нормальным.
Так как компенсаторные возможности посредством дыхания, первоначально используемые организмом, ограничены, решающая роль в поддержании постоянства переходит к почкам. Одной из основных задач почек является удаление из организма Н+-ионов в тех случаях, когда вследствие каких-либо причин в плазме наступает сдвиг в сторону ацидоза. Ацидоз не может быть скорригирован, если не будет удалено соответствующее количество Н+-ионов. Почки используют при этом 3 механизма:
1. Обмен ионов водорода на ионы натрия, которые, соединяясь с образующимися в канальцевых клетках анионами НСО3, полностью подвергаются обратному всасыванию в виде NaHCO3,
Предпосылкой выделения Н+-ионов с помощью этого механизма является активируемая карбоангидразой реакция СО2 + Н2О = Н2СО3, причем Н2СО3 распадается на ионы Н+ и НСО3-. При этом обмене ионов водорода на ионы натрия происходит обратное всасывание всего отфильтрованного в клубочках бикарбоната натрия.
2. Выделение с мочой ионов водорода и обратное всасывание ионов натрия происходит также путем превращения в дистальных отделах канальцев щелочной соли фосфата натрия (Na2HPО4) в кислую соль дифосфата натрия (NaHaPO4).
3. Образование солей аммония: аммиак, образующийся в дистальных отделах почечных канальцев из глутамина и других аминокислот, способствует выделению Н+-ионов и обратному всасыванию ионов натрия; происходит образование NH4Cl вследствие соединения аммиака с HCl. Интенсивность образования аммиака, необходимого для нейтрализации сильной НСl, тем больше, чем выше кислотность мочи.
Табл. 4.3
Основные параметры КОС
рН |
N ≈ 7,4 |
(среднее значение в артериальной крови) |
рСО2 |
40 мм. рт. ст. (парциальное давление СО2 в плазме крови) |
Этот компонент непосредственно отражает дыхательный компонент в регуляции КОС (КЩР). ↑(гиперкапния) наблюдается при гиповентиляции, что характерно для дыхательного ацидоза. ↓(гипокапния) наблюдается при гипервентиляции, что характерно для респираторного алкалоза. Однако, изменения рСО2 могут быть и следствием компенсации со стороны метаболических нарушений КОС. Чтобы отличить эти ситуации друг от друга, требуется рассмотреть рН и [НСО3-] |
рО2 |
95 мм. рт. ст. (парциальное давление в плазме крови) |
|
СБ или SB |
24 мэкв/л |
СБ – стандартный бикарбонат плазмы т.е. [НСО3-] ↓ - при метаболическом ацидозе, или при компенсации дыхательного алкалоза. ↑ - при метаболическом алкалозе или при компенсации дыхательного ацидоза. |
Дополнительные индексы
БО или ВВ (base buffers) |
Буферные основания. Это сумма всех анионов цельной крови, принадлежащих буферным системам. |
ДО или BD (base deficiency) |
Дефицит оснований. Это разница между практической и должной величиной БО при метаболическом ацидозе. Определяется как количество оснований, которое необходимо добавить к крови, чтобы довести ее рН до нормы (при рСО2 = 40 мм. рт. ст. t° = 38°C ) |
ИО или ВЕ (basе excess) |
Избыток оснований. Это разница между фактической и должной величинами БО при метаболическом алкалозе. |
В норме, условно говоря, не существует ни дефицита, ни избытка оснований (ни ДО, ни ИО). Фактически, это выражается в том, что разница должного и фактического БО находится в нормальных условиях в пределах ±2,3 мэкв/л. Выход этого показателя из коридора нормы типичен для метаболических нарушений КОС. Аномально высокие значения характерны для метаболического алкалоза. Аномально низкие – для метаболического ацидоза.
Лабораторно-практическая работа
Опыт 1. Сравнение буферной ёмкости сыворотки крови и фосфатной БС
Отмерить мл |
№ колбы |
|
|
№ 1 |
№ 2 |
Сыворотка крови (разведение 1:10) |
2,0 |
- |
Фосфатная БС (разведение 1:10), рН = 7,4 |
- |
2,0 |
Фенолфталеин (индикатор) |
2 капли |
2 капли |
Титровать 0,1 н р-ром NаОН до малинового окрашивания (рН = 9,0).
Результаты занести в таблицу
мл NаОН |
|
|
Буферную ёмкость рассчитать по формуле:
V р-ра NаОН×10(разведение)×[NаОН]/2(мл) (рНпосле титрования – рНисходное)
|
Буферная ёмкость |
Сыворотка |
|
Фосфатный буфер |
|
Заключение………………………………………………………………………
Окислительно-восстановительные реакции. Химия комплексных соединений
Типы окислительно-восстановительных (редокс) реакций
в организме человека
Окислительно-восстановительными называются реакции, протекающие с изменением степени окисления двух или более веществ.
Степень окисления – это условный заряд на атоме, если считать, что молекула создана по ионному механизму (или – это количество принятых или отданных электронов).
Восстановители – атомы, молекулы, ионы – отдающие электроны.
Окислители - атомы, молекулы, ионы – принимающие электроны.
Восстановители участвуют в процессе окисления, повышая свою степень окисления. Окислители - участвуют в процессе восстановления, понижая свою степень окисления.
Виды окислительно-восстановительных реакций:
1. Межмолекулярные - реакции, в которых окисляющиеся и восстанавливающиеся атомы находятся в молекулах разных веществ, например:
Н2S + Cl2 → S + 2HCl
2. Внутримолекулярные - реакции, в которых окисляющиеся и восстанавливающиеся атомы находятся в молекулах одного и того же вещества, например:
2H2O → 2H2 + O2
3. Диспропорционирование (самоокисление-самовосстановление) - реакции, в которых один и тот же элемент выступает и как окислитель, и как восстановитель, например:
Cl2 + H2O → HClO + HCl
4. Репропорционирование (конпропорционирование, контрдиспропорционирование) - реакции, в которых из двух различных степеней окисления одного и того же элемента получается одна степень окисления:
![]()
Типы окислительно-восстановительных реакций в организме человека:
Реакция дегидрирования: SH2 + HAD+ → S + HADH+H+
Потеря электрона:O20 + 1e → O2-
Перенос 2Н+ от восстановленного субстрата на молекулярный кислород: SH2 + O20 +2e → S + H2O
Присоединение кислорода к субстрату: SH2 + ½O20 +2ē → HO-S-H
Механизм возникновения электродного и
редокс-потенциалов. Уравнения Нернста-Петерса
Мерой окислительно-восстановительной способности веществ служат окислительно-восстановительные потенциалы. Рассмотрим механизм возникновения потенциала. При погружении химически активного металла (Zn, Al) в раствор его соли, например Zn в раствор ZnSO4, происходят дополнительное растворение металла в результате процесса окисления, образование пары, двойного электрического слоя на поверхности металла и возникновение потенциала пары Zn2+/Zn°.
Металл, погруженный в раствор своей соли, например цинк в растворе сульфата цинка, называют электродом первого рода. Это двухфазный электрод, который заряжается отрицательно. Потенциал образуется в результате реакции окисления (рис. 5.1).
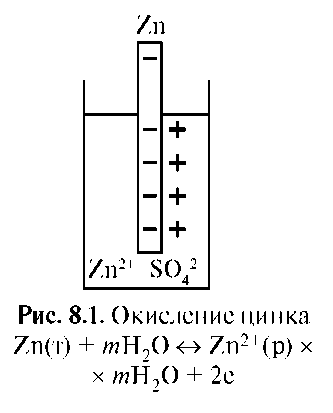
Рис. 5.1. Окисление цинка
Zn (т) + mH2O ↔ Zn2+ (р-р)×mH2O + 2ē
При погружении в раствор своей соли малоактивных металлов (Cu) наблюдается противоположный процесс. На границе металла с раствором соли происходит осаждение металла в результате процесса восстановления иона, обладающего высокой акцепторной способностью к электрону, что обусловлено высоким зарядом ядра и малым радиусом иона. Электрод заряжается положительно, в приэлектродном пространстве избыточные анионы соли формируют второй слой, возникает электродный потенциал пары Cu2+/Cu°. Потенциал образуется в результате процесса восстановления (рис. 5.2). Механизм, величина и знак электродного потенциала определяются строением атомов участников электродного процесса.
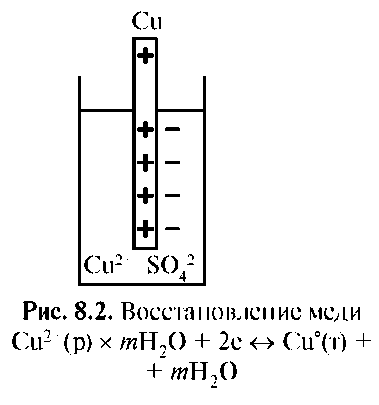
Рис. 5.2. Восстановление меди
Cu2+(р-р) ×mH2O + 2ē ↔ Cu(т) + mH2O
Итак, потенциал, который возникает на границе раздела металла с раствором в результате окислительного и восстановительного процессов, протекающих с участием металла (электрода) и образованием двойного электрического слоя называют электродным потенциалом.
|
Если отводить электроны с цинковой пластины на медную, то равновесие на пластинках нарушается. Для этого соединим цинковую и медную пластины, погруженные в растворы их солей, металлическим проводником, приэлектродные растворы - электролитным мостиком (трубка с раствором K2SO4), чтобы замкнуть цепь. На цинковом электроде протекает полуреакция окисления: Zn0(т) - 2ē → Zn2+(р-р), а на медном - полуреакция восстановления: Cu2+(р-р) + 2ē → Cu0(т)