Материал: 1_metodichka_po_khimii
Электрический ток обусловлен суммарной окислительно-восстановительной реакцией:
Zn0(т) + Cu2+(р-р) → Zn2+(р-р) + Cu0(т)
В-ль ок-ль
Окислительно-восстановительные потенциалы пары зависят от природы участников электродного процесса и соотношения равновесных концентраций окисленной и восстановленной форм участников электродного процесса в растворе, температуры раствора и описываются уравнением Нернста.
Количественной характеристикой окислительно-восстановительной системы является редокс-потенциал, возникающий на границе раздела фаз платина - водный раствор. Величина потенциала в единицах СИ измеряется в вольтах (В) и рассчитывается по уравнению Нернста-Петерса:
|
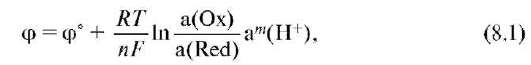
где а(Oх) и a(Red) - активность окисленной и восстановленной форм соответственно; R - универсальная газовая постоянная; Т - термодинамическая температура, К; F - постоянная Фарадея (96500 Кл/моль); n - число электронов, принимающих участие в элементарном редокс-процессе; а - активность ионов гидроксония; m - стехиометрический коэффициент перед ионом водорода в полуреакции. Величина φ° - стандартный редокс-потенциал, т.е. потенциал, измеренный при условиях а(Oх) = a(Red) = a(H+) = 1 и данной температуре.
Стандартный потенциал системы 2Н+/Н2 принят равным 0 В. Стандартные потенциалы являются справочными величинами, табулируются при температуре 298К. Сильнокислая среда не характерна для биологических систем, поэтому для характеристики процессов, протекающих в живых системах, чаще используют формальный потенциал, определяемый при условии а(Oх) = a(Red), pH 7,4 и температуре 310К (физиологический уровень). При записи потенциала пара указывается в виде дроби, причем окислитель записывается в числителе, а восстановитель в знаменателе.
Для 25°С (298К) после подстановки постоянных величин (R = 8,31 Дж/моль×град; F = 96500 Кл/моль) уравнение Нернста принимает следующий вид:
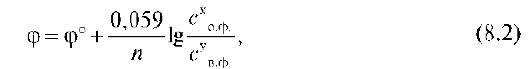
где φ°- стандартный окислительно-восстановительный потенциал пары, В; Со.ф. и Св.ф. - произведение равновесных концентраций окисленной и восстановленной форм соответственно; х и у - стехиометрические коэффициенты в уравнении полуреакций.
Редокс-системы делят на два типа:
1. в системе осуществляется только перенос электронов: Fe3++ē = Fe2+, Sn2+ - 2ē = Sn4+. Это изолированное окислительно-восстановительное равновесие;
2. системы, когда перенос электронов дополняется переносом протонов, т.е. наблюдается совмещенное равновесие разных типов: протолитическое (кислотно-основное) и окислительно-восстановительное с возможной конкуренцией двух частиц протонов и электронов. В биологических системах важные редокс-системы относятся к этому типу.
Примером системы второго типа является процесс утилизации перекиси водорода в организме: Н2О2 + 2Н+ + 2ē ↔ 2Н2О, а также восстановление в кислой среде многих окислителей, содержащих кислород: CrО42-, Cr2О72-, MnО4-. Например, MnО4- + 8Н+ + 5ē = = Mn2+ + 4Н2О. В данной полуреакции участвуют электроны и протоны.
Итак, окислительно-восстановительный потенциал (ОВП) – это потенциал системы, в которой активности окислительной и восстановительной форм данного вещества равны единице. ОВП измеряется с помощью окислительно-восстановительных электродов в сочетании со стандартными электродами сравнения.
В каждой окислительно-восстановительной реакции есть своя редокс-пара – эта пара имеет вещество в окисленной и восстановленной форме (Fe+3/Fe+2).
Количественной мерой активности редокс-пары является величина ее ОВП.
ОВПпары>>>окислитель
ОВПпары<<<восстановитель
ОВП зависит от:
Природы редокс-пары,
Концентрации
Температуры
Сравнительная сила окислителей и восстановителей.
Прогнозирование направления редокс-процессов по
величинам редокс-потенциалов
Окислительно-восстановительный потенциал является мерой окислительно-восстановительной способности веществ. Значение стандартных потенциалов пар указаны в справочных таблицах.
Стандартные потенциалы электродов (Е°), выступающих как восстановители по отношению к водороду, имеют знак «-», а знак «+» имеют стандартные потенциалы электродов, являющихся окислителями.
Металлы, расположенные в порядке возрастания их стандартных электродных потенциалов, образуют электрохимический ряд напряжений металлов: Li, Rb, К, Ва, Sr, Ca, Na, Mg, Al, Mn, Zn, Cr, Fe, Cd, Co, Ni, Sn, Pb, H, Sb, Bi, Cu, Hg, Ag, Pd, Pt, Au.
В ряду редокс-потенциалов отмечают следующие закономерности.
1. Если стандартный редокс-потенциал пары отрицателен, например φ°(Zn2+(р)/Zn°(т)) = -0,76 В, то по отношению к водородной паре, потенциал которой выше, данная пара выступает в качестве восстановителя (реакции окисления).
2. Если потенциал пары положителен, например φ°(Сu2+(р)/ Cu(т)) = +0,345 В по отношению к водородной или другой сопряженной паре, потенциал которой ниже, данная пара является окислителем (реакции восстановления).
3. Чем выше алгебраическая величина стандартного потенциала пары, тем выше окислительная способность окисленной формы и ниже восстановительная способность восстановленной формы этой пары. Снижение величины положительного потенциала и возрастание отрицательного соответствует падению окислительной и росту восстановительной активности. Например:
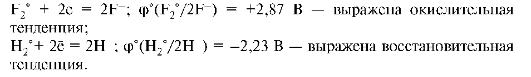
Сопоставление значений стандартных окислительно-восстановительных потенциалов позволяет ответить на вопрос: протекает ли та или иная окислительно-восстановительная реакция?
Разность между стандартными окислительными потенциалами окисленной и восстановленной полупар называют электродвижущей силой (ЭДС).
Е0 = Еок- Евосст
Количественным критерием оценки возможности протекания той или иной окислительно-восстановительной реакции является положительное значение разности стандартных окислительно-восстановительных потенциалов полуреакций окисления и восстановления.
Для установления возможности самопроизвольного протекания в стандартных условиях ОВР необходимо:
Рассчитать ЭДС реакции согласно уравнению Нернста
Е = Е0 + 0,0592/пlgCоф/Свф
Рассчитать энергию Гиббса
G0298= - п×F×E0
Если:
Е > 0, G < 0 - реакция протекает самопроизвольно
Е < 0, G > 0 – реакция протекает в обратном направлении
Е = 0 G = 0 - химическое равновесие
Физико-химические принципы транспорта электронов в
электронотранспортной цепи митохондрий
Все типы окислительно-восстановительных процессов происходят при окислении субстратов в митохондриях, на внутренних мембранах которых размещаются ансамбли из ферментов – дегидрогеназ, коферментов (НАД2, ФАД3, УБХ4), серии цитохромов b, с1, c и фермента – цитохромоксидазы. Они образуют систему клеточной дыхательной цепи, с помощью которой происходит эстафетная передача протонов и электронов от субстрата к молекулам кислорода, доставленным гемоглобином к клетке.
Каждый компонент дыхательной цепи характеризуется определённым значением окислительно-восстановительного потенциала. Движение электронов по дыхательной цепи происходит ступенчато от веществ с низким потенциалом (-0,32 В) к веществам с более высоким потенциалом (+0,82 В), поскольку любое соединение может отдать электроны только соединению с более высоким окислительно-восстановительным потенциалом (табл. 5.1).
Табл. 5.1
Стандартные редокс-потенциалы биомолекул дыхательной цепи
система |
полуреакция |
редокс-потенциал, В |
НАД+/НАДН+Н+ |
НАД+ + 2Н+ + 2 ē → НАДН+Н+ |
-0,32 |
ФАД/ФАД×Н2 |
ФАД+ + 2Н+ + 2 ē → ФАД×Н2 |
-0,22 |
УБХ/ УБХ×Н2 |
УБХ+ 2Н+ + 2 ē → УБХ×Н2 |
-0,04 |
цитохром b |
Fe3+ → Fe2+ |
0,07 |
цитохром с1 |
|
0,23 |
цитохром с |
|
0,25 |
цитохром а+а3 |
Cu2+ →Cu1+ |
0,55 |
О2/Н2О |
О2 + 4Н+ + 4 ē → 2Н2О |
0,82 |
Цепь тканевого дыхания можно представить в виде схемы:
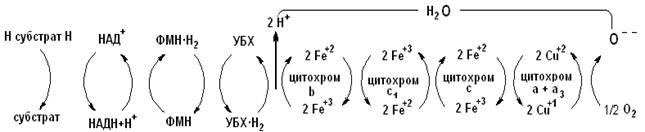
В результате биологического окисления (дегидрирования) два атома водорода (в виде двух протонов и двух электронов) от субстрата поступают в дыхательную цепь. Сначала происходит эстафетная передача протона и пары электронов молекуле НАД+, превращающейся в восстановленную форму НАДН+Н+, затем системе флавиновых оснований (ФАД/ФАД×Н2 или ФМН/ФМН×Н2), следующим акцептором двух протонов и двух электронов является убихинон (УБХ). Далее происходит передача только электронов: два электрона от УБХ×Н2 принимают на себя последовательно цитохромы в соответствии с величинами их редокс-потенциалов (табл. 5.1). Последний из компонентов – цитохромоксидаза переносит электроны непосредственно молекуле кислорода. Восстановленный кислород с двумя протонами, полученными от УБХ×Н2 образует молекулу воды.
½О2 + 2Н+ + 2 ē → Н2О
Необходимо отметить, что каждая молекула кислорода взаимодействует с двумя электронотранспортными цепями, поскольку в структуре цитохромов возможен только одноэлектронный перенос Fe3+ → Fe2+.
Особенностью функционирования дыхательной цепи ферментов является наличие в ней участков, где соседние компоненты резко отличаются значениями окислительно-восстановительных потенциалов, именно здесь происходит сопряжение окисления с фосфорилированием АДФ (это комплекс 1 – НАДН/убихинон, комплекс 3 – убихинон/цитохром с и комплекс 4 - цитохромоксидазный комплекс). Такой комплекс, встроенный в мембрану фосфолипида способен функционировать как протонный насос.
Основные положения координационной теории Вернера.
Природа химической связи в комплексных соединениях
Комплексными соединениями называются соединения, существующие как в кристаллическом состоянии, так и в растворе, особенностью которых является наличие центрального атома, окруженного лигандами. Комплексные соединения можно рассматривать как сложные соединения высшего порядка, состоящие из простых молекул, способных к самостоятельному существованию в растворе.
Координационную теорию Вернера рассмотрим на примере:
K3[Fe(CN)6]
внешняя и внутренняя сфера
Согласно данной теории, центральный атом или ион, в большинстве случаев в форме катиона (обычно положительно заряженный), координирует (т.е. близко располагает) вокруг себя некоторое число анионов или молекул, которые называются лигандами, (или аддендами – старое название). Простые положительно заряженные катионы в роли лигандов не выступают.
Центральный атом (комплексообразователь)
Образование комплексного иона или нейтрального комплекса можно представить себе в виде обратимой реакции общего типа:
M
+ n L
![]() [MLn]
[MLn]
где M – нейтральный атом, положительно или отрицательно заряженный условный ион, объединяющий (координирующий) вокруг себя другие атомы, ионы или молекулы L. Атом M получил название комплексообразователя или центрального атома.
В комплексных ионах [Cu(NH3)4]2+, [SiF6]2- , [Fe(CN)6]4- , [BF4]- комплексообразователями являются медь (II), кремний (IV), железо (II), бор (III). Чаще всего комплексообразователем служит атом элемента в положительной степени окисления.
Отрицательные условные ионы (т.е. атомы в отрицательной степени окисления) играют роль комплексообразователей сравнительно редко. Это, например, атом азота (III) в катионе аммония [NH4]+ и т.п.
Атом-комплексообразователь может обладать нулевой степенью окисления. Так, карбонильные комплексы никеля и железа, имеющие состав [Ni(CO)4] и [Fe(CO)5], содержат атомы никеля (0) и железа (0).
Комплексообразователь (выделен жирно) может участвовать в реакциях получения комплексов, как будучи одноатомным ионом, например:
Ag+ + 2NH3 [Ag(NH3)2]+;
Ag+ + 2CN- [Ag(CN)2]-
так и находясь в составе молекулы:
SiF4 + 2F- [SiF6]2-
PH3 + H+ [PH4]+;
BF3 + NH3 [B(NH3)F3]
В комплексной частице может быть два и более атомов-комплексообразователей. В этом случае говорят о многоядерных комплексах.
Комплексное соединение может включать несколько комплексных ионов, в каждом из которых содержится свой комплексообразователь. Например, в одноядерном комплексном соединении состава [K(H2O)6][Al(H2O)6](SO4)2 комплексообразователи K(I) и Al(III), а в [Cu(NH3)4][PtCl6] – Cu(II) и Pt(IV).
Лиганды
В комплексном ионе или нейтральном комплексе вокруг комплексообразователя координируются ионы, атомы или простые молекулы (L). Все эти частицы, имеющие химические связи с комплексообразователем, называются лигандами (от латинского «ligare» - связывать). В комплексных ионах [SnCl6]2- и [Fe(CN)6]4- лигандами являются ионы Cl- и CN-, а в нейтральном комплексе [Cr(NH3)3(NCS)3] лиганды – молекулы NH3 и ионы NCS-.