Материал: 1_metodichka_po_khimii
Подставляем для Кгидр:
![]()
откуда
[OH-]
= (Kгидр–![]() )1/2
)1/2
Концентрация ионов гидроксила в растворе соли слабой одноосновной кислоты и сильного однокислотного основания равна квадратному корню из произведения константы гидролиза соли на ее концентрацию.
Так
как
![]() ,
то [OH-]
= (
,
то [OH-]
= (![]() )1/2
)1/2
В тех случаях, когда константа диссоциации кислоты очень мала, нельзя пренебрегать в расчете частью ее анионов, связавшейся в недиссоциированные молекулы. В этом случае расчет ведут по более точному выражению
![]() ,
,
откуда
[OH-]
=
![]() .
.
II. Соли сильной одноосновной кислоты и слабого однокислотного основания. Примером такой соли является хлорид аммония. Он сильный электролит и диссоциирует полностью
NH4Cl → NH4+ + Cl-
Вода также частично диссоциирует:
H2O ↔ H+ + OH-
Столкновение ионов NH4+ с ионами ОН- приводит к образованию соединения NH4ОH, легко превращающееся в аммиак и воду. Общую схему процесса можно представить уравнением:
NH4Cl + H2O ↔ NH4+ + Cl- + OH- + H+ ↔ NH4OH + H+ + Cl-
Связывание ионов ОН- из раствора вызывает сдвиг диссоциации воды слева направо. Концентрация ионов Н+ в растворе растет. Таким образом, гидролиз солей слабых однокислотных оснований и сильных одноосновных кислот создает кислую среду.
Рассуждая аналогично I случаю, получим:
![]() .
.
Подставим вместо [NH4ОH] равную ей концентрацию ионов [Н+], а вместо [NH4+] приближенно равную ей концентрацию соли Ссоль.
Получим:
![]()
Если образующееся при гидролизе основание очень слабое, то расчет ведут по более точной формуле
![]() .
.
III. Соли слабой одноосновной кислоты и слабого однокислотного основания. При растворении ацетата аммония в воде наступает его практически полная диссоциация:
CH3COONH4 → NH4+ + CH3COO-
Столкновение ионов NH4+ и СН3СОО- с молекулами воды приводит к образованию слабо диссоциирующих молекул соответственно слабого основания NH4ОH и слабой кислоты СН3СООН по схеме:
CH3COONH4 + H2O ↔ NH4OH + CH3COOH
Так как образующиеся вещества – слабые электролиты, то в результате соли слабых кислот и слабых оснований подвергаются почти полному гидролизу, а реакция среды в растворах определяется соотношением силы кислоты и основания.
Применим к нему закон действия масс для момента равновесия
![]()
Это выражение можно упростить. Умножим числитель и знаменатель на ионное произведение воды
![]() .
.
Константы диссоциации основания и кислоты выражаются соответственно:
![]() ;
;
![]()
откуда следуют выражения для [NH4+] и [СН3СОО-]
![]() ,
,
![]() .
.
Чтобы получить формулу для расчета [Н+], проведем ряд последовательных преобразований. Из уравнения:
[NH4+] = [CH3COO-]; [CH3COOH] = [NH4OH]
Вместо [NH4ОH] подставим равную ей [СН3СООН], получим
![]()
Затем в константу диссоциации кислоты
![]()
введем вместо [СН3СОО-] равную ей [NН4+], получим:
![]()
Умножаем числитель и знаменатель соотношения на [Н+] и после сокращения [СН3СООН] и преобразований получим:
[H+]
=
![]()
Из формулы видно, что концентрация ионов водорода в растворе соли слабой кислоты и слабого основания не зависит от концентрации раствора соли, а только от соотношения констант диссоциации кислоты и основания.
IV. Соль сильного основания и сильной кислоты. Такая соль в растворе диссоциирует полностью, например хлорид калия KCl → K+ + Cl-
В отличие от рассмотренных выше случаев ионы соли – сильного электролита – не могут образовать с водой слабых электролитов, а раз нет взаимодействия с водой, то, следовательно, соли сильных кислот и сильных оснований гидролизу не подвергаются. Среда в растворе остается нейтральной.
Гидролиз многокислотных или многоосновных солей протекаент по ступеням.
Для характеристики гидролиза различных солей вводятся две величины.
Константа гидролиза (Кгидр) равна в момент динамического равновесия отношению произведения концентраций продуктов гидролиза к произведению концентраций гидролизующихся ионов соли.
Степень
гидролиза
(αгидр)
– отношение числа гидролизованных
молекул соли к числу растворенных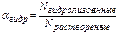
Константы гидролиза соли растут по мере уменьшения констант диссоциации кислот и оснований, образующихся в результате процесса. Следовательно, возрастает и количество гидролизованных молекул. Степень гидролиза соли возрастает по мере уменьшения констант диссоциации кислот и оснований, образующихся в результате процесса.
4.4. Амфолиты. Изоэлектрическая точка
Амфолиты - молекулы, в структуре которых присутствуют как кислотные, так и основные группы (например, аминокислоты, белки). Амфолиты способны присоединять или отщеплять протоны, превращаясь либо в положительно, либо в отрицательно заряженные ионы, причем суммарный электрич. заряд амфолита равен нулю. Этот pH, при котором заряд амфолита равен нулю, обозначается как изоэлектрическая точка молекулы. В изоэлектрической точке амфолит не перемещается в электрическом поле.
Амфолиты образуют растворы с хорошими буферными свойствами. Благодаря способности к выборочной ионизации они противодействуют изменению pH при добавлении кислоты или основания. В присутствии кислот они принимают на себя протоны, удаляя последние из раствора, и противодействуют повышению его кислотности. При добавлении оснований амфолиты высвобождают ионы водорода в раствор, препятствуя возрастанию pH, и тем сохраняя его равновесие.
4.5. Понятие о буферном действии, гомеостазе и стационарном состоянии живого организма
Организм можно определить как физико-химическую систему, существующую в окружающей среде в стационарном состоянии. Именно эта способность живых систем сохранять стационарное состояние в условиях непрерывно меняющейся среды и обусловливает их выживание. Для обеспечения стационарного состояния у всех организмов - от морфологически самых простых до наиболее сложных - выработались разнообразные анатомические, физиологические и поведенческие приспособления, служащие одной цели - сохранению постоянства внутренней среды.
Гомеостаз - относительное динамическое постоянство внутренней среды (крови, лимфы, тканевой жидкости) и устойчивость основных физиологических функций (кровообращения, дыхания, терморегуляции, обмена веществ и т.д.) организма человека и животных. Регуляторные механизмы, поддерживающие физиологическое состояние или свойства клеток, органов и систем целостного организма на оптимальном уровне, называются гомеостатическими. Учение о гомеостазе - это учение о жизненных процессах, имеющих только одну цель: поддержание постоянства условий жизни во внутренней среде, как необходимый элемент свободной и независимой жизни.
Способность раствора поддерживать определенное значение рН называется буферным действием.
Буферным действием обладают:
1. Система слабая кислота – ее соль с сильным основанием, а также сочетание кислой и средней солей слабых кислот или двух кислых солей;
2. Система слабое основание – его соль с сильной кислотой;
3. Ионы и молекулы амфолитов – аминокислотные и белковые системы.
Основная функция буферных систем - предотвращение значительных сдвигов рН путём взаимодействия буфера, как с кислотой, так и с основанием. Действие буферных систем в организме направлено преимущественно на нейтрализацию образующихся кислот.
В организме одновременно существует несколько различных буферных систем. В функциональном плане их можно разделить на бикарбонатную и небикарбонатную. Небикарбонатная буферная система включает гемоглобин, различные белки и фосфаты. Она наиболее активно действует в крови и внутри клеток.
4.6. Буферные системы: определение, классификация
Слабые кислоты и основания, в отличие от сильных (диссоциирующих практически полностью), распадаются на ионы в очень небольшой степени. Поэтому, например, в растворе слабой кислоты, можно выделить:
общую кислотность – концентрация растворённой кислоты, которую можно определить титрованием раствором щёлочи до полной нейтрализации;
активную кислотность – концентрации свободных протонов в растворе;
потенциальную или резервную кислотность, заключённоую в недиссоциированных молекулах кислоты.
Аналогично, слабые основания обладают тремя видами щёлочности.
Кроме того, слабые электролиты подчиняются закону разведения Оствальда, согласно которому степень диссоциации слабого электролита обратно пропорциональна корню квадратному из его концентрации:
α
=![]() ,
,
где К – константа диссоциации, С – молярная концентрация;
или прямо пропорциональна корню квадратному из его разведения:
α
=![]() , где
V – разведение
, где
V – разведение
Как вы помните из курса средней школы, реакция среды в растворах солей определяется их способностью к гидролизу. Так, соли, образованные слабой кислотой и сильным основанием, подвергаясь гидролизу по аниону, смещают равновесие диссоциации воды в сторону образования гидроксид-анионов. Среда становится щелочной. Например:
СН3СОО- + Na+ + Н2О → СН3СООН + Na+ + ОН-
Соли, образованные слабым основанием и сильной кислотой, подвергаясь гидролизу по катиону, смешает равновесие диссоциации воды в сторону образования протонов.
Например: NН4+ + Сl- + Н2О → NН4ОН + H+ + Cl-
Буферные системы (БС) – водные растворы, препятствующие изменению рН при добавлении небольших количеств сильных кислот, оснований, а также при разбавлении и концентрировании.
Состав любой БС включает в себя 2 компонента в следующих вариантах:
а) слабая кислота и её соль, образованная сильным основанием;
б) слабое основание и его соль, образованная сильной кислотой.
Пример БС первого типа – ацетатный буфер:
СН3СООН/СН3СОО-+Na+
где СН3СООН – слабая кислота, а СН3СОО-+Na+ - соль, образованная сильным основанием (NaOH).
Пример БС второго типа – аммиачный буфер:
NH4OH/NH4+ + Cl-
где NH4OH – слабое основание, NH4+ + Cl- - его соль, образованная сильной кислотой (HCl).
Важнейшим компонентом БС является именно слабый электролит. Он обеспечивает резервную кислотность или основность.
Классификация кислотно-основных буферных систем:
Буферные системы могут быть четырех типов:
1. Слабая кислота и ее анион А- /НА:
ацетатная буферная система СН3СОО-/СН3СООН в растворе СН3СООNa и СН3СООН, область действия рН = 3,8-5,8.
Водород-карбонатная система НСО3-/Н2СО3 в растворе NaНСО3 и Н2СО3, область её действия – рН = 5,4-7,4.