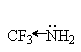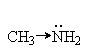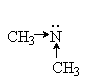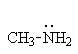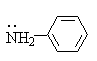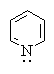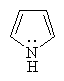Материал: 1_metodichka_po_khimii
Аналогичное влияние оказывают заместители на кислотность спиртов и фенолов.
Основания Бренстеда.
При одинаковом структурном окружении для элементов одного периода с ростом электроотрицательности атома при основном центре основность соединений уменьшается:
аммониевые основания > оксониевые основания
|
ROH |
RNH2 |
|
~2 |
~10 |
Снижение основности связано с тем, что более электроотрицательный атом прочнее удерживает неподеленную пару электронов, которую он должен отдать на образование связи с протоном.
Увеличения s-характера гибридных орбиталей приводит к снижению основности:
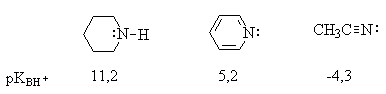
Для элементов одной подгруппы с возрастанием заряда ядра основность уменьшается:
оксониевые основания > сульфониевые основания
Введение электронодонорных заместителей увеличивает, а введение электроакцепторных - понижает основность. Так, электронодонорные заместители увеличивают основность алифатических и ароматических аминов, увеличивая склонность электронной пары азота к атаке протона. Электроноакцепторные заместители, напротив, снижают электронную плотность неподеленной пары электронов азота и делают ее менее восприимчивой для атаки протоном:
|
|
|
|
|
|
|
9,2 |
10,6 |
10,7 |
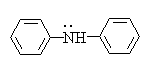
Если свободная пара электронов азота находится в сопряжение с двойной связью или ароматическим кольцом, основность снижается. Так, в анилине свободная пара электронов азота сопряжена с ароматическим кольцом.
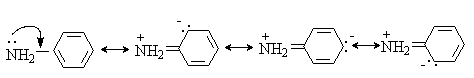
Протонирование анилина приводит к нарушению сопряжения и энергетически менее выгодно, чем протонирование алифатических аминов.
|
|
|
|
|
10,6 |
4,6 |
0,9 |
Амиды карбоновых кислот являются очень слабыми основаниями из-за сопряжения пары электронов азота с карбонильной группой. В результате атом азота приобретает частичный положительный, а атом кислорода – частичный отрицательный заряд, и протонирование амидов происходит, как правило, по атому кислорода.
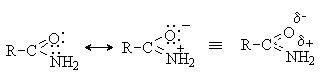
Основность азотсодержащих гетероциклических соединений также определяется доступностью пары электронов азота для атаки протона. Высокой основностью обладают насыщенные азотсодержащие гетероциклы, в которых атом азота находится в состоянии sp3-гибридизации. Основность пиридиниевого атома азота (sp2-гибридизация) ниже. Наконец, пиррольный атом азота практических лишен основных свойств, так как его протонирование означает разрушение ароматической гетероциклической системы:
|
|
|
|
pKa |
11,27 |
5,2 |
- 0.3 |
Кислоты и основания Льюиса
Дж. Льюисом была предложена более общая теория кислот и оснований. Основания Льюиса – это доноры пары электронов (спирты, алкоголят-анионы, простые эфиры, амины и т.д.). Кислоты Льюиса – это акцепторы пары электронов, т.е. соединения, имеющие вакантную орбиталь (ион водорода и катионы металлов: H+, Ag+, Na+, Fe2+; галогениды элементов второго и третьего периодов BF3, AlCl3, FeCl3, ZnCl2; галогены; соединения олова и серы: SnCl4, SO3).
Таким образом, основания Бренстеда и Льюиса – это одни и те же частицы. Однако основность по Бренстеду - способность присоединять только протон, в то время как основность по Льюису – понятие более широкое и означает способность к взаимодействию с любой частицей, имеющей низколежащую свободную орбиталь.
Кислотно-основное взаимодействие по Льюису - доноро-акцепторное взаимодействие и любую гетеролитическую реакцию можно представить как взаимодействие кислоты и основания Льюиса:
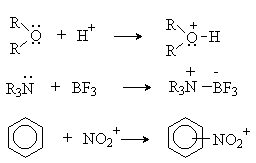
Единой шкалы для сравнения силы кислот и оснований Льюиса не существует, так как их относительная сила будет зависеть от того, какое вещество взято за стандарт (для кислот и оснований Бренстеда таким стандартом является вода). Для оценки легкости протекания кислотно-основного взаимодействия по Льюису Р. Пирсоном была предложена качественная теория «жестких» и «мягких» кислот и оснований (табл. 4.1).
Табл. 4.1
Жесткие и мягкие кислоты и основания
Жесткие |
Промежуточные |
Мягкие |
Кислоты |
||
H+, Na+, K+, Mg2+, Ca2+, Al3+, Fe3+, BF3, AlCl3, RC+=O |
Cu2+, Fe2+, Zn2+, R3C+ |
Ag+, Hg2+, I2 |
Основания |
||
H2O, OH-, F-, ROH, RO-, R2O, NH3, RNH2 |
ArNH2, Br-, C5H5N |
R2S, RSH, RS-, I-, H-, C2H4, C6H6 |
Жесткие основания обладают высокой электроотрицательностью и низкой поляризуемостью. Они трудно окисляются. Их высшие занятые молекулярные орбитали (ВЗМО) имеют низкую энергию.
Мягкие основания имеют низкую электроотрицательность и высокую поляризуемость. Они легко окисляются. Их высшие занятые молекулярные орбитали (ВЗМО) имеют высокую энергию.
Жесткие кислоты имеют высокую электроотрицательность и низкую поляризуемость. Они трудно восстанавливаются. Их низшие свободные молекулярные орбитали (НСМО) имеют низкую энергию.
Мягкие кислоты обладают низкой электроотрицательностью и высокой поляризуемостью. Они легко восстанавливаются. Их низшие свободные молекулярные орбитали (НСМО) имеют высокую энергию.
Самая жесткая кислота - Н+, самая мягкая – СН3Hg+. Наиболее жесткие основания – F- и OH-, наиболее мягкие – I- и Н-.
Принцип жестких и мягких кислот и оснований Пирсона (принцип ЖМКО): жесткие кислоты преимущественно взаимодействуют с жесткими основаниями, а мягкие кислоты – с мягкими основаниями. Это выражается в больших скоростях реакций и в образовании более устойчивых соединений, так как взаимодействие между близкими по энергии орбиталями эффективнее, чем взаимодействие между орбиталями, значительно различающимися по энергии.
Принцип ЖМКО используют для определения преимущественного направления конкурирующих процессов (реакции элиминирования и нуклеофильного замещения, реакции с участием амбидентных нуклеофилов); для направленного создания детоксикантов и лекарственных препаратов.
4.2. Ионизация слабых кислот и оснований. Константа диссоциации слабых кислот и оснований. Закон разведения Оствальда
Слабые кислоты: H2S, HF, CH3COOH, HNO2 (HnЭOm m-n<2)
Слабые
основания: NH4OH,
Me(OH)n (Me-![]() ,
кроме щелочных и щелочно земельных).
,
кроме щелочных и щелочно земельных).
Слабые кислоты и основания диссоциируют обратимо, равновесно, по ступеням, причём каждая последующая ступень протекает слабее предыдущей. Количественно диссоциацию слабых электролитов выражают с помощью α:
![]()
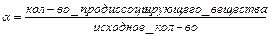
![]() -
степень электролитической диссоциации,
Kд - константа диссоциации (константа
равновесия). Константа диссоциации -
вид константы равновесия, которая
показывает склонность к диссоциации.
-
степень электролитической диссоциации,
Kд - константа диссоциации (константа
равновесия). Константа диссоциации -
вид константы равновесия, которая
показывает склонность к диссоциации.
<<1 и Kд<1
Диссоциация протекает с участием полярных молекул Н2О. Чем их больше, тем в большей степени протекает диссоциация.
Диссоциация слабой кислоты:
Диссоциация CH3COOH происходит в 1 стадию:
CH3COOH↔CH3COO-+Н+;
![]()
Дисоциация H3AsO4 протекает в 3 стадии:
1ст. H3AsO4↔H++ H2AsO4-
Кд1= C(H2AsO4-)×C(H+)/C(H3AsO4)=6×10-3
2ст. H2AsO4↔H++ HAsO4-2
Кд2=1×10-8
3ст. HAsO4↔H++ AsO4-3
Кg3=3×10-12
Кд1> Кд2 >Кд3>
α1> α2> α3
Диссоциация слабых оснований протекает аналогично
NH4OH↔NH4++OH-
Кд=1,7×10-5
Закон разбавления Оствальда.
Закон:
![]() -степень
электролитической диссоциации слабых
электролитов, увеличивается при
разбавлении раствора.
-степень
электролитической диссоциации слабых
электролитов, увеличивается при
разбавлении раствора.
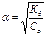 ;
;
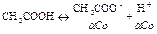
Со
– исходные вещества;
![]() –
продиссоциированные вещества
–
продиссоциированные вещества
Со-
![]() -
не диссоциированные вещества;
-
не диссоциированные вещества;
![]()
4.3. Гидролиз солей. Степень и константа гидролиза
Гидролизом называют реакции взаимодействия веществ с водой, приводящие к образованию слабодиссоциирующих веществ: слабых кислот или оснований, кислых или основных солей. Результат гидролиза можно расценивать как нарушение равновесия диссоциации H2O. Рассмотрим процессы при растворении солей в воде. Соли, как правило, – сильные электролиты, поэтому происходит их полная диссоциация на ионы, которые, в свою очередь, могут взаимодействовать с ионами Н+ или ОН- воды.
Следовательно, гидролиз солей протекает за счет взаимодействия ионов соли с водой. Этот процесс – частный случай реакций ионного обмена, когда в качестве реагента выступает вода.
В зависимости от катионов и анионов соли можно разбить на ряд групп, различающихся между собой по характеру образующих эти соли кислот и оснований:

I. Соли слабой одноосновной кислоты и сильного однокислотного основания. Например, растворяется ацетат калия. Являясь сильным электролитом, он полностью диссоциирует на ионы, но вода также частично диссоциирует. Возможно возникновение следующего процесса:
CH3COOK + H2O ↔ K+ + CH3COO- + OH- + H+ ↔ CH3COOH + K+ + OH-
Так как уксусная кислота – слабый электролит, то при столкновении ее кислотных остатков с ионами Н+ воды, образуются недиссоциированные молекулы уксусной кислоты. Удаление из раствора части ионов Н+ вызывает сдвиг равновесия процесса диссоциации воды слева направо. Содержание ионов ОН- в растворе нарастает. Раствор приобретает щелочную реакцию.
В момент достижения равновесия применение закона действия масс приводит к выражению:
![]() ,
,
[H2O] в разбавленных растворах – величина постоянная, поэтому произведение К [H2O] – тоже константа. Ее называют константой гидролиза Кгидр:
![]()
Константу гидролиза можно выразить через ионное произведение воды и константу диссоциации кислоты. Для этого умножим числитель и знаменатель на [H+] и запишем:
![]()
В результате гидролиза число образующихся молекул слабой кислоты равно числу оставшихся от молекул воды несвязанных ионов -
[ОН-]:[СН3СООН] = [ОН-]
Концентрация ионов соли практически равна концентрации этой соли, так как сильные электролиты диссоциируют полностью:
[CH3COO-]
=
![]()
где
![]() –
концентрация соли в растворе.
–
концентрация соли в растворе.