Материал: 1_metodichka_po_khimii
3.9. Гетерогенные равновесия. Константа растворимости.
Условия образования и растворения осадков
Согласно теории сильных электролитов, при растворении твердых веществ, кристаллы которых построены из ионов, в раствор переходят не молекулы, а образующие кристаллическую решетку ионы. Поэтому в насыщенном растворе таких соединений равновесие устанавливается между перешедшими в раствор ионами и твердой фазой (осадком) растворенного вещества. При этом протекают два взаимно противоположных процесса: переход ионов из осадка в раствор (растворение) и из раствора в осадок (кристаллизация).
Насыщенные растворы труднорастворимых электролитов являются сильно разбавленными. Их ионная сила мала, поэтому можно считать, что коэффициенты активности ионов таких электролитов в растворе равны единице, а сами их активности численно совпадают с молярными концентрациями.
В насыщенном растворе малорастворимой соли хлорида серебра между осадком AgCl и находящимися в жидкой фазе ионами Ag+ и Cl– устанавливается подвижное гетерогенное равновесие:
AgCl(т) ↔Ag+(р) + Cl–(р)
Согласно закону действующих масс, количественно оно характеризуется константой равновесия:
Kравн. = (c(Ag+(p)) × c(Cl–(p))) / c(AgCl(т))
где – c(Ag+(p)) и c(Cl-(p)) – равновесные молярные концентрации ионов Ag+ и Cl– в насыщенном растворе AgCl; c(AgCl(т)) – концентрация AgCl в твердой фазе (осадке).
Избавившись от дроби, выражение для Kравн. можно записать следующим образом:
Kравн. × c(AgCl(т)) = c(Ag+(p)) × c(Cl–(p))
Так как концентрация твердого вещества c(AgCl(т)) есть величина постоянная, то левая часть данного уравнения при неизменных внешних условиях (температуре, давлении) тоже будет являться постоянной величиной. Произведение этих констант (Kравн. × c(AgCl(т))) называют иначе константой растворимости и обозначают Ks (нижний индекс «s» от англ. solubility – растворимость):
Ks = c(Ag+(p)) × c(Cl–(p))
Условия образования и растворения осадков:
АВтв↔А++В-
Осадок образуется тогда, когда произведение концентрации ионов в растворе больше константы растворимости:
[А][В]>Ks
Осадок растворяется, если: [А][В]< Ks
Растворимость трудно растворимых веществ зависит от:
Введения в раствор электролита, содержащего одноименный ион с осадком;
Присутствия посторонних электролитов (солевой эффект);
Присутствия веществ, способных образовывать растворимые комплексы с осадком.
Основные типы химических равновесий и процессов в функционировании живых систем
4.1. Протолитическая теория кислот и оснований. Протолитические
реакции. Понятия о кислотах и основаниях
В протолитической теории кислот и оснований выделяется особая группа веществ - протолитов, взаимодействие между которыми осуществляется при передаче протона Н+ (от одного к другому).
Вещества, которые отдают протон, являются кислотами, а вещества, которые протон присоединяют - основаниями.
Ион водорода - протон - обладает уникальностью, то есть отличается от всех других ионов:
1. обладает малыми размерами (в 10000 раз меньше других);
2. обладает высокой подвижностью;
3. единственный ион, у которого отсутствуют электронные оболочки; он может внедряться в электронные оболочки других атомов, образуя водородную связь.
При растворении НСl в Н2О наблюдается протолитическое взаимодействие: НСl ↔ Н+ + Сl- или
НС1 + Н2О↔ Н3О+ + Сl-
Н3О+ - это ион гидроксония
Согласно этой теории, все кислоты делятся на несколько групп:
1. нейтральные: H2SO4, HC1, Н2О;
2. анионные: HSО4-, H2PО4-, НРО42-
3. катионные: NH4+, H3О+.
Основания:
1. нейтральные: Н2О, NH3;
2. анионные: CN-, СН3СОО-.
Некоторые вещества обладают амфотерностью, например, вода:
Н2О + Н2SO4 ↔ H3O+ + HSO4-
основание кислота кислота основание
Н2O + :NH3 ↔ NH4+ + ОН-
кислота основание кислота основание
Для характеристики протолитических свойств растворителей используется понятие «сродства к протону» - это энергия, которая выделяется при присоединении протона к одной молекуле растворителя. В порядке уменьшения сродства к протону все растворители образуют ряд, например:
NH3; H2О; C2H5OH; HCN; CH3COOH; HNО3; H2SО4 - уменьшение сродства к H+, усиление кислотных свойств. Таким образом, любой член этого ряда является кислотой ко всем предыдущим членам этого ряда, например:
С2Н5ОН + HCN ↔ С2Н5ОН2+ + CN-
основание кислота
Наибольшим сродством к протону обладает аммиак (NH3) - он всегда будет основанием. Например, при растворении спирта в аммиаке:
С2Н5ОН + NH3 → NH4+ +С2Н5О-
кислота основание
Центральным понятием протолитической теории является протолитическая реакция. Это реакция переноса протона от кислоты к основанию. Первоначально было предложено так называть перенос протона от молекулы кислоты к молекуле растворителя. Прочие реакции переноса протона называли прототропными. В последнее время протолитическими называют любые реакции переноса протона.
После потери протона оставшаяся часть молекулы кислоты становится основанием. Вместе они составляют сопряженную кислотно-основную пару. Такие пары частиц записывают в виде дроби: HCl/Cl-, H2SO4/HSO4-, NH4+/NH3.
Протонная теория кислот и оснований Бренстеда
Кислоты Бренстеда – это соединения, способные отдавать протон (доноры протона). Основания Бренстеда – это соединения, способные присоединять протон (акцепторы протона). Для взаимодействия с протоном основание должно иметь свободную пару электронов или электроны π-связи.
Кислоты и основания образуют сопряженные кислотно-основные пары, например:
CH3COOH + H2O ↔ CH3COO- + H3O+
кислота1 основание2 основание1 кислота2
CH3NH2 + H2O ↔ CH3NH3+ + OH-
основание1 кислота2 кислота1 основание2
В общем виде: Н-А + :В ↔ :А + Н-В
кислота1 основание2 основание1 кислота2
|
|
|
|
|
|
|
|
|
|
|
|
Сила кислоты НА будет зависеть от силы основания :В. Поэтому для создания единой шкалы силу кислот и оснований Бренстеда определяют относительно воды, которая является амфотерным соединением и может проявлять и кислотные, и основные свойства.
Сила кислот определяется константой равновесия их взаимодействия с водой как основанием, например:
CH3COOH + H2O CH3COO- + H3O+
![]()
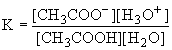
Так как в разбавленных растворах [H2O]=const, то ее можно внести в константу равновесия, которую называют константой кислотности:
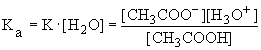
На практике чаще пользуются величинами pKa = - lg Ka. Чем меньше величина pKa, тем сильнее кислота.
Сила оснований определяется константой равновесия взаимодействия их с водой как кислотой:
RNH2 + H2O RNH3+ + OH-
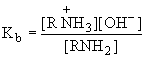 -
константа основности.
-
константа основности.
Для
сопряженных кислоты и основания Ka×Kb=Kw.
Таким образом, в
сопряженной
кислотно-основной паре, чем сильнее
кислота, тем слабее основание и наоборот.
Силу основания чаще выражают не константой
основности, а константой кислотности
сопряженной кислоты ![]() .
Например, для основания RNH2
величина
-
это константа кислотности сопряженной
кислоты
.
Например, для основания RNH2
величина
-
это константа кислотности сопряженной
кислоты ![]() :
:
RNH3+ + H2O RNH2 + H3О+
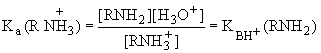
На
практике чаще пользуются величиной ![]() .
Чем больше величина
.
Чем больше величина ![]() ,
тем сильнее основание.
,
тем сильнее основание.
Классификация органических кислот и оснований.
Кислоты и основания Бренстеда классифицируют по природе атома при кислотном или основном центре.
В зависимости от природы элемента, с которым связан протон, различают четыре основных типа органических кислот Бренстеда:
O-H – кислоты - карбоновые кислоты, спирты, фенолы;
S-H – кислоты - тиолы;
N-H – кислоты - амины, амиды, имиды;
C-H – кислоты - углеводороды и их производные.
В зависимости от природы атома, к неподеленной паре электронов которого присоединяется протон, основания Бренстеда делят на три основных типа:
аммониевые основания - амины, нитрилы, азотсодержащие гетероциклические соединения;
оксониевые основания - спирты, простые эфиры, альдегиды, кетоны, карбоновые кислоты и их функциональные производные;
сульфониевые основания - тиолы, сульфиды.
Особый тип оснований Бренстеда представляют π-основания, в которых центром основности являются электроны π-связи (алкены, арены).
Влияние структурных факторов на относительную силу кислот и оснований.
Сила кислоты или основания определяется положением равновесия кислотно-основного взаимодействия и зависит от разности свободных энергий исходных и конечных соединений. Поэтому факторы, которые стабилизируют сопряженное основание в большей степени, чем кислоту, увеличивают кислотность и уменьшают основность. Факторы, стабилизирующие преимущественно кислоту по сравнению с основанием, действуют в противоположном направлении. Поскольку сопряженные основания, как правило, несут отрицательный заряд, то увеличению кислотности способствуют факторы, стабилизирующие анион.
Влияние строения на силу кислот и оснований.
Кислоты Бренстеда.
Сила кислоты зависит от природы атома при кислотном центре и от его структурного окружения. Для оценки относительной силы кислот важны такие характеристики атома при кислотном центре как его электроотрицательность и поляризуемость.
При прочих равных условиях для элементов одного периода с ростом электроотрицательности атома кислотность соединений увеличивается, так как высокая электроотрицательность атома при кислотном центре стабилизирует образующийся при отщеплении протона анион. Так, кислотность уменьшается в ряду:
OH-кислоты> NH-кислоты> CH-кислоты
|
CH3O-H |
CH3NH-H |
CH3CH2-H |
pKa |
16 |
30 |
40 |
Электроотрицательность атома зависит не только от его природы, но и от типа гибридизации и возрастает по мере увеличения s-характера гибридных орбиталей. Параллельно возрастает кислотность соединений:
|
СH3CH2-H |
CH2=CH-H |
|
pKa |
40 |
36 |
25 |
Для элементов одной подгруппы с возрастанием заряда ядра кислотность соединений увеличивается:
OH-кислоты < SH-кислоты
|
CH3O-H |
CH3S-H |
pKa |
16,0 |
10,5 |
Увеличение кислотности соединений, несмотря на снижение электроотрицательности атомов в подгруппе, связано с увеличением их поляризуемости по мере возрастания радиуса атома. Большая поляризуемость атома способствует лучшей делокализации отрицательного заряда и повышению стабильности сопряженного основания.
При одинаковой природе атома при кислотном центре сила кислоты определяется его структурным окружением. Увеличению силы кислоты способствует делокализация отрицательного заряда в сопряженном основании (анионе) и его рассредоточение на большем количестве атомов.
Так, карбоновые кислоты – одни из самых сильных органических кислот. Их сила обусловлена стабилизацией карбоксилат-аниона за счет делокализации отрицательного заряда в сопряженной системе. В результате отрицательный заряд в карбоксилат-анионе рассредоточен между двумя атомами кислорода, а обе связи С-O абсолютно равноценны:
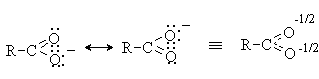
Фенолы являются более сильными кислотами, чем спирты, за счет резонансной стабилизации фенолят-аниона, отрицательный заряд которого делокализован по ароматическому кольцу:
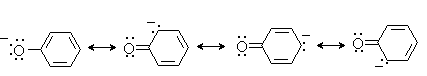
В результате по силе органические OH-кислоты могут быть расположены в следующий ряд:
|
ROH |
< |
H2O |
< |
ArOH |
< |
RCOOH |
pKa |
16-17 |
|
15,7 |
|
8-11 |
|
4-5 |
Введение заместителя в связанный с кислотным центром углеводородный радикал влияет на силу кислоты. Электроноакцепторные заместители увеличивают, а электронодонорные - уменьшают кислотность. Влияние электроноакцепторных заместителей связано с их способностью делокализовать отрицательный заряд и, тем самым стабилизировать сопряженное основание (анион). Влияние электронодонорных заместителей, напротив, приводит к дестабилизации аниона.
Электроноакцепторные заместители увеличивают силу алифатических и ароматических карбоновых кислот, электронодонорные заместители действуют в противоположном направлении:
|
Cl-CH2-COOH |
H-COOH |
CH3-COOH |
|
|||
pKa |
2,8 |
3,7 |
4,7 |
|
|||
|
|
|
|
||||
|
+M > -I |
|
-M и –I |
||||
pKa |
4,47 |
4,20 |
3,43 |
||||